Clear Sky Science · pl
Interferon-β i FTY720 łagodzą postępujące zapalenie OUN poprzez sygnalizację astrocytów związaną z SOCS1
Dlaczego to badanie ma znaczenie dla osób ze stwardnieniem rozsianym
Dla wielu osób ze stwardnieniem rozsianym (SR) największym lękiem nie są wczesne rzuty, lecz powolna, postępująca utrata funkcji, która może nastąpić później. W tej późniejszej, postępującej fazie uszkodzenia w mózgu i rdzeniu kręgowym postępują nawet wtedy, gdy standardowe leki ukierunkowane na układ odpornościowy we krwi działają prawidłowo. W pracy tej badano sposób dotarcia do tej „ukrytej” zapalnej aktywności przez połączenie istniejącego leku doustnego na SR z formą długo stosowanego leku podawaną bezpośrednio w kierunku mózgu.
Przewlekła choroba mózgu z ograniczonymi opcjami
SR to choroba autoimmunologiczna, w której własne komórki odpornościowe organizmu atakują osłonkę włókien nerwowych, prowadząc do zaburzeń widzenia, osłabienia i innych objawów neurologicznych. Na początku objawy zwykle pojawiają się i ustępują. Z upływem czasu wielu pacjentów wchodzi w fazę postępującą, charakteryzującą się stopniową, często nieodwracalną niepełnosprawnością. W tej fazie bariera krew–mózg staje się trudniejsza do przeniknięcia dla leków, a szkodliwa aktywność komórek rezydujących w mózgu, zwanych glejem — w szczególności astrocytów i mikrogleju — odgrywa coraz większą rolę. Obecne terapie, które głównie działają przez blokowanie komórek odpornościowych we krwi, oferują jedynie ograniczoną pomoc, gdy ta faza się utrwali.
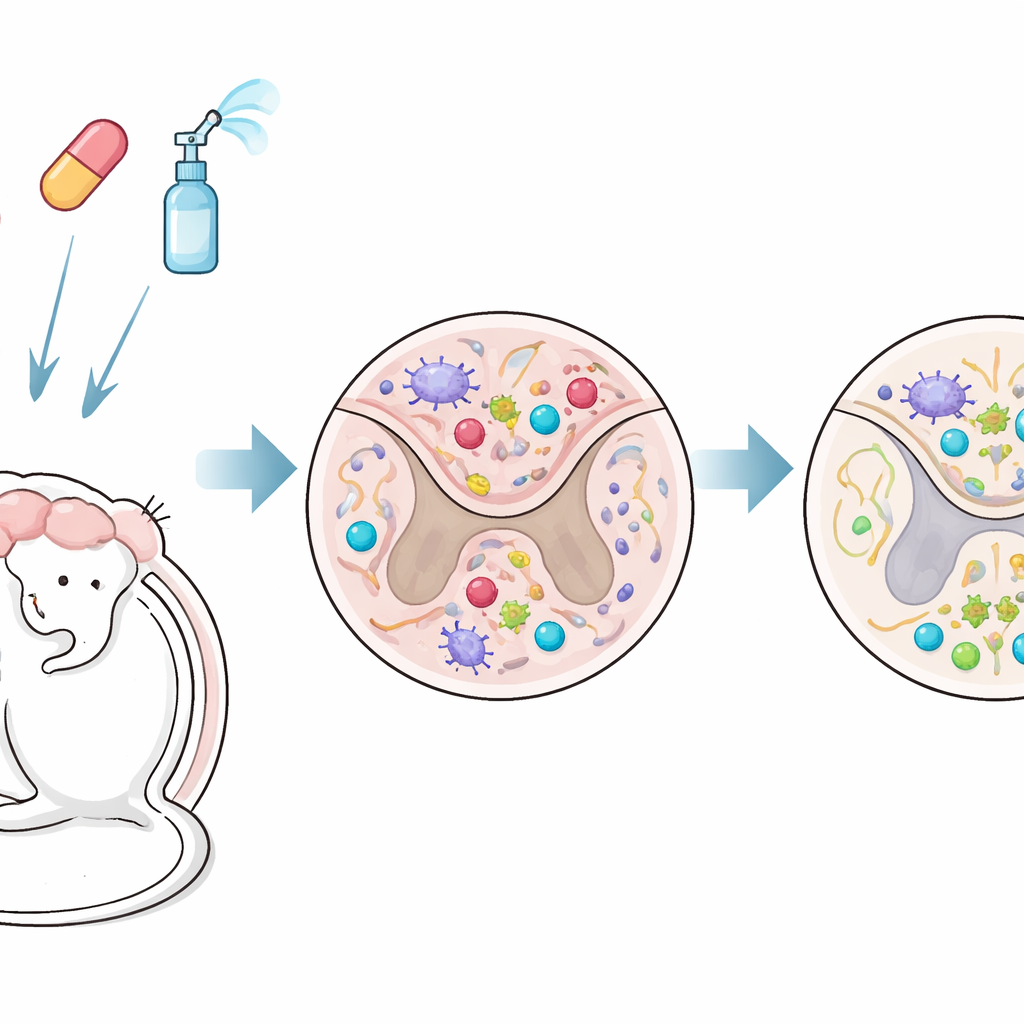
Połączenie dwóch leków, by dotrzeć i do krwi, i do mózgu
Naukowcy przetestowali terapię skojarzoną w modelu myszy, który ściśle naśladuje postępujące SR. Jeden z leków, fingolimod (FTY720), to pigułka, która uwięzia komórki odpornościowe w węzłach chłonnych i może także wnikać do mózgu. Drugi, interferon‑beta, to długo stosowana terapia SR, która zwykle działa poza mózgiem, ponieważ nie przechodzi łatwo przez barierę krew–mózg. W tym badaniu interferon‑beta podawano donosowo — przez nos — aby ominąć tę barierę i dotrzeć do ośrodkowego układu nerwowego w sposób bardziej bezpośredni. Leczenie rozpoczęto po tym, jak myszy rozwinęły już przewlekłe problemy neurologiczne, co odzwierciedla etap, gdy uszkodzenia zwykle trudniej odwrócić.
Mniej uszkodzeń i uspokojona aktywność odpornościowa
Myszy, które otrzymały terapię skojarzoną fingolimodem i donosowym interferonem‑beta, radziły sobie lepiej niż te leczone samym fingolimodem. Ich oceny choroby poprawiły się bardziej, a niektóre istniejące deficyty neurologiczne zmniejszyły się. Po zbadaniu rdzeni kręgowych stwierdzono więcej zachowanej mieliny, mniej oznak uszkodzenia aksonów oraz mniej napływających komórek odpornościowych. Zmniejszyła się liczba prozapalnych komórek T i monocytów, a pozostałe komórki T produkowały mniej szkodliwych mediatorów, takich jak interferon‑gamma i IL‑17. Co ważne, terapia skojarzona także stłumiła szkodliwe sygnały pochodzące od astrocytów i mikrogleju, komórek glejowych, które kształtują lokalne środowisko w mózgu i rdzeniu kręgowym.
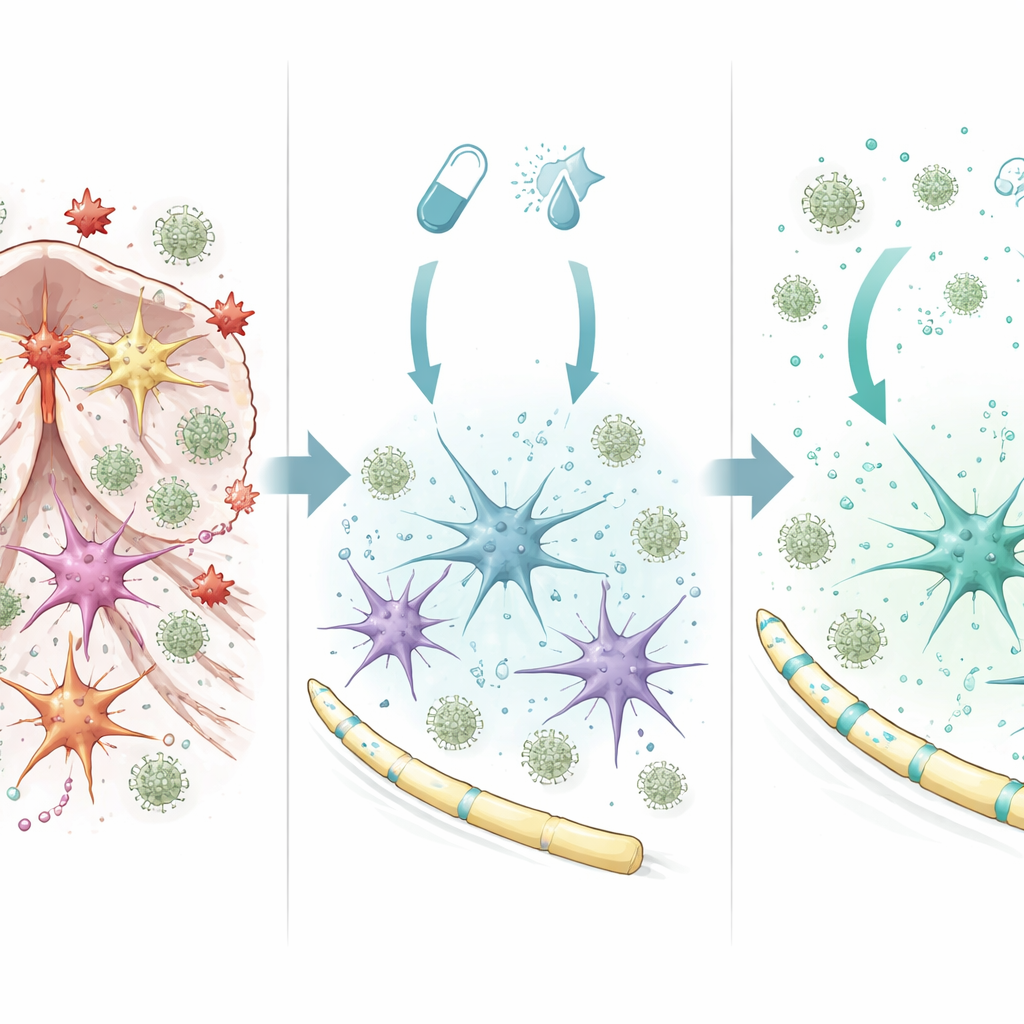
Astrocyty przechodzą z zachowań szkodliwych w ochronne
Aby zrozumieć, jak terapia skojarzona działa w mózgu, zespół badał oczyszczone astrocyty w hodowlach. Pod wpływem fingolimodu i interferonu‑beta astrocyty włączały szeroki zestaw genów związanych z przeżyciem komórek, zmniejszeniem stanu zapalnego i zdrowszą osłonką nerwową. Kluczową rolę odgrywał regulator zwany SOCS1, który działa jak hamulec sygnalizacji zapalnej. Zablokowanie SOCS1 w astrocytach usuwało dużą część ochronnego wzorca genowego i powodowało, że komórki te wydzielały więcej czynników zapalnych przyciągających komórki odpornościowe. W przeciwieństwie do tego, gdy SOCS1 był aktywny, astrocyty produkowały więcej sygnałów wzrostu i naprawy oraz wydzielały mieszaninę cząsteczek ograniczających migrację prozapalnych monocytów. Podobne ochronne przesunięcia zaobserwowano w liniach komórkowych ludzkich astrocytów i mikrogleju leczonych kombinacją leków, co sugeruje, że mechanizm ma znaczenie także poza modelem myszy.
Co to może oznaczać dla przyszłych terapii SR
Badanie to pokazuje, że połączenie fingolimodu z donosowym interferonem‑beta może robić więcej niż blokować komórki odpornościowe we krwi. Może również przeprogramować astrocyty w ośrodkowym układzie nerwowym w kierunku spokojniejszego, bardziej ochronnego stanu, z SOCS1 jako centralnym węzłem kontrolnym. Chociaż prace prowadzone były u myszy i w hodowlach komórkowych, a interferon‑beta sam w sobie nie był testowany równolegle w każdym eksperymencie, wyniki wskazują na obiecującą strategię: celować jednocześnie w obwodowy układ odpornościowy i własne komórki wspierające mózgu. Jeśli podobne efekty można osiągnąć i potwierdzić jako bezpieczne u ludzi, takie skojarzone, ukierunkowane na mózg podejścia mogą pomóc spowolnić lub częściowo odwrócić ciche uszkodzenia napędzające postępujące SR.
Cytowanie: Tsaktanis, T., Beyer, T., Nirschl, L. et al. Interferon-β and FTY720 ameliorate progressive CNS inflammation via SOCS1-associated astrocyte signaling. Sci Rep 16, 9851 (2026). https://doi.org/10.1038/s41598-026-45303-9
Słowa kluczowe: postępująca stwardnienie rozsiane, fingolimod, interferon beta, astrocyty, neurozapalanie