Clear Sky Science · pl
Dane krystalograficzne syntazy dolichylofosforanu mannopyranozy z Pyrococcus furiosus sugerują, że enzym może przełączać (flipować) swój produkt glikolipidowy
Jak termofilne mikroby utrzymują powłokę komórkową w formie
Wiele mikroorganizmów żyjących w wrzących środowiskach przetrwa dzięki ochronnej powłoce cukrowej na powierzchni komórki. Zbudowanie tej powłoki wymaga specjalnych cząsteczek tłuszcz–cukier, które muszą być wytwarzane po jednej stronie błony komórkowej, a następnie przeniesione na drugą. W tej pracy zanalizowano jeden z enzymów tworzących takie cząsteczki u mikroba kochającego wysokie temperatury i zasugerowano, że zaskakująco ten sam białkowy element może także pomagać w „flipowaniu” produktu przez błonę — wykonując dwie funkcje jednocześnie.
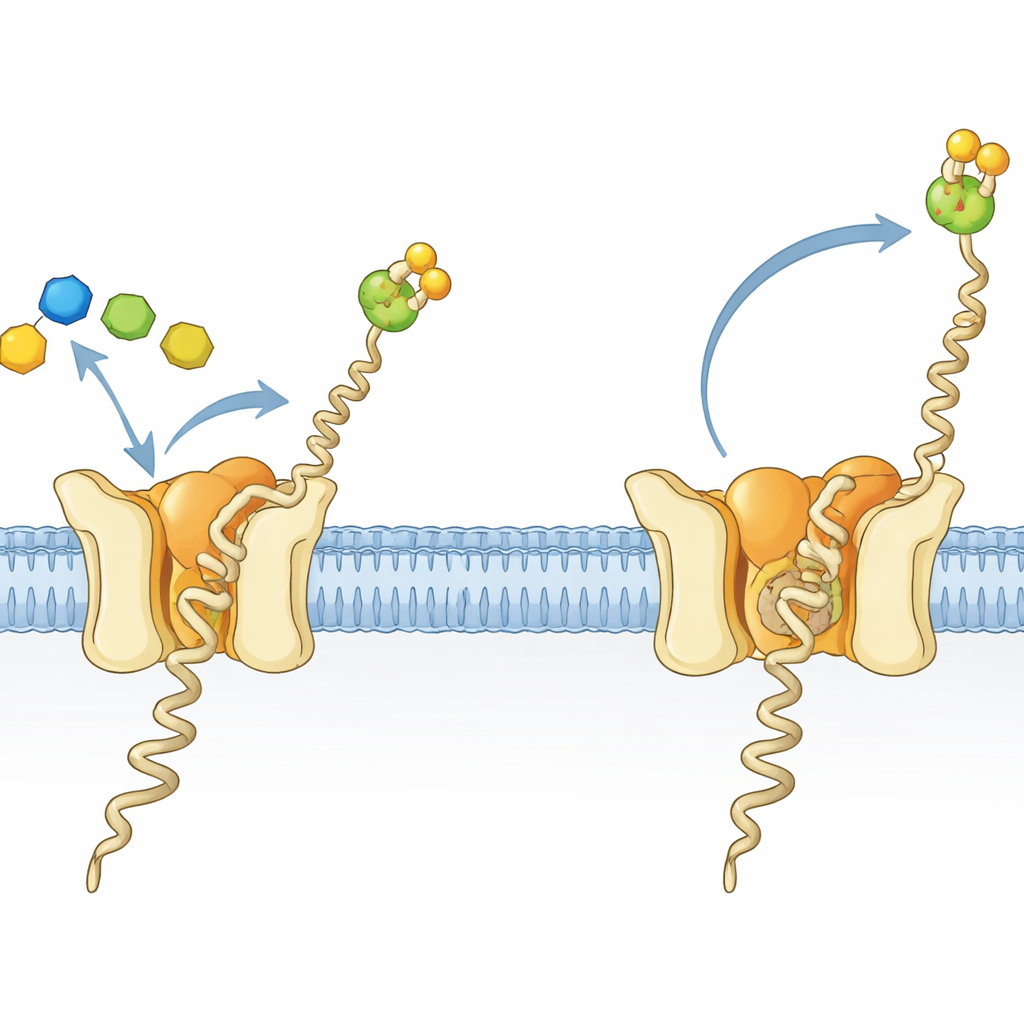
Maleńka fabryka kluczowej cząsteczki tłuszcz–cukier
Komórki we wszystkich domenach życia ozdabiają wiele białek łańcuchami cukrowymi — proces niezbędny dla prawidłowego fałdowania, stabilności i komunikacji międzykomórkowej. U archaeonów i eukariontów ważnym budulcem tych dekoracji jest cząsteczka tłuszcz–cukier zwana dolichylofosforanem mannozy (Dol-P-Man). Składa się z długiego tłustego ogona zakotwiczonego w błonie oraz grupy cukrowo‑fosforanowej wystającej do środowiska wodnego. Dol‑P‑Man powstaje dzięki enzymowi dolichylofosforan mannozy syntazie (DPMS), który przenosi resztę mannozy z rozpuszczalnego donora na lipid związany z błoną. W hipertermofilnym archaeonie Pyrococcus furiosus DPMS jest białkiem jednoniciowym, nazwanym typem III DPMS, z rozpuszczalną domeną katalityczną przyczepioną do czteroheliksowej części przechodzącej przez błonę, której rola była niejasna.
Uchwycenie enzymu w akcji
Naukowcy skrystalizowali DPMS z P. furiosus razem z jego substratami i śledzili reakcję metodą krystalografii rentgenowskiej. Ich nowa struktura, połączona z trzema wcześniejszymi, przedstawia serię migawkowych stanów wokół momentu przeniesienia cukru. W jednym stanie donor (GDP‑mannoza) i akceptor przypominający Dol‑P są związane w precyzyjnej geometrii, która ustawia reaktywny węgiel mannozy tuż przed grupą fosforanową Dol‑P — idealna konfiguracja „przed‑transferowa”. Pętle enzymu działają jak przednie i tylne drzwi: zamykają się, by ustabilizować donora i jon metalu, a potem przebudowują się, by otworzyć tor wejścia dla Dol‑P i wyjścia dla zużytego GDP po przekazaniu cukru. Te szczegóły wyjaśniają, jak enzym zapewnia wydajne i dokładne przenoszenie cukru na powierzchni błony.
Odwrócony produkt ukryty w błonie
Bardziej zaskakujący był drugi, odrębny stan zaobserwowany w tych samych kryształach. Tu gotowy Dol‑P‑Man nie znajduje się w centrum aktywnym, lecz osadzony głębiej w domenie przechodzącej przez błonę, w orientacji „do góry nogami”. Jego głowa cukrowo‑fosforanowa siedzi w polarnej kieszeni między dwiema parami helis (TMD1 i TMD2), podczas gdy tłusty ogon biegnie wzdłuż rowka uformowanego przez helisy. Kluczowy aminokwas, fenyloalanina, wydaje się działać jak bramka, która może albo zablokować, albo otworzyć dostęp do tej kieszeni. Jakość gęstości elektronowej i sposób upakowania białka w krysztale przemawiają za tym, że odwrócony Dol‑P‑Man nie jest artefaktem kontaktów krystalicznych, lecz prawdziwym, dobrze obsadzonym stanem, który enzym może przyjmować.
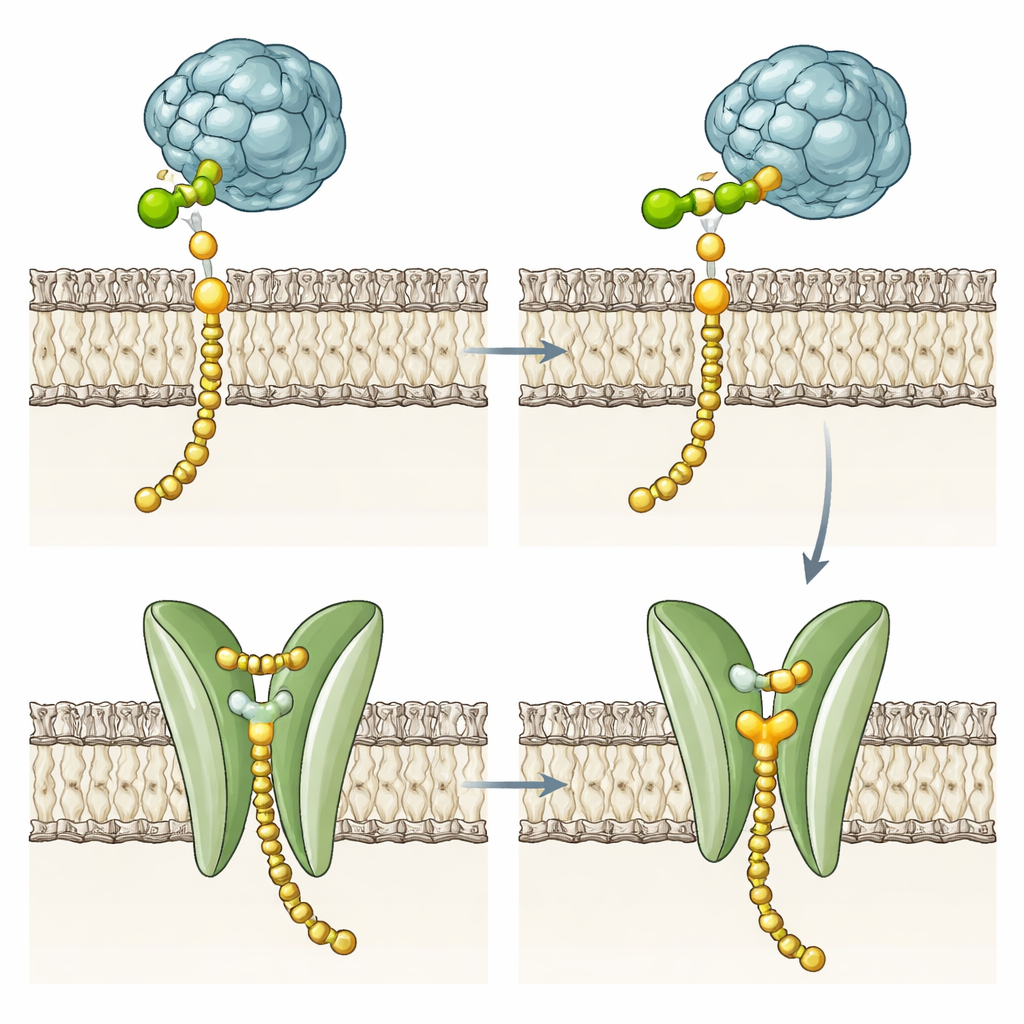
Mutanty enzymu sugerują drugie zadanie
Aby sprawdzić, czy domena przechodząca przez błonę jest niezbędna dla chemii przenoszenia cukru, zespół skonstruował wiele wariantów. Usunęli większość lub wszystkie helisy, zastąpili je innym segmentem błonowym z drożdżowego DPMS albo zmienili kluczowe reszty w kieszeni i fenyloalaninową bramkę. Co zaskakujące, mutanty te wciąż wytwarzały Dol‑P‑Man w tempie podobnym do enzymu nienaruszonego, chociaż niektóre były nieco mniej stabilne w błonie. Pokazuje to, że sedno reakcji mieści się w rozpuszczalnej domenie katalitycznej, a czteroheliksowy pęczek nie jest potrzebny do przyłączenia mannozy do Dol‑P. Zamiast tego zachowana polarna kieszeń, rowek i reszta pełnią rolę wyspecjalizowaną w obsłudze gotowego produktu, szczególnie u hipertermofilnych archaeonów, których sztywne błony sprawiają, że spontaniczne flipowanie lipidów jest energetycznie kosztowne.
Dlaczego enzym o podwójnej funkcji ma znaczenie
Uwzględniając dowody strukturalne i mutacyjne, autorzy proponują, że typ‑III DPMS jest białkiem „moonlightingowym” — pełni dwie funkcje. Najpierw syntetyzuje Dol‑P‑Man po wewnętrznej stronie błony plazmatycznej archaeonu; potem domena transbłonowa może pomóc w przełączeniu tej cząsteczki tłuszcz–cukier tak, by grupa główna pojawiła się na zewnątrz komórki, gotowa do wykorzystania przez inne enzymy budujące zewnętrzną powłokę cukrową. Ewolucja wydaje się faworyzować takie chimeryczne rozwiązanie głównie u ekstremalnie termofilnych archaeonów, gdzie lokalizowanie miejsca syntezy blisko wyspecjalizowanego rowka flipującego może zminimalizować straty i uszkodzenia termiczne. Choć praca ta nie dowodzi jeszcze bezpośrednio aktywności flipowania, dostarcza konkretnego modelu strukturalnego, w jaki sposób enzym może zarówno tworzyć, jak i przemieszczać istotny pośrednik lipidowy przez surową barierę błonową.
Cytowanie: Gandini, R., Keskitalo, M.M., Reichenbach, T. et al. Crystallographic data for Pyrococcus furiosus dolichylphosphate mannose synthase suggest that the enzyme could flip its glycolipid product. Sci Rep 16, 9076 (2026). https://doi.org/10.1038/s41598-026-44343-5
Słowa kluczowe: dolichylofosforan mannozy, flipaza lipidowa, archaea, glikozylacja białek, enzymy błonowe