Clear Sky Science · pl
Modelowanie patogenezy toksyn Clostridioides difficile i ochrony przez surowicę z przeciwciałami na immunokompetentnej platformie jelita na chipie
Dlaczego ten model zakażenia jelit ma znaczenie
Antybiotyki ratują życie, ale mogą też osłabić naturalną mikrobiotę jelitową, otwierając drogę dla groźnych infekcji. Jednym z najpoważniejszych sprawców jest Clostridioides difficile — bakteria wywołująca ciężkie biegunki i zagrażające życiu zapalenie okrężnicy, zwłaszcza u pacjentów hospitalizowanych. W tym badaniu opisano miniaturowe „jelito na chipie”, które odtwarza kluczowe cechy ludzkiego przewodu pokarmowego, w tym naczynia krwionośne i komórki układu odpornościowego, aby na żywo obserwować, jak toksyny C. difficile uszkadzają jelito i jak terapie oparte na przeciwciałach mogą powstrzymać te uszkodzenia.
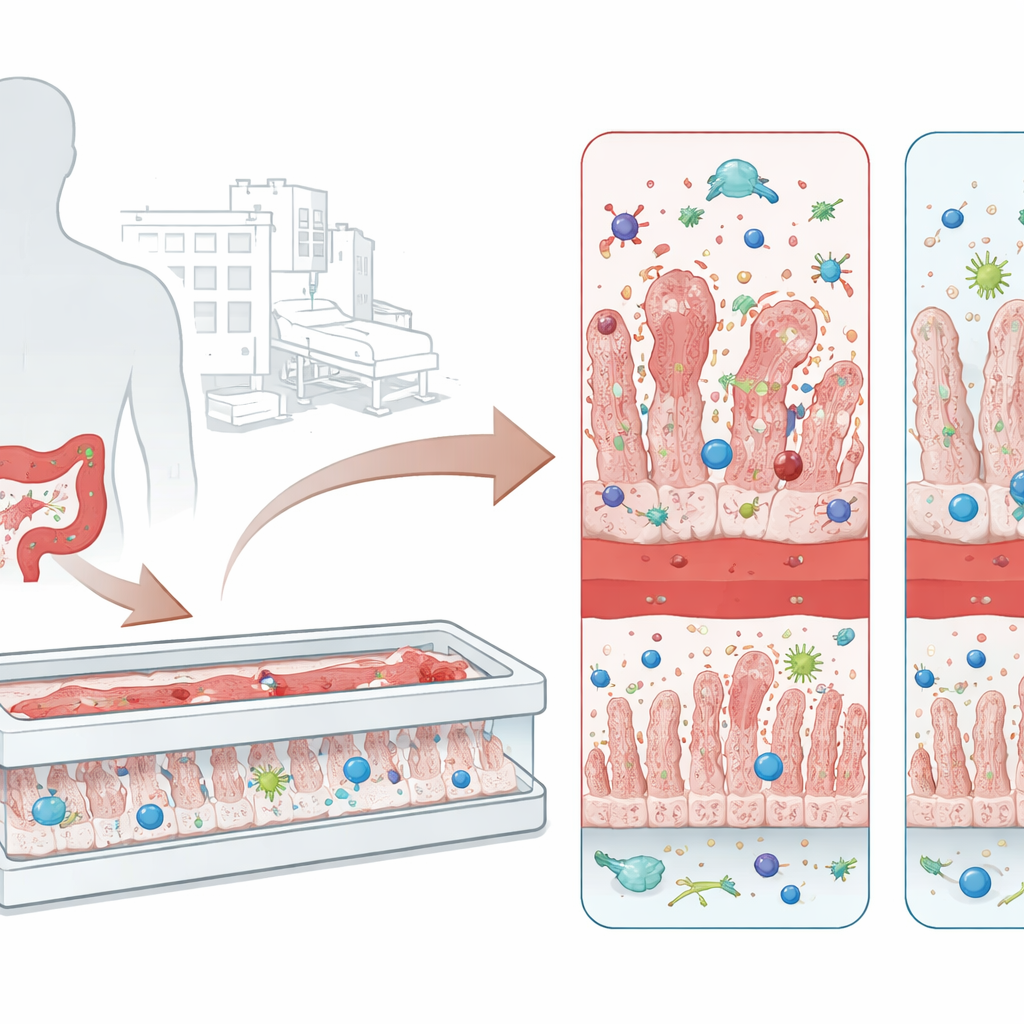
Od uporczywego szpitalnego zarazka do uszkodzenia jelit
C. difficile rozwija się u osób, których naturalna flora jelitowa została zaburzona, często po kuracji szerokospektralnymi antybiotykami. Mikroorganizm przetrwa w niekorzystnych warunkach jako odporne przetrwalniki, a po skolonizowaniu okrężnicy wydziela dwie główne toksyny znane jako TcdA i TcdB. Toksyny te atakują komórki jelitowe, rozluźniają zamknięcia między nimi i wywołują fale stanu zapalnego. Skutki mieszczą się w spektrum od dokuczliwej biegunki po rzekomobłoniaste zapalenie jelita, w którym ścianę jelita pokrywają warstwy martwej tkanki i komórek odpornościowych. Obecne terapie opierają się głównie na kolejnych antybiotykach i czasami przeszczepie mikrobioty jelitowej, jednak wielu pacjentów doświadcza nawrotów, co podkreśla potrzebę lepszych metod badania choroby i testowania terapii blokujących toksyny.
Budowa maleńkiego, żywego jelita na chipie
Tradycyjne modele laboratoryjne hodują płaską warstwę komórek jelitowych na podłożu. Choć użyteczne, te dwuwymiarowe kultury nie mają naczyń krwionośnych, komórek odpornościowych ani delikatnego przepływu płynów, które kształtują prawdziwe jelito. Naukowcy zastosowali zamiast tego mikroinżynieryjne urządzenie „jelito-na-chipie” z dwiema równoległymi kanalami oddzielonymi porowatą membraną. Jedna strona jest wyścielona komórkami jelitowymi, które formują palczaste wypustki przypominające kosmki i tworzą szczelne bariery. Przeciwległy kanał zawiera ludzkie komórki śródbłonka naczyniowego. Do tej miniaturowej tkanki dodano makrofagi pochodzące z monocytów, które osiadają w ścianie jelita, oraz krążące neutrofile, które mogą przemieszczać się przez kanał naczyniowy i infiltrują tkankę, tworząc immunokompetentne jelito-na-chipie (i‑IoC), które wierniej naśladuje żywe jelito.
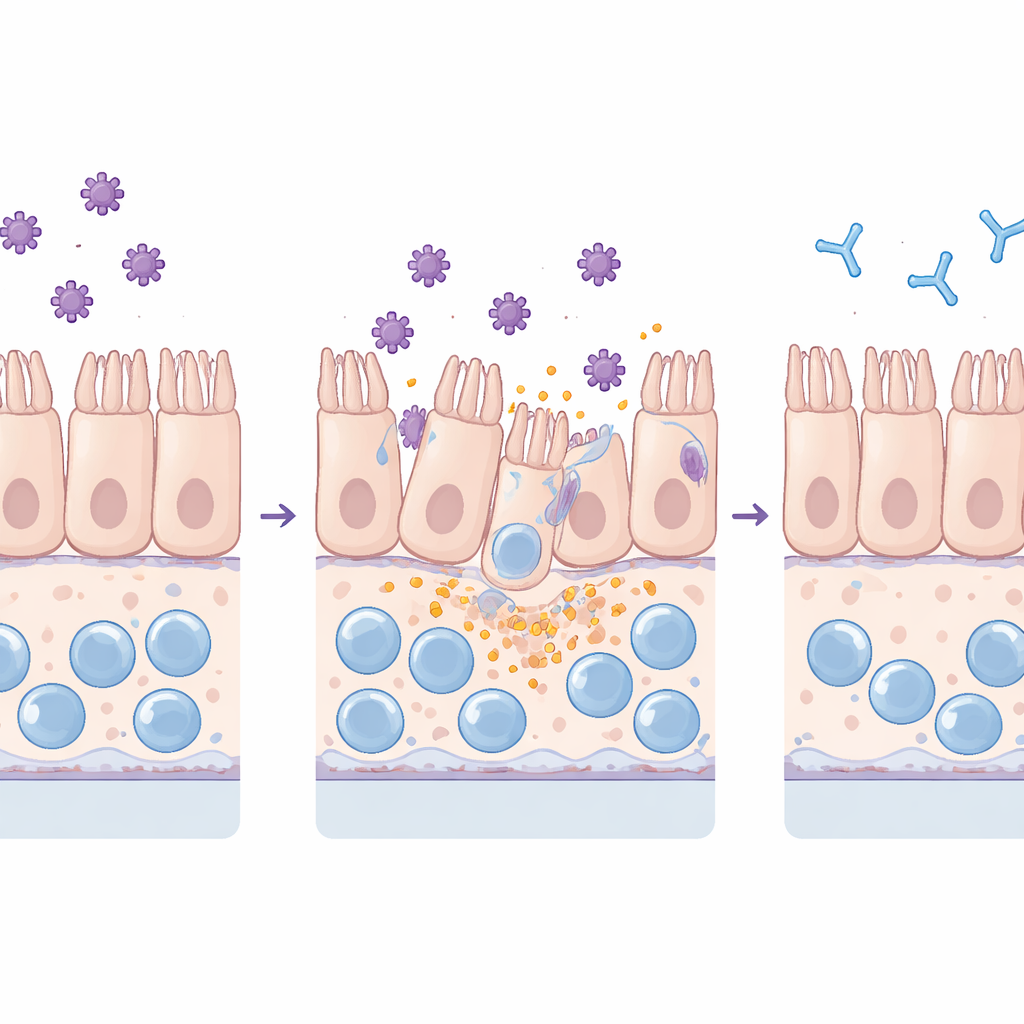
Obserwowanie, jak toksyny uszkadzają barierę
Zespół wystawił zarówno standardowe płaskie kultury, jak i bardziej złożony chip na oczyszczone toksyny TcdA i TcdB. Monitorowano, jak dobrze bariera jelitowa zatrzymuje fluorescencyjne barwniki, badano białka łączące, które trzymają sąsiednie komórki razem, oraz mierzyli molekuły zapalne i markery uszkodzenia komórek w płynach otaczających tkankę. Obie toksyny uszkadzały tkankę, lecz w odmienny sposób: TcdA głównie zaburzała połączenia szczelne i powodowała zaokrąglanie się komórek, podczas gdy TcdB prowadziła do masowego odpadania komórek z warstwy. Co istotne, chip wykrywał te efekty przy znacznie niższych stężeniach toksyn niż kultury płaskie, odzwierciedlając jego większą czułość i bardziej życiopodobne zachowanie przy ciągłym przepływie.
Komórki odpornościowe podsycają stan zapalny — i można je chronić
Dodanie makrofagów i neutrofili do chipa wzmocniło reakcję na toksyny. Makrofagi zwiększały uwalnianie kluczowych mediatorów zapalnych, takich jak IL‑6 i IL‑8, lecz same były eliminowane, co odpowiada zapalnemu typowi śmierci komórkowej. Neutrofile przylegały do ściany naczynia i migrowały do tkanki jelitowej, co odzwierciedla napływ komórek odpornościowych obserwowany u pacjentów. Dłuższa ekspozycja na toksyny uszkadzała nie tylko nabłonek jelitowy, lecz ostatecznie także warstwę naczyniową. Gdy jednak badacze wstępnie zmieszali toksyny z surowicami zawierającymi przeciwciała neutralizujące toksyny, strukturalne uszkodzenia, przecieki bariery, gwałtowne wzrosty cytokin, utrata makrofagów i napływ neutrofili były wyraźnie zmniejszone. W dłuższych eksperymentach tkanki uszkodzone przez TcdB mogły się częściowo zregenerować po usunięciu toksyn, podczas gdy TcdA pozostawiał trwalsze uszkodzenia, co sugeruje różne zdolności naprawcze po ekspozycji na każdą z toksyn.
Co to oznacza dla pacjentów i terapii
Dla czytelnika niebędącego specjalistą kluczowy wniosek jest taki, że ten maleńki, żywy model jelita realistycznie odtwarza, jak toksyny C. difficile uszkadzają przewód pokarmowy i pobudzają układ odpornościowy, a także pokazuje, jak skuteczne mogą być przeciwciała antytoksynowe w ochronie tkanki. W porównaniu z prostymi warstwami komórkowymi jelito‑na‑chipie jest bardziej czułe, zawiera naczynia krwionośne i komórki odpornościowe oraz może pracować przez kilka dni, aby uchwycić zarówno wczesne uszkodzenia, jak i próby regeneracji. To czyni go obiecującym polem testowym dla nowej generacji terapii i szczepionek neutralizujących toksyny bez dalszego zaburzania mikrobioty jelitowej, a potencjalnie także narzędziem do dopasowywania terapii na podstawie komórek pochodzących od konkretnych pacjentów w przyszłości.
Cytowanie: Wegner, V.D., Warschinke, M., Brahim, I.B. et al. Modeling Clostridioides difficile toxin pathogenesis and antiserum protection in an immunocompetent intestine-on-chip platform. Sci Rep 16, 9233 (2026). https://doi.org/10.1038/s41598-026-44170-8
Słowa kluczowe: Clostridioides difficile, jelito-na-chipie, zakażenie jelit, przeciwciała neutralizujące, modele organ-on-chip