Clear Sky Science · pl
Mikroskopia multiphotonowa bez barwników i uczenie maszynowe do rozpoznawania raka wątrobowokomórkowego
Dlaczego to ma znaczenie dla osób z rakiem wątroby
Rak wątroby, w szczególności rak wątrobowokomórkowy, jest zarówno powszechny, jak i śmiertelny, a operacja często stanowi jedyną szansę na wyleczenie. Podczas zabiegu chirurdzy muszą usunąć cały guz, oszczędzając jednocześnie jak najwięcej zdrowej wątroby, co jest trudnym kompromisem, zwłaszcza gdy zmieniona chorobowo wątroba już wygląda nieprawidłowo. Badanie to bada nowy sposób „widzenia” raka w czasie rzeczywistym podczas operacji, bez barwników czy czasochłonnych badań laboratoryjnych, łącząc zaawansowaną mikroskopię laserową ze sztuczną inteligencją. Celem jest pomoc chirurgom w szybszym i dokładniejszym odnajdywaniu prawdziwej granicy guza, co może poprawić wyniki leczenia pacjentów.
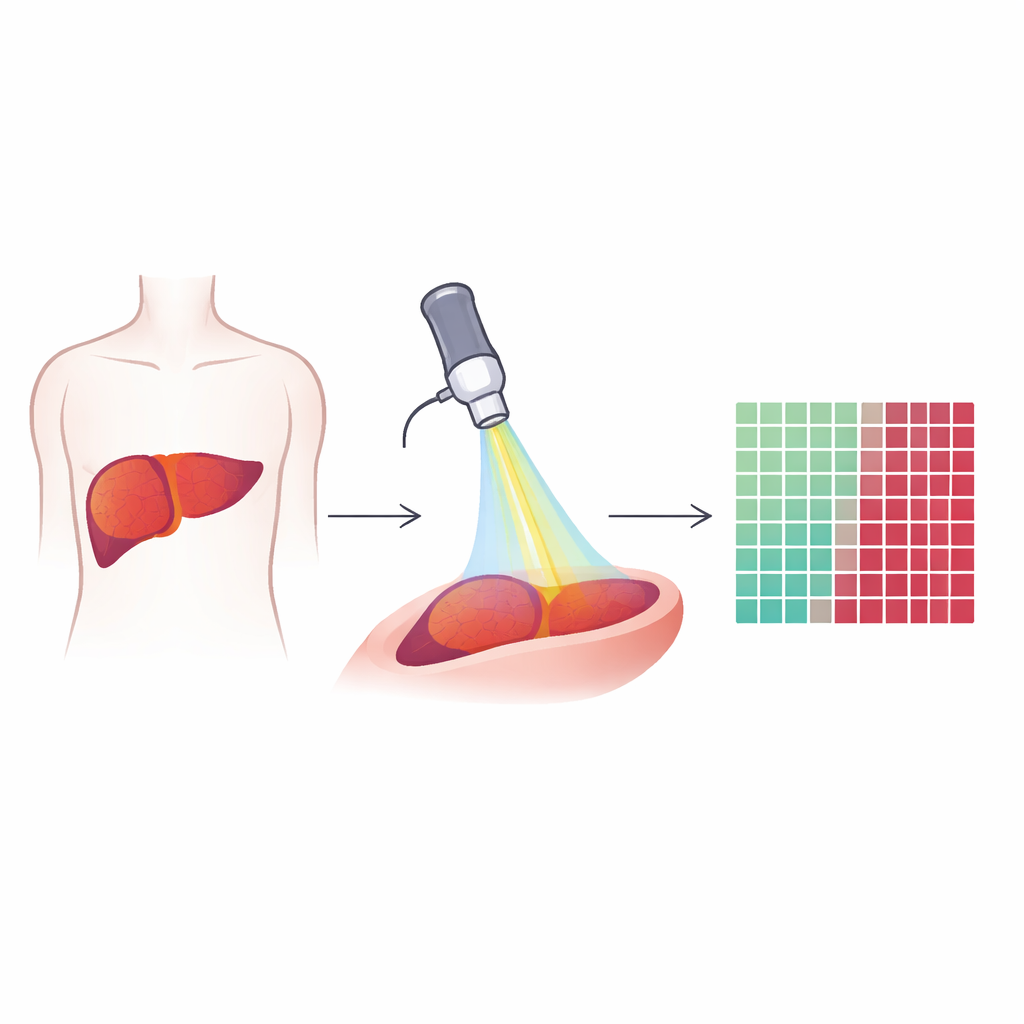
Zaglądanie w głąb tkanek za pomocą specjalnego światła
Naukowcy zastosowali technikę zwaną mikroskopią multiphotonową, która wykorzystuje bardzo krótkie impulsy lasera, by naturalne cząsteczki w tkance zaczęły emitować światło lub generować sygnały. Zamiast dodawać barwniki czy środki kontrastowe, metoda odczytuje to, co już tam jest: tłuszcze, włókna kolagenowe oraz naturalnie fluorescencyjne substancje w komórkach. Z każdego małego pola widzenia próbek wątroby zarejestrowano trzy rodzaje sygnałów: jeden uwidacznia lipidy, drugi pokazuje autofluorescencję od cząsteczek takich jak NADH i witamina A, a trzeci ujawnia sztywne włókna kolagenowe. Wspólnie te sygnały tworzą barwne, wysokorozdzielcze obrazy, które pokazują zarówno pojedyncze komórki, jak i ogólną architekturę tkanki wątrobowej i guzów.
Uchwycenie wielu oblicz raka wątroby
Zespół badał tkanki od 76 pacjentów po operacjach z powodu raka wątroby, analizując zarówno guz, jak i otaczającą wątrobę. Wykazali, że to obrazowanie bez barwników potrafi odwzorować klasyczne wzorce wzrostu raka wątrobowokomórkowego, takie jak cienkie lub grube blaszki komórek nowotworowych, zwarte płachty czy struktury gruczołopodobne. Pokazuje też zmiany w otaczającej wątrobie, w tym odkładanie się tłuszczu i bliznowacenie, które są powszechne u pacjentów z przewlekłą chorobą wątroby. Co ważne, wzorce te były widoczne nawet przy względnie niskiej rozdzielczości obrazów, podobnej do tej, jaką mogłyby dostarczać przyszłe endoskopowe urządzenia wewnątrz ciała. Sugeruje to, że podejście to może być praktyczne w sali operacyjnej, a nie tylko w laboratorium.
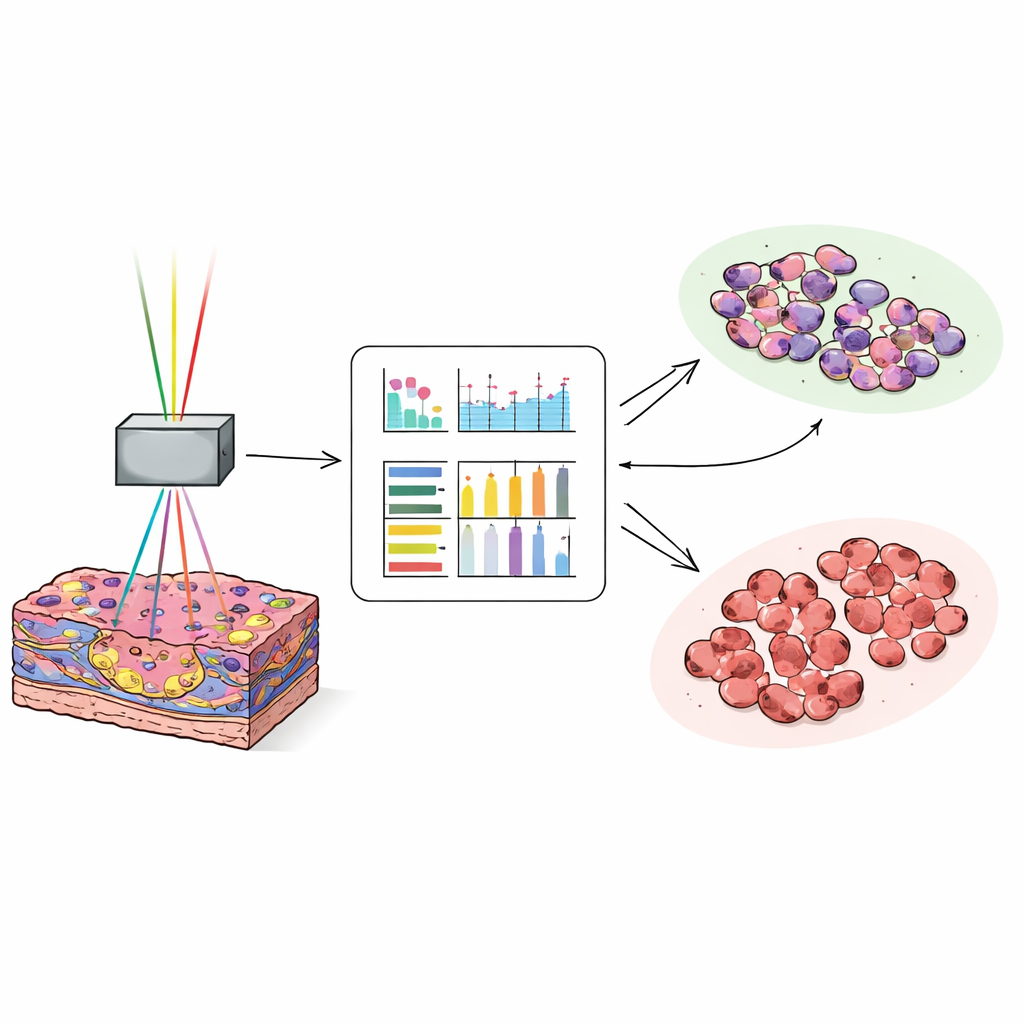
Nauczanie komputera rozpoznawania krawędzi guza
Aby przełożyć bogate, ale skomplikowane obrazy na szybkie decyzje, naukowcy przekształcili każdy obraz w liczby opisujące teksturę, takie jak gładkość, szorstkość czy zróżnicowanie wzorców pikseli. Dla każdego kanału obrazu obliczyli 17 takich miar, a następnie przeszkolili sieć neuronową na około 25 000 obrazów od 35 pacjentów, by odróżniać tkankę guzową od zdrowej wątroby. Model przetestowano następnie na około 27 000 nowych obrazów od kolejnych 38 pacjentów. Gdy komputer korzystał z połączenia sygnałów autofluorescencji i wrażliwego na kolagen kanału, poprawnie oznaczył obrazy jako guzowe lub normalne w około 97 na 100 przypadków. Nawet najbardziej subtelne, dobrze zróżnicowane guzy, które mogą być trudne do rozpoznania na szybkich mrożonych preparatach, sklasyfikowano z wysoką dokładnością.
Co wzory świetlne mówią o raku
Porównując różne kombinacje sygnałów, badanie wykazało, że autofluorescencja niesie najwięcej użytecznych informacji do odróżniania nowotworu od tkanek nie-nowotworowych. Ten blask pochodzi od wielu naturalnych cząsteczek w komórkach oraz struktur takich jak elastyna i kolagen, więc koduje gęstość komórek, rozmiar i kształt jąder (widoczne jako ciemniejsze obszary), krople tłuszczu oraz skład otaczającej tkanki. Dodanie sygnału specyficznego dla kolagenu dodatkowo wyostrzało kontrast między guzem a tkanką wątroby w tle, odzwierciedlając znane różnice w rozmieszczeniu włókien i naczyń. Ku zaskoczeniu, sygnał skupiony na lipidach wnosił mniejszy wkład do automatycznej klasyfikacji — praktyczna wskazówka, ponieważ może pozwolić na prostsze konstrukcje urządzeń opierających się na pojedynczej wiązce lasera zamiast bardziej złożonych układów dwuwiązkowych.
Od stołu laboratoryjnego do sali operacyjnej
Aby naśladować rzeczywiste zastosowanie chirurgiczne, zespół zastosował swój najlepszy model także do próbek tkanki obejmujących rzeczywistą granicę między guzem a wątrobą, tworząc mapy prawdopodobieństwa, które uwidaczniały miejsca, gdzie kończył się nowotwór, a zaczynała tkanka normalna. Mapy te generalnie dobrze zgadzały się z konwencjonalną histologią, choć silnie stłuszczone lub bogate w kolagen obszary czasami myliły klasyfikator. Autorzy wskazują na pozostające przeszkody przed zastosowaniem tej technologii w trakcie operacji na żywo, w tym ograniczoną głębokość obrazowania optycznego, potrzebę solidnych, sterylnych endoskopów, ruch i krew w polu operacyjnym oraz wyzwanie walidacji sztucznej inteligencji na dużych, rzeczywistych zbiorach danych. Mimo to praca pokazuje, że mikroskopia multiphotonowa bez barwników w połączeniu z uczeniem maszynowym może działać jak szybki, cyfrowy mikroskop, który pewnego dnia może pomóc chirurgom ciąć bardziej precyzyjnie i bezpieczniej, zwiększając szanse na całkowite usunięcie nowotworu przy zachowaniu jak największej ilości zdrowej wątroby.
Cytowanie: Galli, R., Korn, S., Aust, D. et al. Label-free multiphoton microscopy and machine learning for recognition of hepatocellular carcinoma. Sci Rep 16, 8734 (2026). https://doi.org/10.1038/s41598-026-43831-y
Słowa kluczowe: obrazowanie raka wątroby, mikroskopia multiphotonowa, autofluorescencja, marginesy chirurgiczne, uczenie maszynowe