Clear Sky Science · pl
Wyjaśnianie związku między powinowactwem a mocą działania terapeutycznego IgE
Wykorzystanie przeciwciał alergicznych przeciwko rakowi
Osoby cierpiące na alergie dobrze znają siłę przeciwciał IgE — cząsteczek odpowiedzialnych za łzawienie oczu i nagłe kichanie. W tym badaniu postawiono zaskakujące pytanie: czy tę samą silną biologię można przekierować do walki z rakiem, a jeśli tak, to jak precyzyjnie należy skalibrować te przeciwciała, by działały najlepiej? Badacze skupili się na raku piersi produkującym białko HER2, w tym przypadkach, gdzie HER2 występuje w bardzo niskich ilościach i leki dostępne obecnie często zawodzą.
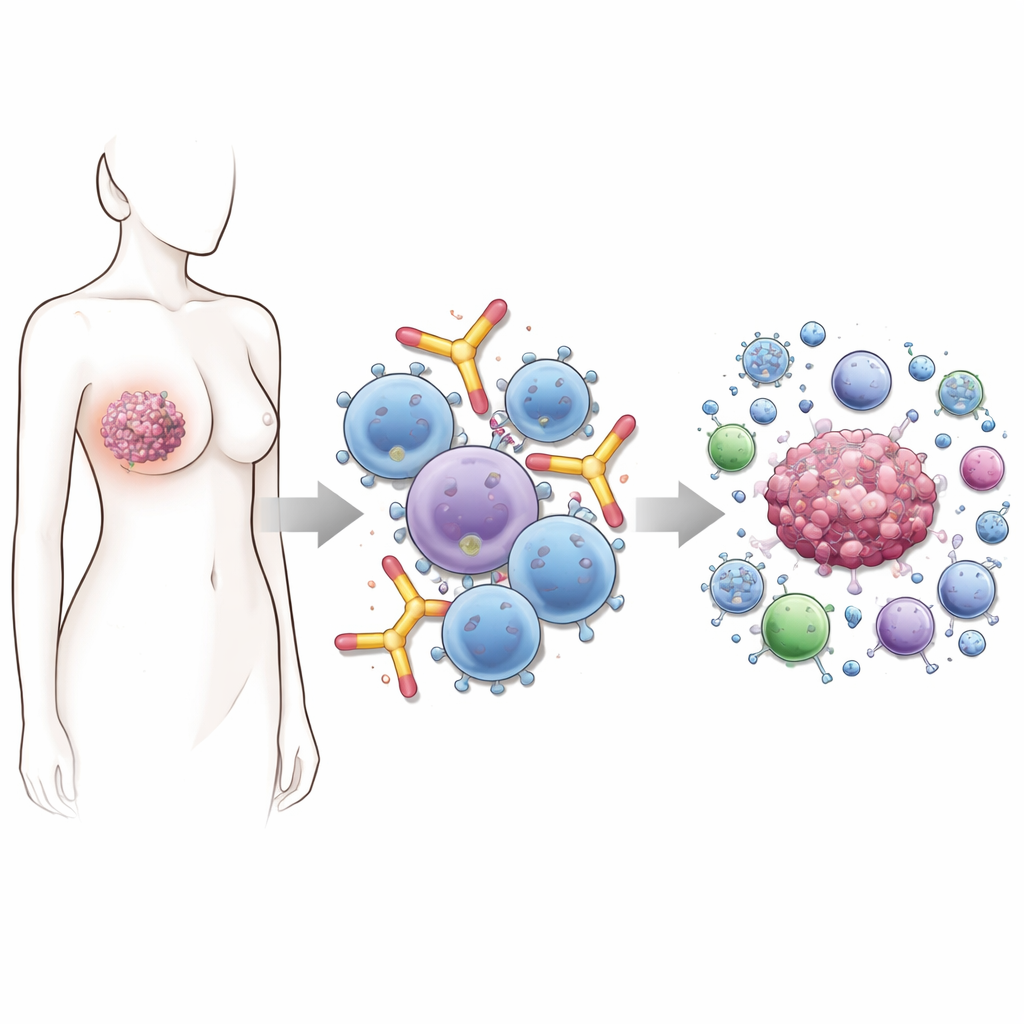
Dlaczego ta klasa przeciwciał jest wyjątkowa
Większość dostępnych dziś leków przeciwciałowych należy do klasy IgG. To główne narzędzia współczesnej terapii nowotworów, lecz mają one ograniczenia — zwłaszcza gdy guzy unikają ataku, zmniejszając ilość celu na swojej powierzchni. Przeciwciała IgE są inne. Naturalnie mocno wiążą się z komórkami odpornościowymi takimi jak komórki tuczne, bazofile, monocyty i makrofagi, przygotowując je do szybkiej reakcji. W alergii skutkuje to gwałtownymi reakcjami na pyłki czy pokarmy. W raku ta sama „okablowana” gotowość może oznaczać szybkie, ukierunkowane ataki na komórki nowotworowe, gdy tylko IgE napotka swój cel na powierzchni guza.
Projektowanie bardziej precyzyjnego IgE szukającego raka
Zespół wcześniej opracował przeciwciało IgE o nazwie EPS 226, które rozpoznaje HER2 na komórkach raka piersi i potrafi hamować wzrost guza w modelach eksperymentalnych. W tym nowym badaniu postanowili odpowiedzieć na subtelne, lecz kluczowe pytanie projektowe: czy zwiększenie siły wiązania przeciwciała z HER2 rzeczywiście poprawia jego zdolność do mobilizacji układu odpornościowego, czy też naturalne „wielorękie” wiązanie IgE (zwane awidnością) już wystarcza? Aby to zbadać, zastosowali skierowany mutageneza i selekcję w bakteriach, generując miliony drobnych wariantów regionu wiążącego HER2, a następnie wyłowili 12 nowych wariantów IgE, które wiązały HER2 silniej niż oryginalne przeciwciało.
Testy na komórkach i w modelach zwierzęcych
Udoskonalone przeciwciała poddano następnie serii testów na komórkach. Gdy załadowano je na komórki tuczne i wystawiono na działanie komórek nowotworowych pozytywnych na HER2, większość silniej wiążących IgE wywoływała silniejszą degranulację — reakcję aktywacyjną uwalniającą silne związki immunologiczne. Jeden wariant, nazwany EPS 232, wyróżniał się zdolnością do aktywacji komórek przy jednoczesnym efektywnym wiązaniu HER2 na komórkach ludzkich i szczurzych. Dalsze badania wykazały, że EPS 232 lepiej wyposażał komórki odpornościowe do zabijania raka: wzmacniał cytotoksyczność bazofili i sprzyjał efektywniejszemu fagocytowaniu komórek HER2-pozytywnych przez inżynieryjne komórki odpornościowe oraz przez pierwotne ludzkie makrofagi. Co ciekawe, zwiększanie siły wiązania pomagało tylko do pewnego stopnia; warianty o ekstremalnie wysokim powinowactwie nie przewyższały EPS 232, co sugeruje istnienie „słodkiego punktu”, w którym chwyt jest na tyle mocny, by być skutecznym, ale nie tak silny, by ograniczać liczbę przeciwciał i komórek odpornościowych mogących zaangażować się w każdy komórkowy cel.
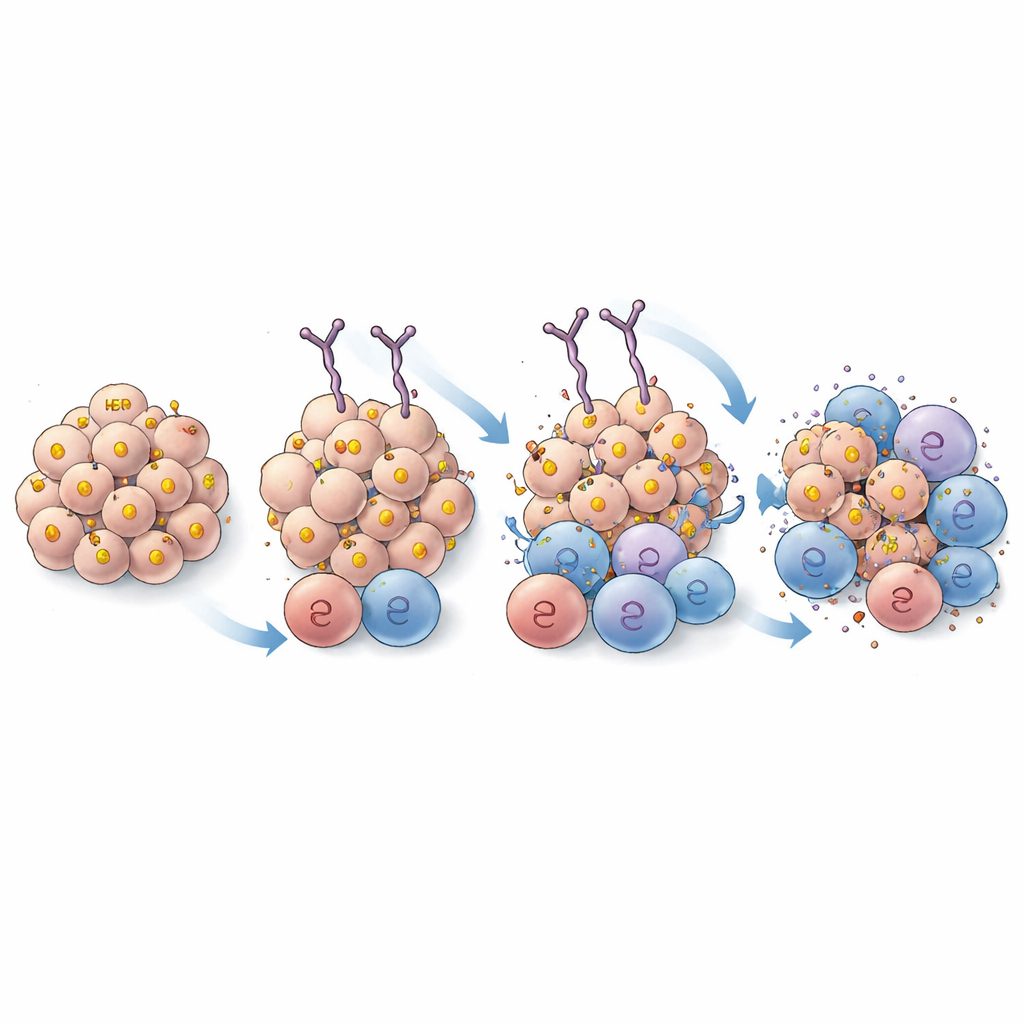
Zbliżenie na sposób wiązania przeciwciała
Aby upewnić się, że zyski wynikają ze silniejszego chwycenia, a nie z rozpoznania nowego fragmentu HER2, naukowcy zastosowali wysokorozdzielczą krio-elektronową mikroskopię, by zobrazować, jak EPS 232 i oryginalny EPS 226 osiadają na białku HER2. Struktury pokazały, że oba przeciwciała dokują do tego samego regionu HER2 i wykorzystują bardzo podobne punkty kontaktu, z jedynie subtelnymi różnicami, które nie powinny zmieniać ogólnego miejsca wiązania. To wspiera tezę, że poprawa wydajności EPS 232 wynika z lepszego powinowactwa, a nie zmiany celu.
Od laboratorium do kontroli guza
Prawdziwy egzamin przyniosły modele zwierzęce. U myszy noszących ludzkie guzy piersi i wyposażonych w ludzkie komórki odpornościowe, EPS 232 hamował wzrost guza skuteczniej i przy niższych dawkach niż EPS 226. U szczurów z agresywnym modelem raka piersi wytwarzającym ultra-niskie poziomy HER2 — podobnymi do niektórych raków potrójnie ujemnych — zaadaptowana szczurza wersja EPS 232 nie tylko bardziej spowolniła wzrost guza w porównaniu do poprzednika, ale również wydłużyła przeżycie. Guzy z leczonych zwierząt wykazywały zwiększoną infiltrację komórek T i makrofagów, co wskazuje, że ulepszone przeciwciało lepiej przekształcało mikrośrodowisko guza w bardziej sprzyjające atakowi immunologicznemu.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Dla czytelnika ogólnego najważniejszym przesłaniem jest to, że precyzyjne dostrojenie siły, z jaką przeciwciało IgE chwytapokierowany na raka cel, może realnie wpłynąć na jego skuteczność, nawet jeśli IgE już tworzy wiele jednoczesnych kontaktów z komórkami. Badanie wskazuje EPS 232 jako wiodącego kandydata na lek IgE przeciwko rakom piersi HER2-pozytywnym i HER2-niskim, w tym formom, które obecnie mają ograniczone opcje leczenia. Szerzej pokazuje też, że „alergicznego” typu przeciwciała można inżynieryjnie dostosować z właściwą równowagą siły wiązania, by zamienić system skłonny do kichania w narzędzie pomagające układowi odpornościowemu tropić i eliminować guzy.
Cytowanie: Marano, F., McKenzie, C., Birtley, J.R. et al. Elucidating the relationship between affinity and potency in the performance of therapeutic IgE. Sci Rep 16, 10555 (2026). https://doi.org/10.1038/s41598-026-43772-6
Słowa kluczowe: terapeutyczne IgE, rak piersi HER2, powinowactwo przeciwciała, immunoterapia nowotworów, rak piersi potrójnie ujemny