Clear Sky Science · pl
Stratyfikacja według dawki przepisu poprawia predykcję dawki opartą na głębokim uczeniu dla VMAT w miejscowo zaawansowanym NSCLC
Dlaczego inteligentniejsze plany radioterapii mają znaczenie
Gdy lekarze leczą zaawansowanego raka płuca za pomocą promieniowania, balansują na cienkiej granicy: dostarczyć wystarczającej energii, by kontrolować guz, jednocześnie chroniąc wrażliwe pobliskie narządy. Projektowanie takich planów jest powolne, złożone i w dużym stopniu zależy od umiejętności planisty. W badaniu tym sprawdzono, jak sztuczna inteligencja może przewidywać rozkład dawki w klatce piersiowej i – co istotne – pokazano, że uczenie SI na starannie pogrupowanych poziomach dawki poprawia trafność prognoz i ich użyteczność kliniczną.
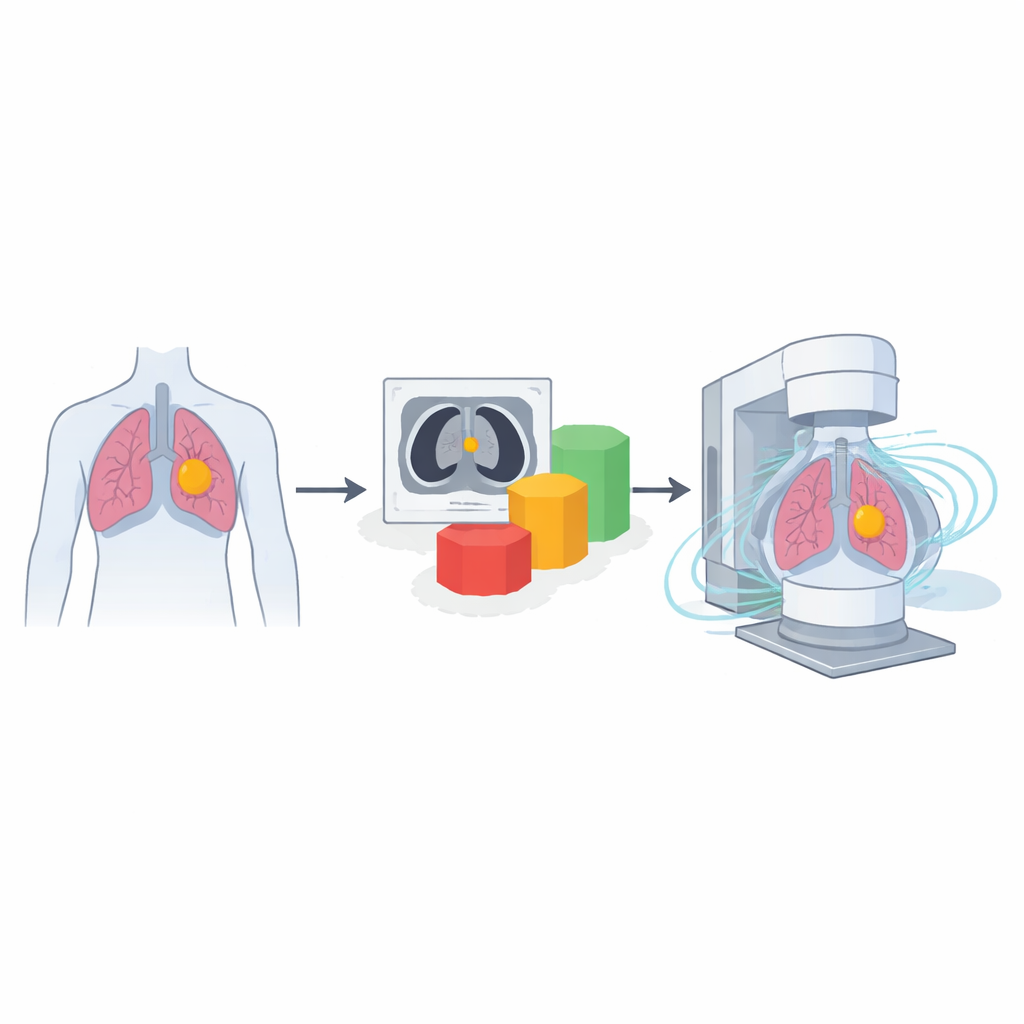
Jak leczony jest rak płuca za pomocą ukierunkowanych wiązek
Większość osób z miejscowo zaawansowanym niedrobnokomórkowym rakiem płuca nie kwalifikuje się do usunięcia guza chirurgicznie. Zamiast tego często stosuje się chemioterapię wraz z precyzyjnie ukształtowanymi wiązkami promieniowania, które obracają się wokół klatki piersiowej w łukach — technikę znaną jako VMAT. Celem jest dostarczenie wysokiej, jednorodnej dawki do guza przy jednoczesnym ograniczeniu ekspozycji płuc, serca, przełyku i rdzenia kręgowego. Osiągnięcie tej równowagi zwykle wymaga wielokrotnych korekt metodą prób i błędów, co pochłania czas i może opóźniać decyzje terapeutyczne. Gdyby lekarze mogli szybko oszacować, jaki rozkład dawki jest realistycznie osiągalny u danego pacjenta, mogliby wcześniej wybrać najlepszą strategię leczenia.
Nauczanie algorytmu rozpoznawania wzorców dawki
Naukowcy zwrócili się ku głębokiemu uczeniu, formie SI, która wyłapuje wzorce bezpośrednio z obrazów. Zebrali skany CT i gotowe plany leczenia od 72 pacjentów z rakiem płuca leczonych VMAT. Dla każdego pacjenta przeliczyli, jak ten sam układ wiązek dostarczyłby trzy różne dawki całkowite: 50, 54 i 60 grejów (Gy), standardowej jednostki promieniowania. Każdy przypadek został zamieniony na trójwymiarową siatkę oznaczającą guz, kluczowe narządy i bazowy obraz CT. Te dziewięć kanałów informacji zostało wprowadzone do 3D U-Netu, popularnej architektury sieci neuronowej, która może nauczyć się, jak dawka zwykle rozkłada się w ciele w zależności od anatomii.
Dlaczego grupowanie według dawki przepisu ma znaczenie
Kluczowe pytanie dotyczyło tego, jak poradzić sobie z faktem, że pacjentom przepisywane są różne dawki całkowite. Zespół zbudował cztery w przeciwnym razie identyczne modele SI. Trzy były „jedno‑przepisowe”, każdy trenowany wyłącznie na planach o jednej poziomej dawce (50, 54 lub 60 Gy). Czwarty model mieszał przypadki 50 i 60 Gy bez informowania sieci, jakiej dawki dotyczył dany przykład. W testach na nowych pacjentach modele specyficzne dla przepisu lepiej odtwarzały rzeczywistą dawkę w guzie, utrzymując zarówno pokrycie, jak i ogniska gorąca blisko planów klinicznych, zazwyczaj w granicach kilku Gy. W przeciwieństwie do tego model mieszany popełniał zauważalnie większe błędy w obszarach o najwyższej dawce w guzie oraz wokół rdzenia kręgowego, gdzie dawka musi pozostawać poniżej rygorystycznych limitów bezpieczeństwa.
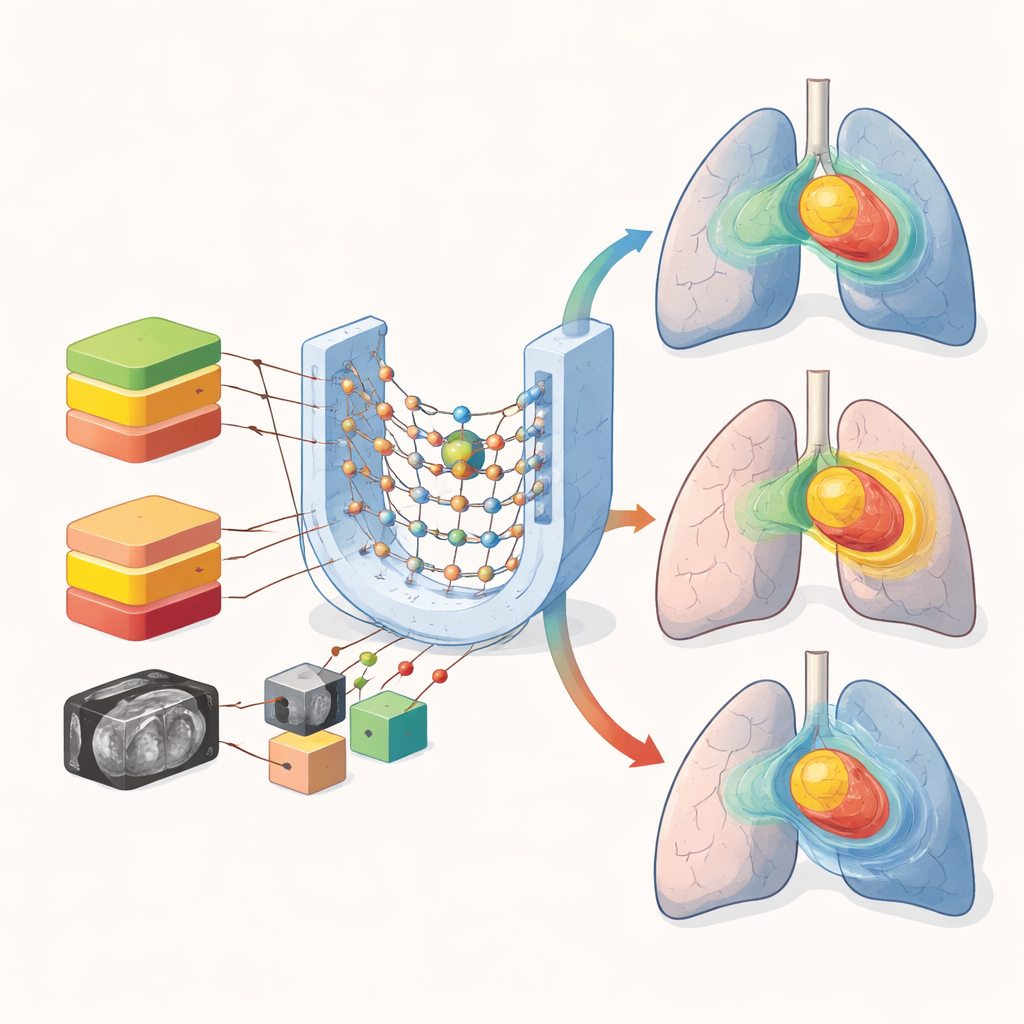
Ochrona ważnych narządów przy jednoczesnym przyspieszeniu planowania
Ciekawie, dla wielu narządów takich jak płuca, serce i przełyk modele mieszane i stratyfikowane działały podobnie. Średnie błędy dawki dla tych większych struktur pozostały umiarkowane we wszystkich podejściach. Główną słabością mieszania przepisów ujawniono w małych, wrażliwych strukturach jak rdzeń kręgowy, gdzie istotne jest ostre opadanie dawki. Kontrole wizualne przewidywanych map dawki pokazały, że wszystkie modele uchwyciły ogólny kształt obszaru wysokiej dawki w guzie, ale mieszanie przepisów prowadziło do większego rozmycia ostrych gradientów i obszarów niskiej dawki w płucach. Różnice te, choć subtelne w liczbach, mogą mieć znaczenie, gdy lekarze decydują, czy wyższa dawka przepisu jest bezpieczna.
Co to oznacza dla pacjentów i placówek
Dla pacjentów to opracowanie nie zastępuje dokładnych obliczeń dawki wykonywanych przez systemy kliniczne, ale może pomóc skupić czas i wysiłek na planach, które są rzeczywiście wykonalne i bezpieczne. Pokazując, że grupowanie danych treningowych według dawki przepisu istotnie wyostrza prognozy SI — szczególnie dla pokrycia guza i ochrony rdzenia kręgowego — badanie podkreśla praktyczny wybór projektowy, który może uczynić pomoc komputerową bardziej godną zaufania. Po dalszych testach na większych i bardziej zróżnicowanych grupach pacjentów takie modele mogłyby stać się codziennymi narzędziami dającymi lekarzom szybki, anatomiczny podgląd prawdopodobnych kompromisów dawki, wspierając lepsze i bardziej spójne planowanie leczenia.
Cytowanie: Chaipanya, T., Nimjaroen, K., Chamchod, S. et al. Prescription‑dose stratification improves deep learning‑based VMAT dose prediction in locally advanced NSCLC. Sci Rep 16, 8707 (2026). https://doi.org/10.1038/s41598-026-43192-6
Słowa kluczowe: radioterapia raka płuca, predykcja dawki z użyciem głębokiego uczenia, planowanie VMAT, optymalizacja planu leczenia, narządy krytyczne