Clear Sky Science · pl
PGE2 reguluje ferroptozę i osteogenezę komórek MC3T3-E1 poprzez NOS2
Dlaczego prostowanie zębów wpływa na kości
Narzędy ortodontyczne i przezroczyste nakładki robią więcej niż przesuwają zęby — prowokują kość wokół każdego zęba do przebudowy. Ta powolna, biologiczna praca konstrukcyjna jest jednym z powodów, dla których leczenie ortodontyczne może trwać lata. W tym badaniu przyjrzano się komórkom tworzącym kość, aby zrozumieć, jak powszechny sygnał zapalny, prostaglandyna E2, może jednocześnie przyspieszać przesuwanie zębów i subtelnie osłabiać nową kość, wskazując kierunki przyszłych sposobów na szybsze i trwalsze leczenie ortodontyczne.
Sygnały uwalniane, gdy zęby są przesuwane
Kiedy ortodonta wywiera siłę na ząb, więzadło i kość wokół korzenia doświadczają kontrolowanego urazu. Komórki w tym obszarze uwalniają przekaźniki chemiczne, w tym prostaglandynę E2, które koordynują, jak kość jest rozkładana po jednej stronie zęba i odbudowywana po drugiej. Autorzy skupili się na komórkach tworzących kość, zwanych osteoblastami, używając standardowej mysiej linii komórkowej jako modelu. Chcieli wiedzieć, jak prostaglandyna E2 wpływa na dwa kluczowe wyniki w tych komórkach: ich zdolność do budowy zmineralizowanej tkanki kostnej oraz skłonność do przechodzenia przez niedawno odkrytą, zależną od żelaza formę śmierci komórkowej zwaną ferroptozą.
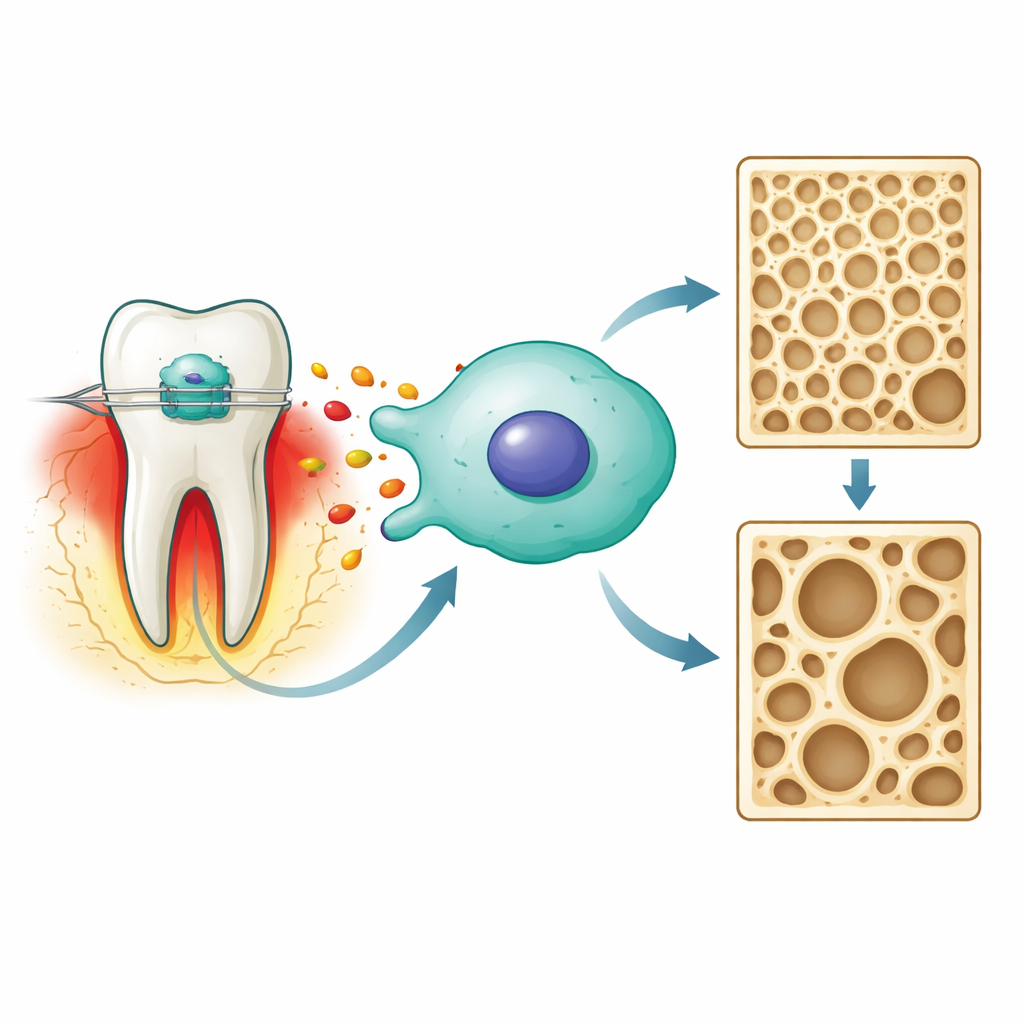
Szlak stresowy skupiony wokół jednego enzymu
Wykorzystując dane genowe od szczurów poddanych ruchowi zębów, zespół najpierw poszukiwał cząsteczek powiązanych zarówno z siłą ortodontyczną, jak i z ferroptozą. Jako kandydat wyróżnił się enzym zwany syntazą tlenku azotu 2 (NOS2), który okazał się kluczowym węzłem. W hodowli komórkowej ekspozycja komórek osteoblastopodobnych na klinicznie istotną dawkę prostaglandyny E2 wywołała stan „sterylnego” zapalenia — bez udziału zarazków, jedynie w wyniku stresu mechanicznego. Pod wpływem tego sygnału wzrosły poziomy NOS2, podobnie jak inne markery stresu i szkodliwe reaktywne cząsteczki tlenu, podczas gdy spadły białka ochronne antyoksydacyjne i zajmujące się gospodarką żelaza. Razem te zmiany są znamienne dla rozpoczynającej się w komórce ferroptozy.
Gdy budowniczowie kości wyłączają się
To samo leczenie prostaglandyną E2 osłabiło też zdolność komórek do pełnienia funkcji budowniczych kości. Klasyczne markery tworzenia kości spadły, a testy wizualizujące wczesną, kostnopodobną mineralizację i aktywność kluczowego enzymu — fosfatazy alkalicznej — wykazały słabsze wybarwienia i mniejsze odkładanie minerału. Gdy badacze dodali ferrostatynę-1, lek znany z blokowania ferroptozy, większość tych uszkodzeń została odwrócona: obniżył się stres oksydacyjny, sygnały ferroptozy ucichły, a aktywność osteogenna odbudowała się. Sugeruje to, że przynajmniej w tym modelu zapalny sygnał hamuje tworzenie kości częściowo przez popychanie komórek w kierunku ferroptozy.
Regulacja NOS2 jak przełącznika
Aby sprawdzić, czy NOS2 jest jedynie obserwatorem, czy aktywnym sprawcą, zespół genetycznie zmieniał jego poziomy w górę i w dół. Redukcja NOS2 w komórkach traktowanych prostaglandyną osłabiła markery ferroptozy, zmniejszyła uszkodzenia oksydacyjne i przywróciła zachowanie sprzyjające tworzeniu kości do poziomów zbliżonych do normy. Nadekspresja NOS2 działała odwrotnie: nasiliła stres i jeszcze bardziej stłumiła cechy budowania kości. Co szczególnie istotne, samo zwiększenie poziomu NOS2 — bez dodawania prostaglandyny E2 — wystarczyło, by wywołać zmiany podobne do ferroptozy i osłabić osteogenezę. To pokazuje, że NOS2 nie tylko reaguje na zapalenie; może samo w sobie popychać osteoblasty do rezygnacji z tworzenia mocnej, zmineralizowanej tkanki kostnej.
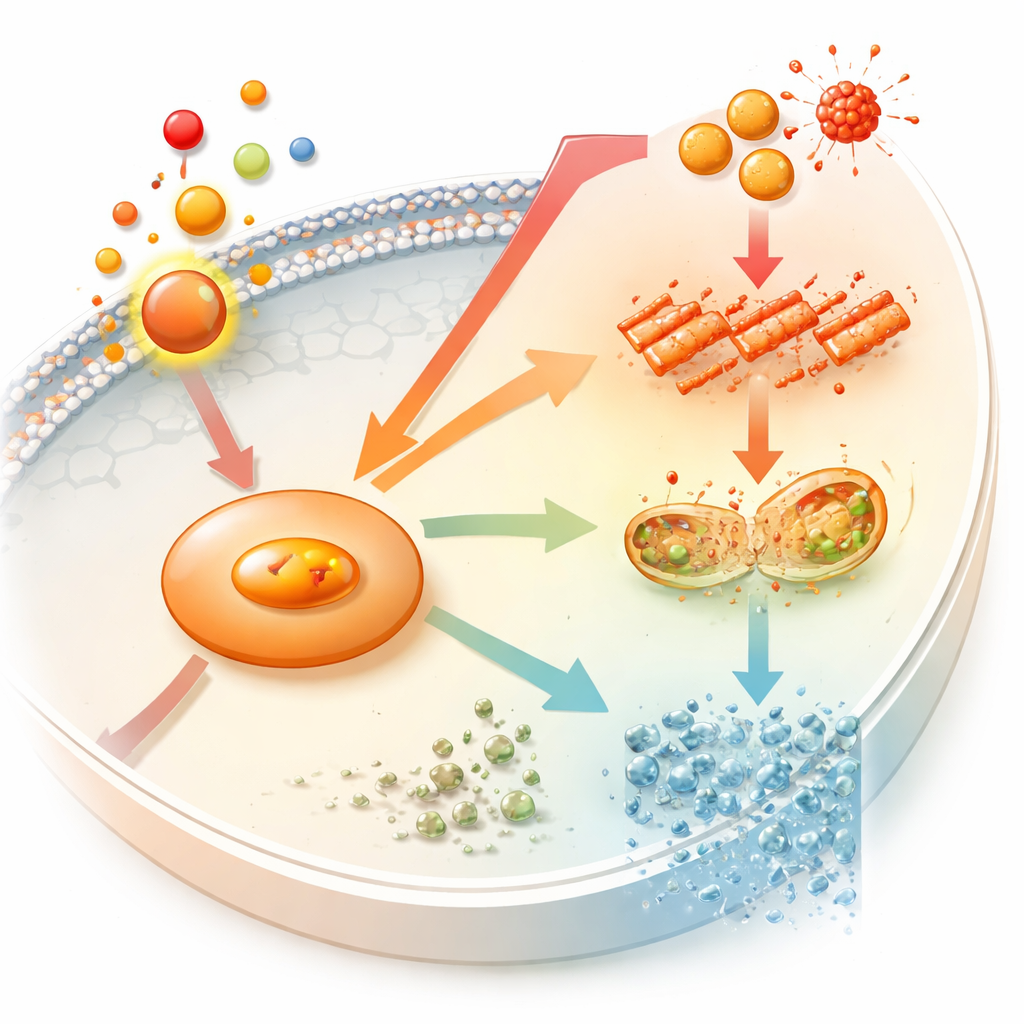
Co to oznacza dla przyszłych aparatów ortodontycznych
Wspólnie te eksperymenty przedstawiają nową oś w biologii kości podczas ruchu zębów: prostaglandyna E2 zwiększa NOS2, NOS2 napędza uszkodzenia oksydacyjne i ferroptozę, a zdolność do tworzenia kości maleje. Dla pacjentów nie oznacza to, że aparaty są niebezpieczne, ale wyjaśnia, dlaczego leczenie może wymagać delikatnej równowagi między szybkim przesuwaniem zębów a zachowaniem silnej kości otaczającej. W dłuższej perspektywie leki lub materiały, które wyważają aktywność NOS2 lub chronią osteoblasty przed ferroptozą, mogłyby pomóc ortodontom skrócić czas leczenia przy jednoczesnym utrzymaniu, a nawet poprawie jakości i stabilności kości podporowej.
Cytowanie: Sun, M., Yang, Y., Pang, L. et al. PGE2 regulates ferroptosis and osteogenesis of MC3T3-E1 cells via NOS2. Sci Rep 16, 8893 (2026). https://doi.org/10.1038/s41598-026-43001-0
Słowa kluczowe: ruch zębów w ortodoncji, remodelowanie kości, ferroptoza, syntaza tlenku azotu, funkcja osteoblastów