Clear Sky Science · pl
Badanie podwójnej roli pęcherzyków zewnątrzkomórkowych w krzepnięciu i modulacji układu odpornościowego w glejakach
Dlaczego zakrzepy mają znaczenie w nowotworach mózgu
Osoby z rozpoznanym glejakiem wielopostaciowym, najbardziej agresywną postacią nowotworu mózgu, często stają przed nieoczekiwanym zagrożeniem: groźnymi zakrzepami krwi w nogach lub mózgu. Zakrzepy te mogą skracać czas przeżycia i komplikować już wymagające leczenie. W badaniu postawiono proste, lecz kluczowe pytanie: co w komórkach glejaka sprawia, że otaczająca je krew tak chętnie tworzy skrzepliny, i jak drobne cząstki uwalniane przez guz do krwi wpływają na obronę immunologiczną organizmu?
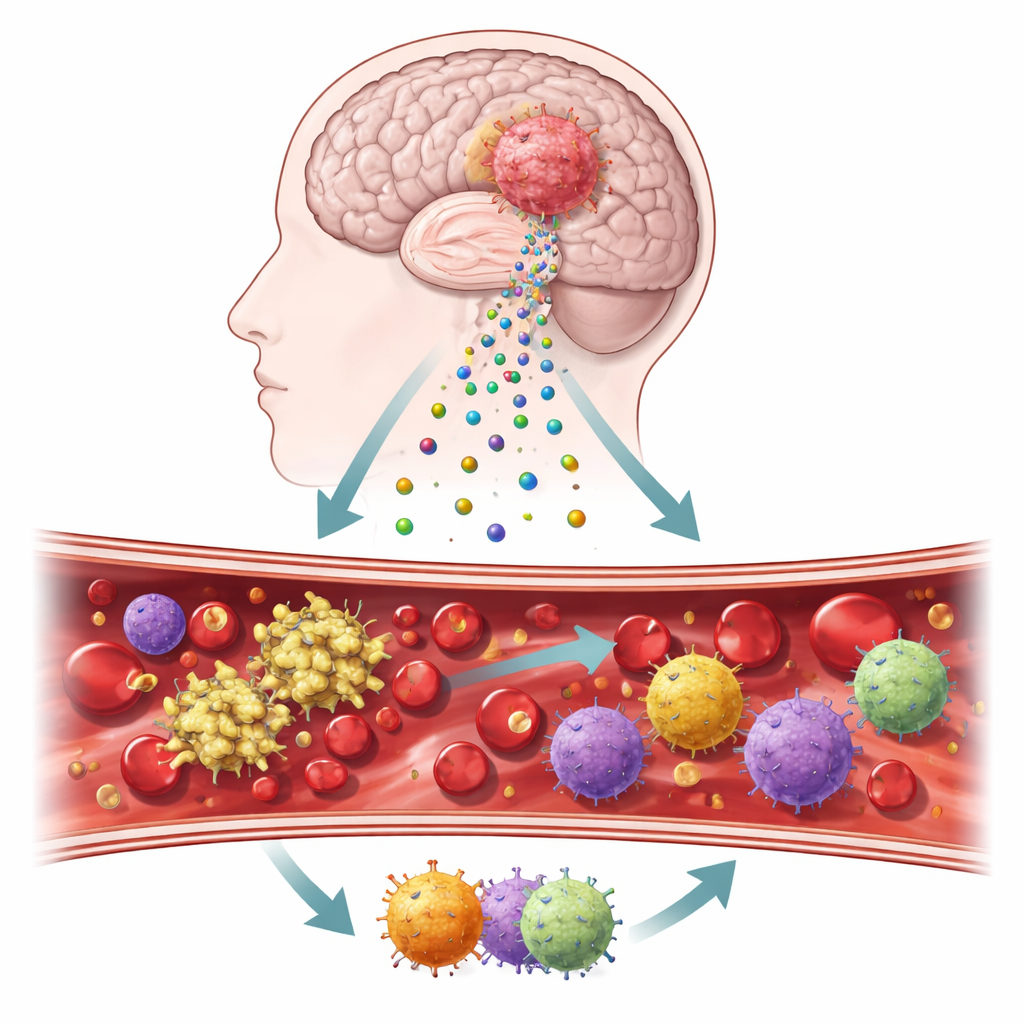
Maleńcy posłańcy opuszczający guz mózgu
Naukowcy skoncentrowali się na mikroskopijnych pęcherzykach zwanych pęcherzykami zewnątrzkomórkowymi, które odrywają się od komórek nowotworowych i przemieszczają się w krwi oraz tkance mózgowej. Na ich powierzchni znajdują się dwa kluczowe białka — czynnik tkankowy i podoplanina — które wiadomo, że wywołują krzepnięcie i wpływają na stan zapalny. Wykorzystując próbki guza, krew pobraną podczas operacji oraz hodowle komórek pochodzące z guzów pacjentów, zespół opracował etapowy schemat śledzenia zachowania tych molekuł u prawdziwych pacjentów oraz w kontrolowanych testach laboratoryjnych. Porównali także tkankę guza ze zdrowym mózgiem, aby ocenić natężenie sygnałów związanych z krzepnięciem.
Spokojne parametry krwi, ale pobudzone otoczenie guza
Standardowe badania szpitalne sugerowały, że przed zabiegiem krew wielu pacjentów wygląda zaskakująco normalnie: typowe czasy krzepnięcia i parametry trwałości skrzepu mieściły się w granicach referencyjnych. Jednak badanie samych guzów ujawniło inny obraz. Tkanka glejaka wykazywała konsekwentnie wysokie poziomy czynnika tkankowego i podoplaniny oraz bardzo niskie stężenia naturalnego hamulca, jakim jest inhibitor szlaku czynnika tkankowego. Linie komórkowe pochodzące od pacjentów zachowały w hodowli ten wzorzec, potwierdzając, że „prozakrzepowa” sygnatura jest cechą wewnętrzną komórek nowotworowych. Gdy te komórki lub pęcherzyki, które uwalniały, mieszano z osoczem w laboratorium, skrzepliny tworzyły się szybciej, zwłaszcza przez tzw. drogę zewnętrzną zależną od czynnika tkankowego.
Różne komórki guza — różne strategie krzepnięcia
Nie wszystkie glejaki zachowywały się identycznie. Niektóre linie komórkowe pochodzące od pacjentów miały bardzo wysoki poziom czynnika tkankowego, inne więcej podoplaniny, a niektóre miały niewiele obu białek. Komórki bogate w czynnik tkankowy były najskuteczniejsze w skracaniu czasu krzepnięcia, podczas gdy komórki z przewagą podoplaniny wpływały umiarkowanie, oddziałując na płytki krwi. Kiedy jedną z takich linii podzielono na podgrupy wyrażające tylko czynnik tkankowy, tylko podoplaninę, oba białka albo żadne, komórki długo nie zachowywały tej odrębności. W ciągu trzech tygodni wracały do mieszanych profili, ujawniając wysoki stopień plastyczności. Towarzyszyły temu zmiany w stresie oksydacyjnym w komórkach, co sugeruje, że chemiczne napięcie w guzie może przesuwać komórki w kierunku bardziej prozakrzepowych stanów.
Pęcherzyki kształtujące odporność mózgu i krwi
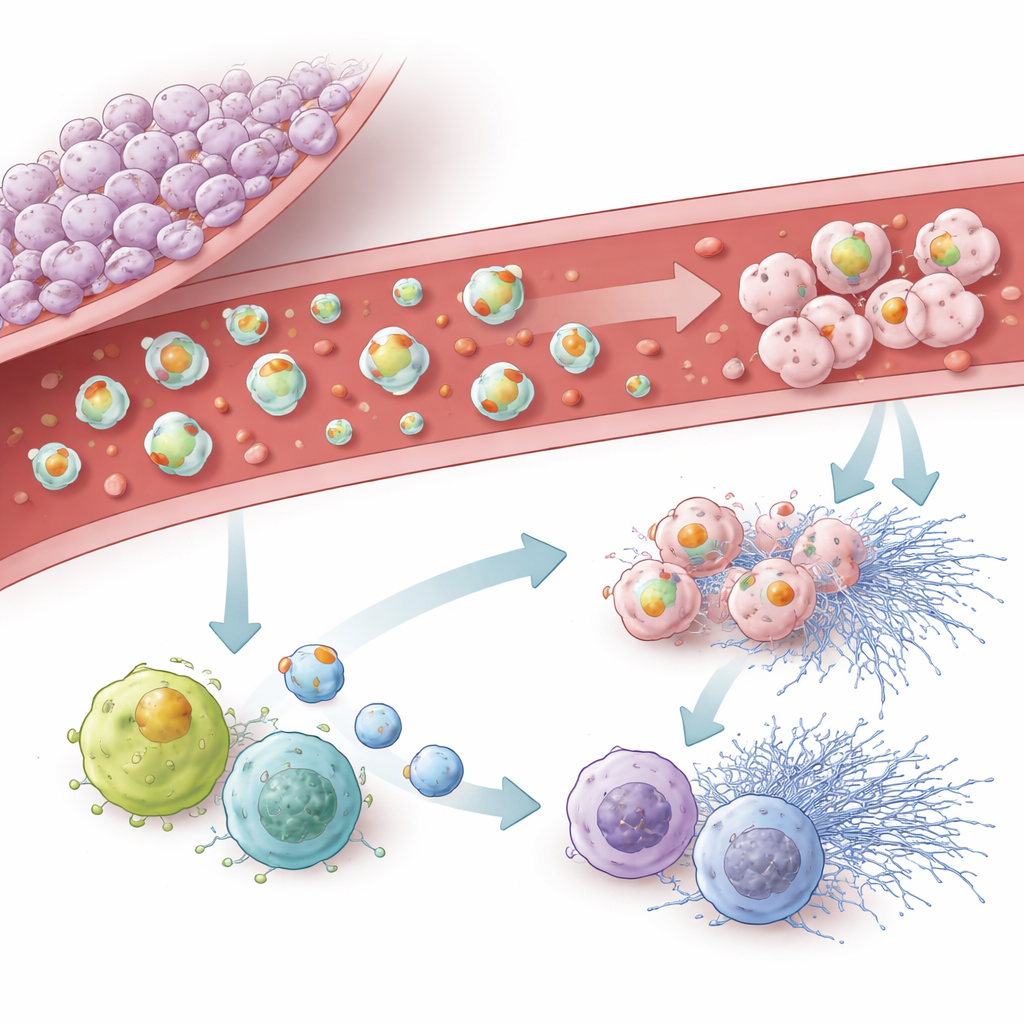
Zespół przyjrzał się następnie, w jaki sposób pęcherzyki pochodzące z guza oddziałują na własne komórki odpornościowe mózgu — mikrogleję — oraz na krążące białe krwinki i neutrofile. Pęcherzyki z linii o silnym potencjale prozakrzepowym były chętnie wchłaniane przez mikrogleję i spowalniały ich migrację, jednocześnie kierując je ku bardziej zapalnemu, „M1‑podobnemu” stanowi oraz wywołując oznaki starzenia komórkowego. W krwiobiegu pęcherzyki bogate w czynnik tkankowy aktywowały leukocyty, zwiększały produkcję reaktywnych form tlenu i sprzyjały uwolnieniu lepkich, przypominających sieć struktur z neutrofili, zwanych zewnątrzkomórkowymi pułapkami. Pęcherzyki niosące podoplaninę były słabsze w wywoływaniu tych gwałtownych reakcji immunologicznych, ale silnie stymulowały program podobny do starzenia komórkowego, w którym komórki odpornościowe przestają się dzielić i zmieniają swoją funkcję. Nawet pęcherzyki pozbawione obu kluczowych białek mogły wywołać pewien stopień senescencji, co sugeruje, że inne składniki ładunku również mają znaczenie.
Co to oznacza dla pacjentów i przyszłej opieki
W sumie wyniki pokazują, że glejak nie powoduje ogólnego uwęglenia krwi wszędzie w organizmie. Zamiast tego guz i uwalniane przez niego pęcherzyki tworzą zlokalizowaną, wysoce złożoną strefę, w której krzepnięcie i zapalenie wzajemnie się napędzają. Czynnik tkankowy wyłania się jako główny motor tworzenia skrzepów i aktywacji zapalnej, podczas gdy podoplanina dorzuca własny wpływ na płytki krwi, starzenie immunologiczne i zachowanie mikroglei. Ponieważ te pęcherzyki krążą we krwi i odzwierciedlają stan guza, mogą w przyszłości posłużyć jako markery krwiowe do identyfikacji pacjentów szczególnie narażonych na zakrzepy. Mogą także wskazywać kierunki bardziej precyzyjnej prewencji, ukierunkowanej na prozakrzepowe mechanizmy guza, bez konieczności szerokiego rozrzedzania krwi.
Cytowanie: Wolff, A., Waitz, G., Kaps, P. et al. Exploring the dual role of extracellular vesicles in coagulation and immune modulation in glioblastoma. Sci Rep 16, 9534 (2026). https://doi.org/10.1038/s41598-026-42867-4
Słowa kluczowe: glejak, zakrzepy krwi, pęcherzyki zewnątrzkomórkowe, mikrośrodowisko guza, odpowiedź immunologiczna