Clear Sky Science · pl
Ocena rusztowania dodecyny Mycobacterium tuberculosis jako platformy multimeryzacji wpływającej na immunogenność antygenów L2 HPV
Dlaczego te badania mają znaczenie dla przyszłych szczepionek
Ludzkie brodawczaki (HPV) powodują niemal wszystkie przypadki raka szyjki macicy oraz rosnący odsetek innych nowotworów, a istniejące szczepionki są skomplikowane w produkcji i nie obejmują w pełni wszystkich niebezpiecznych typów wirusa. W tym badaniu zbadano nowe podejście do budowy prostszej, szerzej chroniącej szczepionki przeciw HPV, która mogłaby być tańsza, bardziej stabilna i łatwiejsza w użyciu na całym świecie, szczególnie w krajach o niskich i średnich dochodach. Poprzez przeorganizowanie sposobu prezentacji kluczowych fragmentów białek wirusa układowi odpornościowemu, badacze dążą do nakłonienia organizmu do wytworzenia silnych przeciwciał przeciw wielu typom HPV jednocześnie.
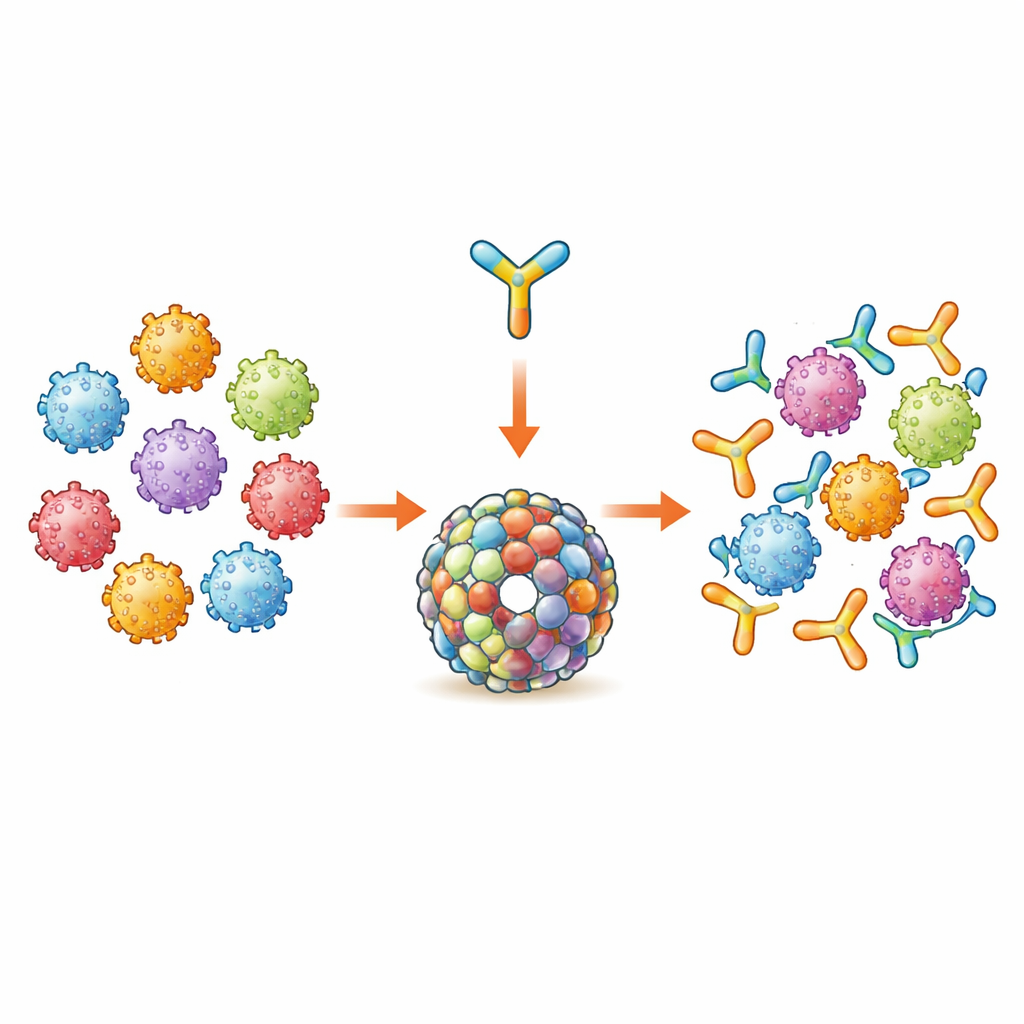
Nowy element budulcowy dla ochrony przed HPV
Obecne szczepionki przeciw HPV opierają się na białku kapsydu wirusa zwanego L1, które samoistnie składa się w cząstki podobne do wirusa i silnie stymuluje produkcję przeciwciał, ale głównie przeciw kilku typom HPV uwzględnionym w danej szczepionce. Zespół skoncentrował się zamiast tego na drugim białku wirusa, L2, które zawiera krótkie regiony podobne w wielu typach HPV i dlatego może wywołać szerszą ochronę. Wykorzystali wcześniej zaprojektowany antygen o nazwie Trx-8mer, w którym krótkie, zachowane fragmenty L2 z ośmiu typów HPV są zszyte razem i prezentowane na stabilnym nośniku białkowym. Wcześniejsze prace wykazały już, że połączenie siedmiu takich jednostek Trx-8mer w pierścieniowy kompleks (szczepionka nazwana PANHPVAX) wywołuje silne, krzyżowo ochronne odpowiedzi przeciwciał i jest obecnie wczesnym etapem badań klinicznych u ludzi.
Przekształcenie białka bakteryjnego w platformę szczepionkową
W tym badaniu badacze próbowali pójść dalej niż siedem kopii i umieścić jeszcze więcej antygenów L2 w każdej cząstce, wychodząc z założenia, że silnie powtarzalne wzory szczególnie dobrze aktywują komórki B produkujące przeciwciała. Wybrali niewielkie, odporne na wysoką temperaturę białko pochodzące z bakterii gruźlicy, zwane dodecyną, które naturalnie składa się w puste kule złożone z dwunastu identycznych podjednostek. Poprzez genetyczne połączenie Trx-8mer z dodecyną stworzyli kilka nowych kandydatów na szczepionkę zaprojektowanych do samoskładania w multimerowe nanocząstki prezentujące wiele kopii L2. Te cząstki można było wytwarzać w bakteriach, oczyszczać w wysokiej temperaturze dzięki ich odporności i potwierdzać wieloma metodami biofizycznymi, że tworzą zamierzone struktury na poziomie nanometrowym.
Kiedy bezpośrednie złączenie nie wystarcza
Zaskakująco, samo przytwierdzenie ładunku L2 bezpośrednio do rusztowania dodecyny nie przewyższyło referencyjnej szczepionki heptamerowej PANHPVAX u myszy. Chociaż multimerowe cząstki tworzyły się zgodnie z planem i indukowały przeciwciała neutralizujące zarówno przeciw typom uwzględnionym w szczepionce, jak i poza nią, miana były generalnie niższe niż te obserwowane po PANHPVAX. Dodanie wbudowanego epitopu pomocniczych komórek T, który czasami wzmacnia odpowiedź przeciwciał, również nie poprawiło wyników. Modelowanie strukturalne i dane funkcjonalne sugerowały, że masywne, bezpośrednio złączone jednostki Trx-8mer mogły się wzajemnie blokować i ukrywać krytyczne regiony L2 przed receptorami komórek B, osłabiając odpowiedź immunologiczną, mimo teoretycznie większej liczby kopii antygenu.
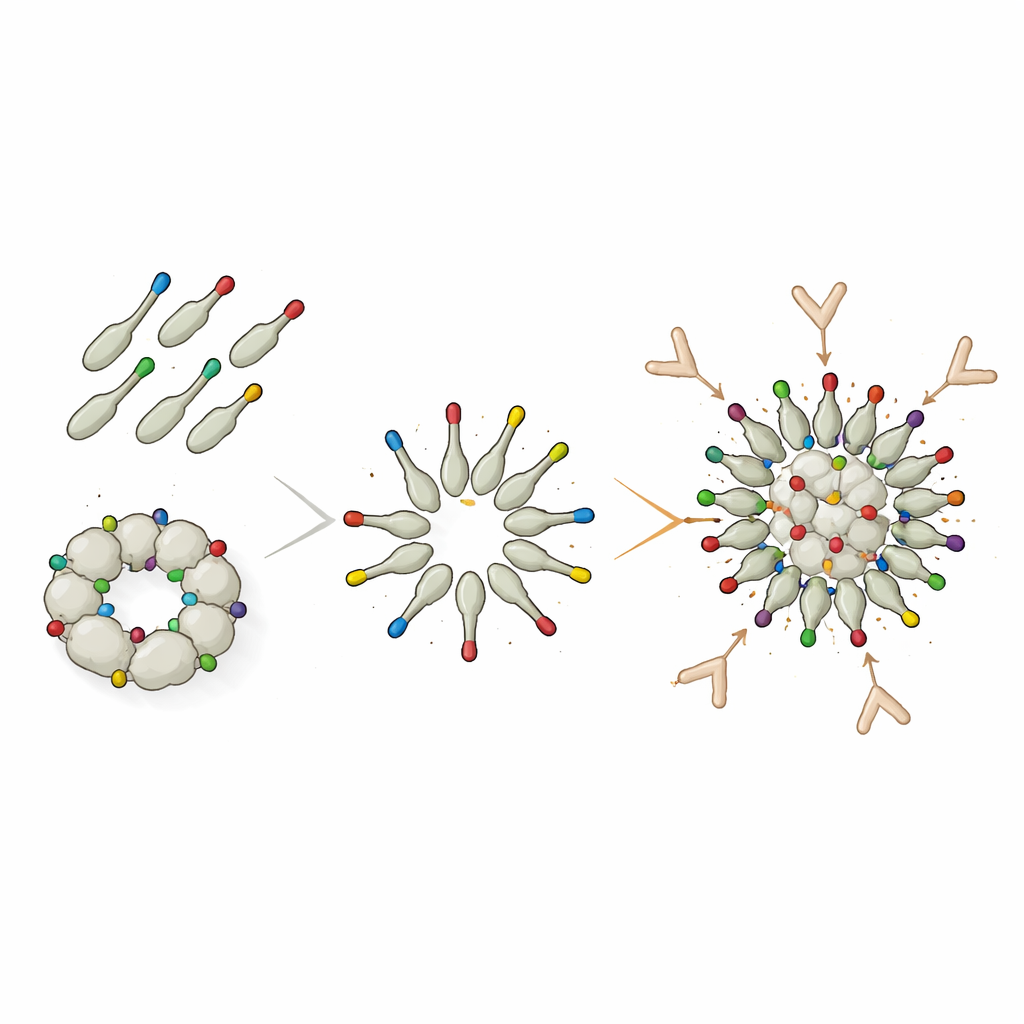
„Klikalne” doczepianie radykalnie zwiększa odpowiedzi
Aby przezwyciężyć te ograniczenia strukturalne, zespół przeszedł na modułowy system „białkowego kleju” o nazwie DogTag/DogCatcher. W tym rozwiązaniu dodecyna była najpierw produkowana z jedynie małym peptydem DogTag na powierzchni, co pozwalało jej swobodnie składać się w czyste nanocząstki. Osobno antygen Trx-8mer połączono z odpowiadającym mu partnerem DogCatcher. Po wymieszaniu Tag i Catcher łączyły się za pomocą spontanicznego wiązania kowalencyjnego, przytwierdzając jednostki Trx-8mer niosące L2 do uprzednio uformowanych cząstek dodecyny. Chociaż tylko około połowa Trx-8mer faktycznie przyczepiła się do nanocząstek, a reszta pozostała wolna w roztworze, myszy immunizowane tym „ozdobionym” konstruktem wytworzyły znacznie wyższe miana przeciwciał neutralizujących przeciw kilku wysokiego ryzyka typom HPV niż w przypadku cząstek z bezpośrednim złączeniem. Dla niektórych typów, takich jak HPV16, ozdobione cząstki przewyższały nawet PANHPVAX.
Implikacje dla przystępnych, szerokich szczepionek przeciw HPV
Podsumowując, badanie pokazuje, że sposób rozmieszczenia antygenów w przestrzeni może mieć większe znaczenie niż liczba kopii przedstawiona „na papierze”. Uprzednie zmontowanie wytrzymałego rusztowania nanocząsteczkowego, a następnie „przyczepienie” do niego antygenów dało fragmentom L2 korzystniejsze odstępy i orientację, prowadząc do silniejszych i szerszych odpowiedzi przeciwciał u myszy. Ponieważ cząstki oparte na dodecynie są małe, wysoce termostabilne i produkowane w bakteriach, stanowią obiecujących kandydatów na szczepionki kolejnej generacji przeciw HPV, które mogłyby być tańsze w wytwarzaniu i mniej zależne od chłodzenia. Przy dalszym udoskonaleniu i testach ta modułowa platforma mogłaby wspierać szczepionki chroniące przed wieloma typami HPV w jednym, dostępnym zastrzyku, a nawet zostać dostosowana do łączenia komponentów prewencyjnych i terapeutycznych w tej samej nanocząstce.
Cytowanie: Kaplan, E., Mariz, F.C., Zhao, X. et al. Assessment of Mycobacterium tuberculosis dodecin scaffold as a multimerization platform on the immunogenicity of HPV L2 antigens. Sci Rep 16, 9086 (2026). https://doi.org/10.1038/s41598-026-42678-7
Słowa kluczowe: szczepionka przeciw HPV, immunogen nanocząsteczkowy, antygen L2, rusztowanie dodecyny, konjugacja białkowa