Clear Sky Science · pl
Mapowanie nocnej pobudliwości w zaburzeniach snu i bólu
Dlaczego niespokojne noce mają znaczenie
Większość z nas wyobraża sobie sen jako gładki, cichy stan, ale pod powierzchnią mózg nieustannie reguluje głębokość odpoczynku. Drobne wybuchy aktywności — krótkie „poruszenia”, które nie wybudzają nas całkowicie — pomagają utrzymać sen stabilnym. W tym badaniu pytano, jak te ukryte poruszenia rozwijają się w ciągu nocy w kilku stanach powiązanych z zaburzonym snem: w zaburzeniu zachowania podczas snu REM, narkolepsji, terrorach nocnych i somnambulizmie oraz w przewlekłym bólu związanym z fibromialgią. Śledząc te zmiany moment po momencie, zamiast jedynie liczyć godziny w poszczególnych stadiach snu, autorzy mają nadzieję ujawnić wzory, które kiedyś mogłyby wspierać diagnostykę i leczenie.
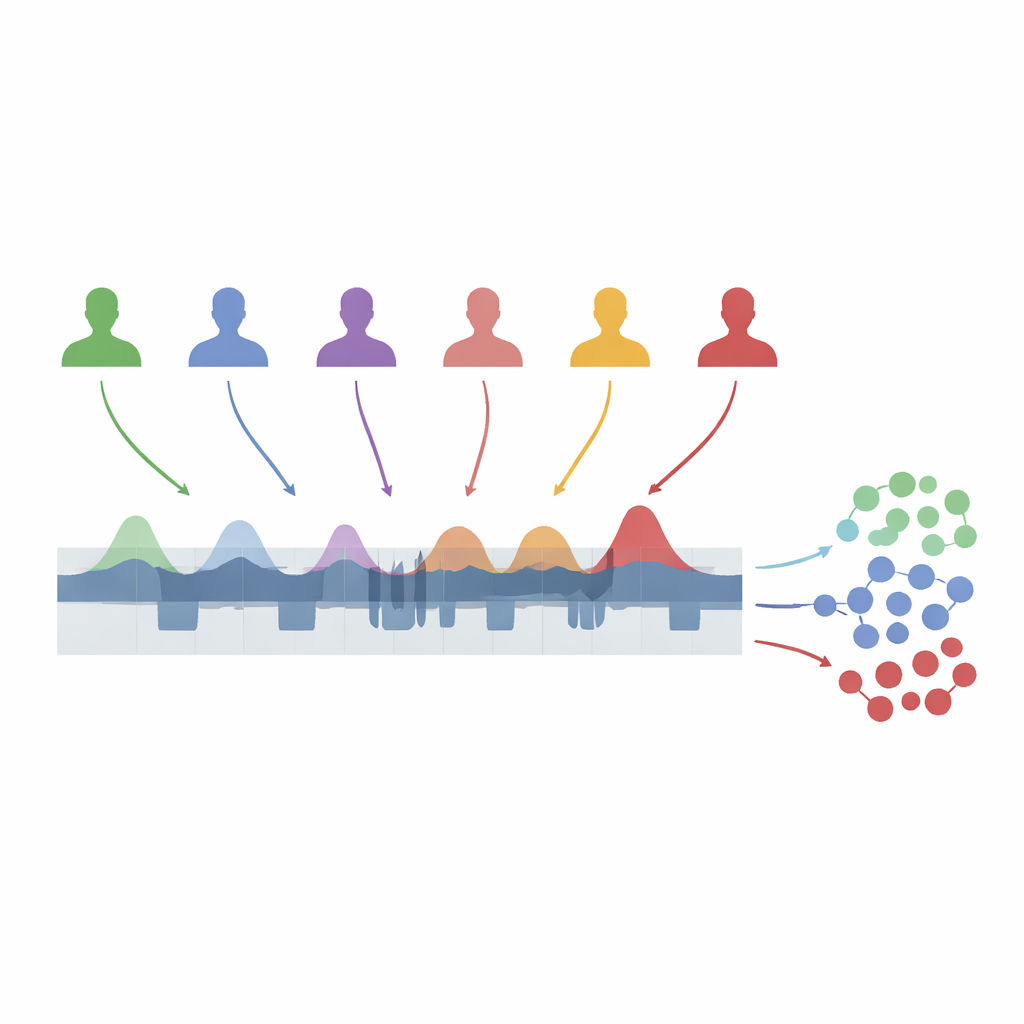
Ukryty rytm w głębokim śnie
Podczas snu bez szybkich ruchów gałek ocznych (non‑REM) mózg naprzemiennie przechodzi spokojniejsze okresy i krótkie wybuchy aktywności. Badacze snu nazywają to cyklicznym wzorcem naprzemiennym: krótkimi fazami „A” aktywacji, po których następują spokojniejsze fazy „B”. W obrębie faz A wyróżnia się trzy odmiany. Pierwszy podtyp, A1, łączy się mocno z wolnymi, dużymi falami mózgowymi i prawdopodobnie pomaga utrzymać stabilność głębokiego snu. Drugi i trzeci, A2 i A3, odzwierciedlają stopniowo silniejszą aktywację i zbliżają mózg do pobudzenia. Zamiast traktować te zdarzenia jako losowy szum, ostatnie prace postrzegają je jako kluczowy element równoważenia przez mózg potrzeby pozostania w śnie z koniecznością pozostawania wrażliwym na otoczenie.
Nowy sposób śledzenia nocnej pobudliwości
Zespół przeanalizował nocne zapisy fal mózgowych od 109 dorosłych: zdrowych ochotników oraz pacjentów z idiopatycznym zaburzeniem zachowania podczas snu REM, narkolepsją typu 1, parasomniami non‑REM i fibromialgią. Korzystając z zautomatyzowanego algorytmu wytrenowanego na danych oznaczonych przez ekspertów, wykrywali każdy moment, w którym mózg wchodził w A1, A2 lub A3 podczas snu non‑REM. Podzielili potem noc każdej osoby na jednosekundowe bloki i obliczyli, dla każdego bloku, jaka część czasu przypadała na dany podtyp. Ten „wskaźnik fazy A” daje bieżący pomiar tego, jak często mózg jest krótko aktywowany, bez prób rekonstruowania każdego pełnego cyklu aktywacji i spokoju. Aby porównać osoby o bardzo różnych porach zasypiania i długości snu, autorzy rozciągnęli każdą noc na standardową skalę od zgaszenia świateł do włączenia świateł rano.
Jak różne zaburzenia przekształcają nocną podróż
U zdrowych śpiących zdarzenia A1 były najczęstsze na początku nocy, gdy ciśnienie snu jest wysokie, a następnie stopniowo zanikały ku porankowi. Pasuje to do koncepcji, że silne, wolne fale pomagają stabilizować pierwsze cykle głębokiego snu i są potem coraz mniej potrzebne, gdy mózg się regeneruje. We wszystkich grupach uczestników A2 i A3 były mniej wyraźne i zmieniały się łagodniej w czasie. Dla odmiany wszystkie cztery stany kliniczne wykazały stłumioną wersję zdrowego wzorca A1. Osoby z zaburzeniem zachowania podczas snu REM i te z narkolepsją miały zauważalnie mniej zdarzeń A1 i A2 w średnio‑głębokim etapie snu non‑REM, a osoby z zaburzeniem zachowania podczas snu REM dodatkowo brak A1 w najgłębszym etapie. Fibromialgia wykazywała szeroki spadek zarówno A1, jak i A2, szczególnie w tym średnio‑głębokim etapie. Parasomnie non‑REM wyróżniały się: pokazywały wczesnonocny skok A1 i A2 podczas lekkiego snu, ale później redukcję A1 w śnie głębokim. Razem te profile sugerują, że każde zaburzenie ma własny „odcisk palca” dotyczący sposobu, w jaki krótkie wybuchy pobudzenia mózgu są utkane przez noc.
Co wzory mogą znaczyć dla mózgu
Te charakterystyczne dla zaburzeń odciski palca wskazują na różne rodzaje nierównowagi między systemami promującymi głębokie, regenerujące fale wolne a systemami skłaniającymi mózg ku pobudzeniu. Zmniejszenie A1 i A2 w zaburzeniu zachowania podczas snu REM i narkolepsji może odzwierciedlać słabsze uruchamianie stabilizujących odpowiedzi związanych z falami wolnymi, co sprawia, że sen jest bardziej kruche, nawet gdy całkowity czas głębokiego snu wydaje się normalny. W parasomniach mieszanka dodatkowej aktywacji podczas lekkiego snu i słabszego buforowania w śnie głębokim pasuje do koncepcji niestabilnych granic między stanami snu i czuwania, które mogą prowadzić do dramatycznych zachowań, takich jak chodzenie po śnie. W fibromialgii szeroka utrata A1 i A2 może pomóc wyjaśnić, dlaczego sen może wydawać się nienapawający energią mimo pozornie normalnej ilości snu głębokiego: drobnoziarnista, ochronna mikrostruktura jest zmieniona, co może zwiększać wrażliwość na ból i inne doznania.
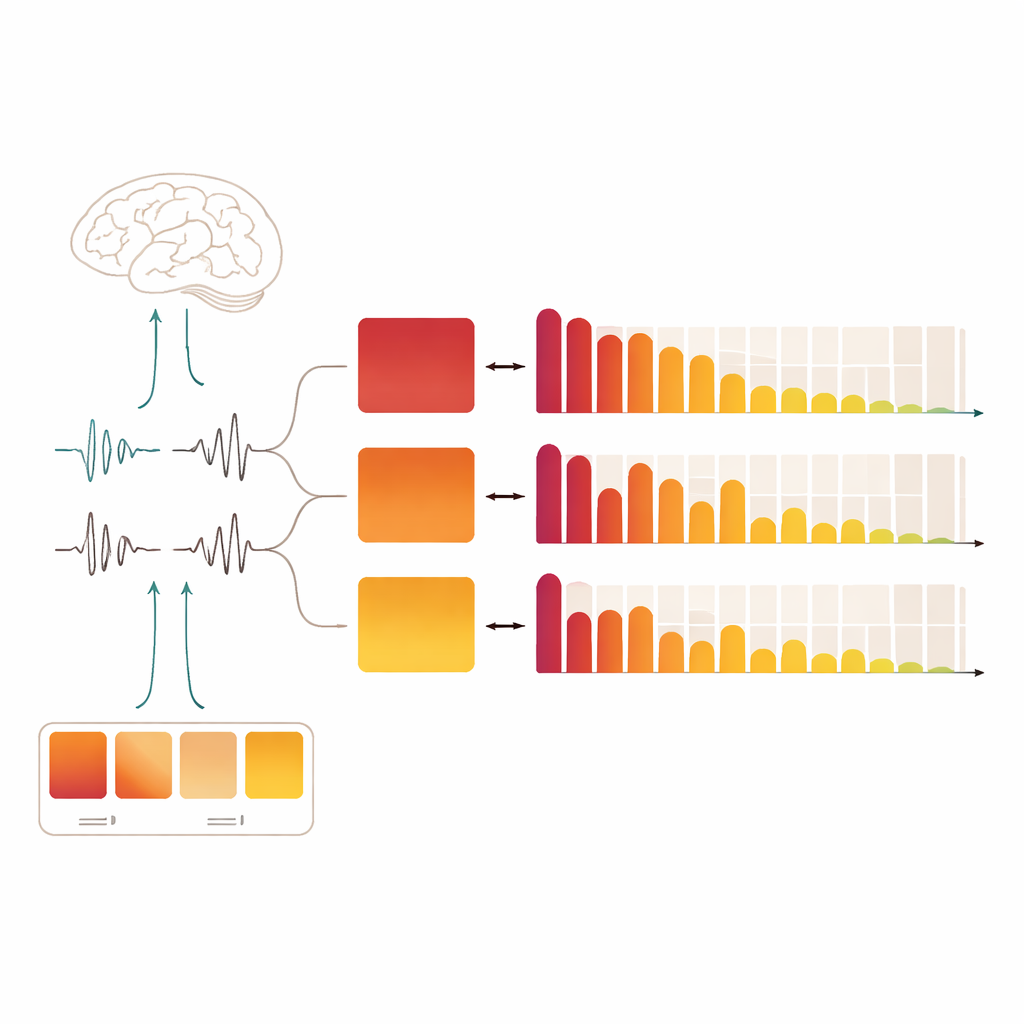
Od opisowych map do przyszłych narzędzi snu
Autorzy podkreślają, że ich praca ma charakter eksploracyjny: wielkości grup były umiarkowane, zdrowi ochotnicy nie byli idealnie dopasowani do pacjentów, a oni skupili się tylko na aktywnych fazach A, nie na pełnych cyklach obejmujących spokojniejsze fazy B. Mimo to wyniki pokazują, że śledzenie wzrostów i spadków krótkich zdarzeń pobudzeniowych w ciągu nocy może ujawnić wyróżniające się sygnatury różnych zaburzeń snu i bólu. Jeśli potwierdzą to większe, prospektywne badania, tego rodzaju mapowanie przez całą noc mogłoby przyczynić się do nowych biomarkerów — obiektywnych miar pomagających klasyfikować pacjentów, śledzić przebieg choroby i ukierunkowywać terapie, które regulują równowagę między stabilnością a pobudzeniem w śnie, zamiast jedynie usypiać pacjentów.
Cytowanie: Biabani, N., Mendonça, F., Mutti, C. et al. Mapping nocturnal arousal across sleep and pain disorders. Sci Rep 16, 8668 (2026). https://doi.org/10.1038/s41598-026-42639-0
Słowa kluczowe: mikrostruktura snu, nocna pobudliwość, cykliczny wzorzec naprzemienny, zaburzenia snu, fibromialgia i sen