Clear Sky Science · pl
GV1001 redukuje patologiczne 4R tau i deficyty funkcjonalne w modelach istotnych dla postępującego porażenia nadjądrowego
Dlaczego to ma znaczenie dla pacjentów i rodzin
Postępujące porażenie nadjądrowe (PSP) to rzadka, lecz wyniszczająca choroba mózgu, która w ciągu zaledwie kilku lat odbiera ludziom równowagę, sprawność ruchową i jasne myślenie. Obecnie nie ma leków, które mogłyby spowolnić jej postęp. To badanie analizuje małą cząsteczkę leku o nazwie GV1001, opracowaną pierwotnie w onkologii, i wykazuje, że może ona łagodzić problemy z ruchem oraz zmniejszać kluczowe zmiany chorobowe w komórkach mózgu w modelach laboratoryjnych PSP. Praca ta sugeruje nowe podejście do grupy schorzeń napędzanych przez szkodliwą postać białka tau.
Pomocnik ruchu w mózgu, który zawodzi
Wiele chorób mózgu wiąże się z tau — białkiem, które normalnie stabilizuje wewnętrzne „tory”, po których transportowane są materiały w komórkach nerwowych. W PSP gromadzi się szczególna postać, zwana 4R tau, w określonych głębokich obszarach mózgu, zwłaszcza w śródmózgowiu, gdzie zaburza strukturę komórek, uszkadza połączenia i ostatecznie prowadzi do ich obumierania. U chorych pojawia się sztywność, upadki, problemy z ruchem oczu i zaburzenia poznawcze, często prowadzące do szybkiego pogorszenia w ciągu pięciu do ośmiu lat. W przeciwieństwie do choroby Alzheimera, PSP jest zdominowane przez formę 4R tau, co czyni ją ważnym celem dla terapii ukierunkowanych na zaburzenia ruchowe związane z tau.
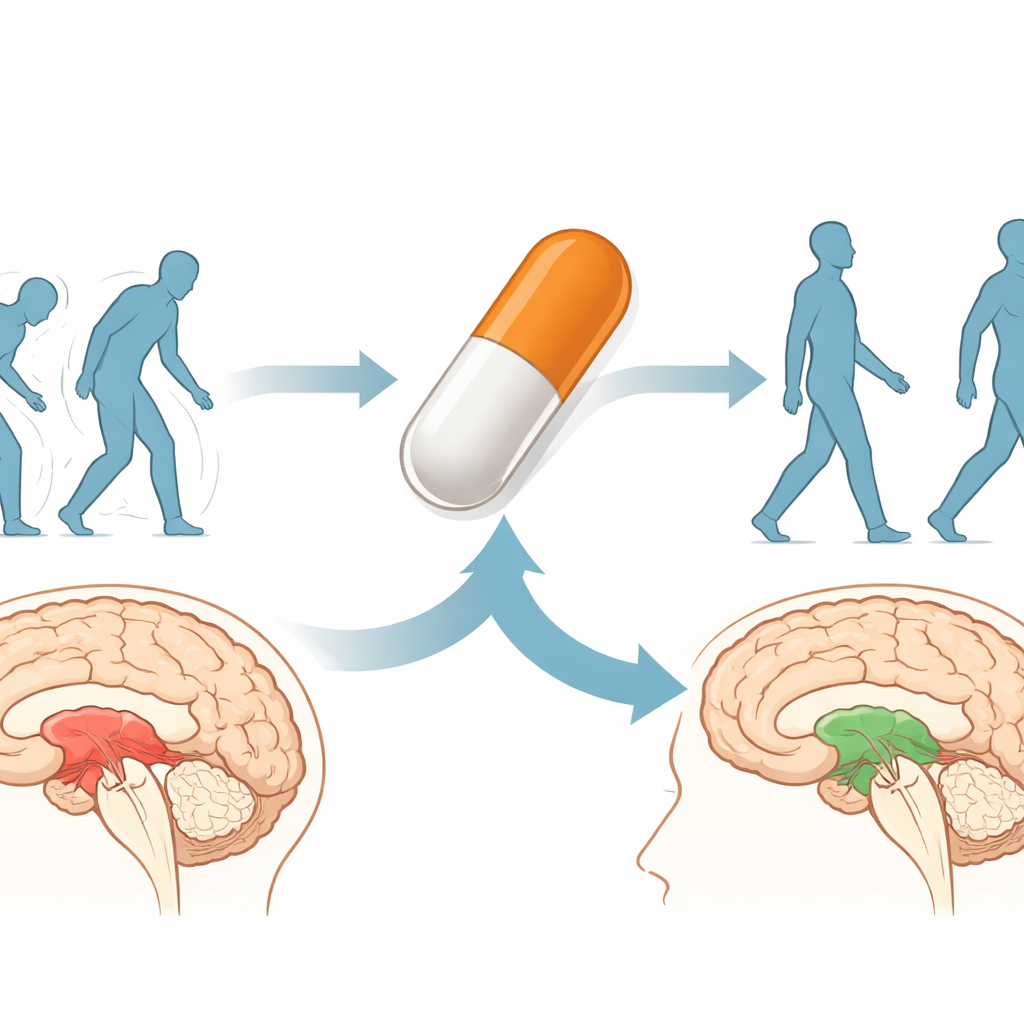
Kandydat z onkologii znajduje nowe zastosowanie
GV1001 to krótki peptyd pochodzący z ludzkiej telomerazy, enzymu aktywnego w wielu nowotworach. Był już testowany w różnych guzach, a w ostatnim czasie także w schorzeniach takich jak powiększona prostata czy choroba Alzheimera, z ogólnie dobrym profilem bezpieczeństwa. Wcześniejsze prace wykazały, że GV1001 może chronić komórki mózgowe przed uszkodzeniem oksydacyjnym, wspierać mitochondria produkujące energię oraz łagodzić reakcje zapalne w mózgu. Obecne badanie sprawdza, czy te szerokie działania ochronne, wraz z ewentualnymi nowymi efektami, mogą uczynić GV1001 użytecznym w zaburzeniach, gdzie 4R tau jest głównym winowajcą, takich jak PSP.
Testowanie ruchu, pamięci i zmian mózgowych u myszy
Naukowcy użyli specjalnie zmodyfikowanej myszy, która produkuje humanopodobne 4R tau skłonne do agregacji, co z czasem prowadzi do problemów z ruchem i pamięcią. Od siódmego miesiąca życia myszy otrzymywały GV1001 podskórnie trzy razy w tygodniu przez około pięć miesięcy. W porównaniu z zwierzętami nieleczonymi, myszy leczone GV1001 dłużej utrzymywały się na wirującym rotarodzie, przemieszczały się dalej i szybciej na otwartej arenie oraz lepiej rozpoznawały nowe przedmioty, co sugeruje poprawę zdolności motorycznych i pamięci. Po zbadaniu mózgów odkryto mniejsze agregacje tau i mniej chemicznych znaczników związanych z „nadaktywnością” tau w wielu obszarach, w tym w korze, hipokampie i istocie czarnej, wszystkich istotnych dla ruchu i funkcji poznawczych.
Zajrzeć do komórek i uciszyć zapalenie mózgu
Poza samym tau, PSP i pokrewne choroby cechuje utrata synaps — punktów kontaktu między komórkami nerwowymi — oraz nadmierna aktywacja komórek wspierających zwanych astrocytami i mikroglejem, które napędzają przewlekłe zapalenie. U leczonych myszy poziomy kluczowych białek synaptycznych wróciły w kierunku normy, co sugeruje, że GV1001 pomaga zachować połączenia nerwowe. Markery aktywowanych astrocytów i mikrogleju obniżyły się, zarówno w mózgach myszy, jak i w ludzkich liniach komórkowych pobudzonych do stanu przypominającego zapalenie. Lek zmniejszył także poziomy TSPO, białka używanego w badaniach obrazowych do śledzenia zapalenia mózgu, co stwarza możliwość, że przyszłe badania obrazowe mogłyby monitorować wpływ GV1001 u pacjentów.
Bezpośrednie ukierunkowanie szkodliwej formy 4R tau
Aby sprawdzić, czy GV1001 wpływa specyficznie na 4R tau, zespół stworzył model komórkowy PSP, różnicując ludzkie komórki o cechach nerwowych i eksponując je na annonacynę, toksynę roślinną uszkadzającą mitochondria i zwiększającą 4R tau. Jak oczekiwano, annonacyna gwałtownie zwiększyła ilość 4R tau bez zmiany całkowitej ilości tau. Gdy GV1001 dodano po wystąpieniu tego uszkodzenia, nadmiar 4R tau i stosunek 4R tau do tau całkowitego spadły w kierunku normy, podczas gdy poziom całkowitego tau pozostał w dużej mierze niezmieniony. Podobne selektywne redukcje 4R tau zaobserwowano w mózgach leczonych myszy. Wyniki te sugerują, że GV1001 robi więcej niż tylko ogólną ochronę komórek — wydaje się regulować w dół tę formę tau, ściśle powiązaną z PSP.
Co to może znaczyć dla przyszłych terapii
Podsumowując, wyniki pokazują, że GV1001 może poprawiać ruch i pamięć, zmniejszać toksyczne zmiany tau, chronić synapsy i łagodzić zapalenie mózgu w modelach odzwierciedlających kluczowe aspekty PSP i innych chorób napędzanych przez 4R tau. Wstępne badania kliniczne u osób z PSP już zasugerowały spowolnienie pogarszania się objawów i dobrą tolerancję, choć potrzebne są znacznie większe i dłuższe badania. Dla pacjentów i rodzin praca ta daje ostrożne przesłanie optymizmu, że lek pierwotnie zaprojektowany do leczenia nowotworów może zostać ponownie wykorzystany, by spowolnić przebieg szybko postępującej choroby mózgu, celując w jej podstawową nieprawidłowość białkową.
Cytowanie: Jang, KB., Kang, D.M., Lee, MH. et al. GV1001 reduces pathological 4R tau and functional deficits in models relevant to progressive supranuclear palsy. Sci Rep 16, 8638 (2026). https://doi.org/10.1038/s41598-026-42195-7
Słowa kluczowe: postępujące porażenie nadjądrowe, białko tau, 4R tauopatia, neurozapalność, GV1001