Clear Sky Science · pl
Wieloośrodkowe kliniczno‑patologiczne badanie zmian z zakresu spektrum miozomu odontogennego z wykorzystaniem patologii ilościowej
Dlaczego to ma znaczenie dla pacjentów i stomatologów
Głęboko w kości szczęki rzadkie guzki mogą przez miesiące lub lata rosnąć bezobjawowo, zanim zostaną wykryte. Zmiany te, nazywane miozomami odontogennymi i miozofibromami, nie są nowotworami złośliwymi, ale mogą się rozrastać, osłabiać kość i utrudniać zabieg chirurgiczny. Przez dekady patolodzy oceniali je głównie „na oko”, co powodowało rozbieżności w opisie i klasyfikacji podobnych zmian w różnych ośrodkach. To badanie wprowadza zaawansowane narzędzia analizy obrazu do pracy ze szkiełkiem mikroskopowym, pokazując, jak sztuczna inteligencja (AI) może pomóc lekarzom widzieć te guzy wyraźniej i bardziej konsekwentnie.
Rzadkie guzy szczęki o myląco podobnym wyglądzie
Miozom odontogenny i miozofibroma odontogenna powstają z tkanek zaangażowanych w powstawanie zębów. Oba to miękkie, galaretowate zmiany osadzone w kości szczęki. Pod mikroskopem zawierają mieszaninę luźnych, myksoidalnych obszarów i gęstszych pasm włóknistych. Tradycyjnie patolodzy starali się je rozróżniać, szacując, jaka część guza jest włóknista, a jaka myksoidalna. Jednak te guzy są rzadkie i brak ogólnie przyjętych zasad określających, ile tkanki włóknistej wystarczy, by zmienić rozpoznanie z jednej nazwy na inną. W rezultacie różne szpitale mogą nadawać różne nazwy bardzo podobnym zmianom, mimo że pacjenci mają porównywalne objawy i wyniki badań obrazowych.
Przekształcanie preparatów mikroskopowych w liczby
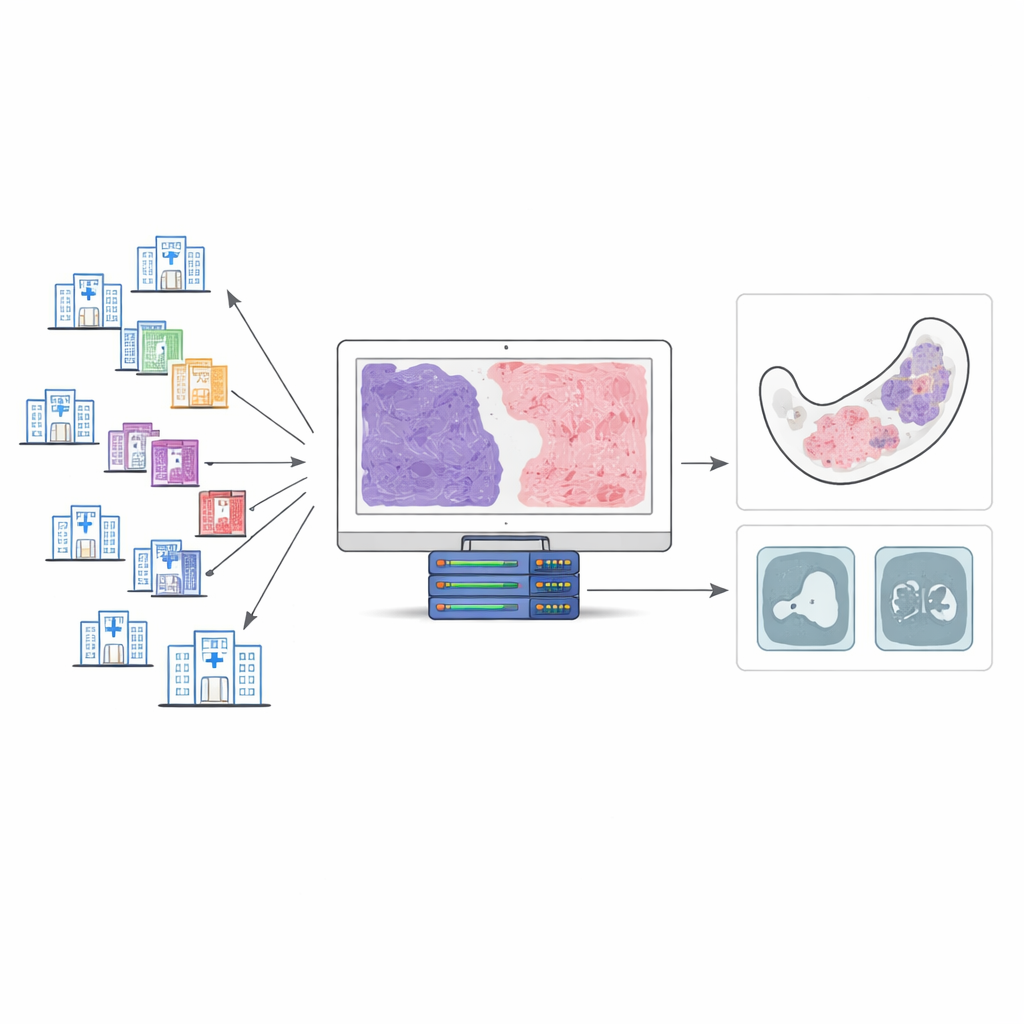
Zespół badawczy zgromadził 143 próbki tkanek od pacjentów leczonych w 34 szpitalach na przestrzeni dwóch dekad, ostatecznie koncentrując się na 100 przypadkach spełniających rygorystyczne kryteria jakości. Wszystkie próbki zabarwiono specjalnym barwnikiem (trichrom Massona), który różnicuje tkankę włóknistą od otaczającej zmiany. Dwaj eksperci – patolodzy jamy ustnej – dokładnie przejrzeli każdy przypadek i oszacowali odsetek tkanki włóknistej w krokach co 10%. Te oceny ekspertów posłużyły jako odniesienie do wytrenowania systemu AI, aby wykonywał to samo zadanie automatycznie, ale w sposób w pełni ilościowy.
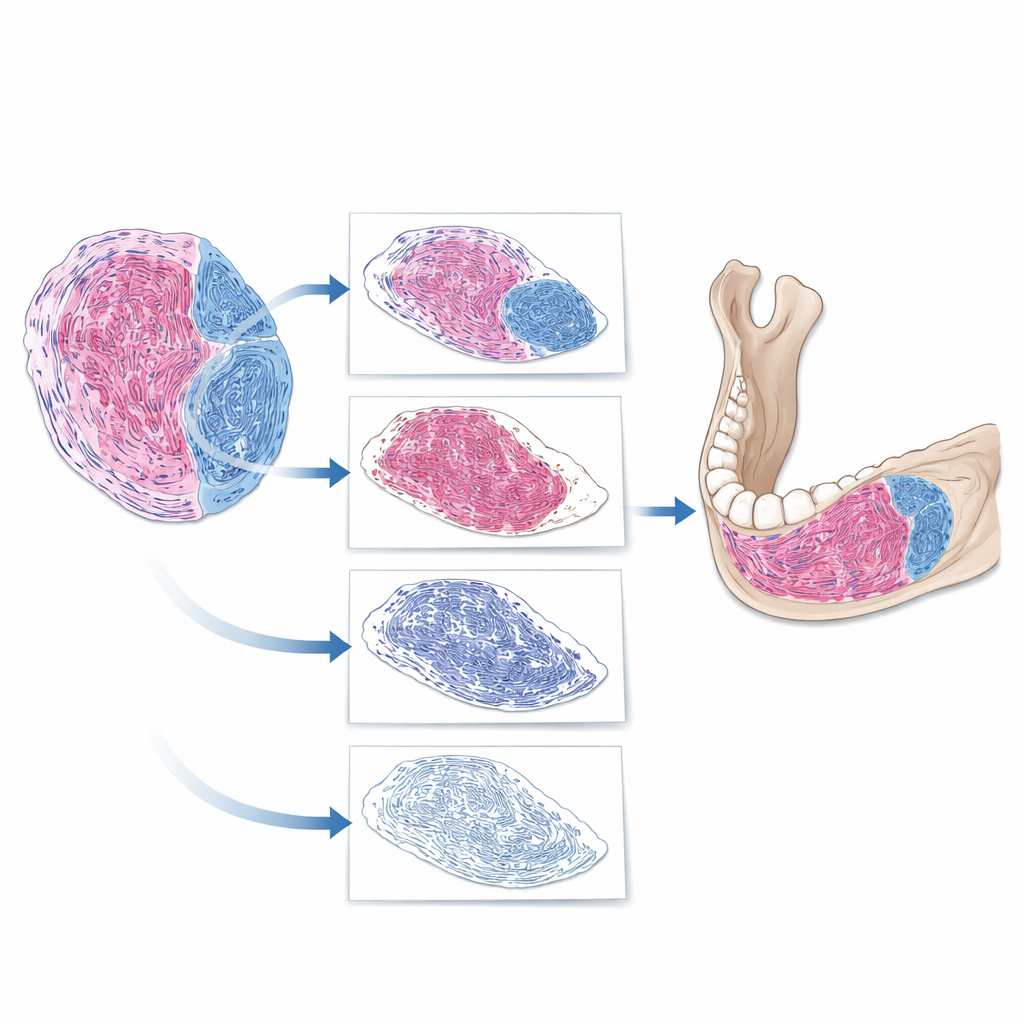
Jak AI „czyta” preparat
Zespół zbudował krokowy cyfrowy pipeline do analizy obrazów całych szkiełek. Najpierw oprogramowanie oddzieliło rzeczywistą tkankę od pustego tła preparatu. Następnie wyizolowało guz od sąsiednich struktur, takich jak kość i zęby. W końcu, w obrębie guza, usunęło jądra komórkowe i skupiło się na pozostałej substancji, identyfikując obszary przyjmujące barwnik charakterystyczny dla tkanki włóknistej. Na tej podstawie AI obliczyło proporcję tkanki włóknistej: pole zajmowane przez tkankę włóknistą podzielone przez całkowitą powierzchnię guza. Gdy badacze porównali wartości wygenerowane przez AI z ocenami ekspertów, zgodność była wysoka, z rozrzutem około 10 punktów procentowych w większości pojedynczych przypadków. Sugeruje to, że AI może wiarygodnie odzwierciedlać ocenę ekspercką, jednocześnie wyrażając ją jako precyzyjne pomiary zamiast przybliżonych wrażeń.
Co skład włóknisty mówi o wyglądzie guza
Dysponując tymi pomiarami, badacze sprawdzili, jak zawartość tkanki włóknistej wiąże się z cechami klinicznymi i radiologicznymi. Stwierdzili, że ilość tkanki włóknistej znacznie różniła się między instytucjami, odzwierciedlając różnice w pierwotnym opisywaniu guzów przez patologów. W analizie obrazów wyróżnił się jeden wzorzec: guzy wyglądające na jedną jamę w badaniach (zmiany jednokomorowe) miały zwykle wyższy udział tkanki włóknistej niż te o wielu małych przegrodach (zmiany wielokomorowe). Zgodne jest to z ideą, że bardziej włóknista, zwarta tkanka może tworzyć jednorodną, jednokomorową masę, podczas gdy luźniejsza, bogata w płyn tkanka może rozdzielać się na kilka przestrzeni.
Co to oznacza dla przyszłej diagnostyki i opieki
Badanie nie ma na celu zmiany nazw chorób ani zastąpienia patologów maszynami. Pokazuje natomiast, że ilościowa patologia wspomagana AI może dostarczyć wspólnej miary dla rzadkich guzów szczęki w wielu ośrodkach. Przekształcając subtelne tekstury tkanki w powtarzalne liczby, podejście to ujawnia, jak bardzo codzienne rozpoznania zależą od subiektywnej oceny i oferuje sposób ograniczenia tej zmienności. Dla pacjentów bardziej spójna interpretacja takich zmian może wspierać jasniejsze decyzje terapeutyczne i lepsze porównywanie wyników leczenia między centrami. W miarę jak podobne metody będą stosowane do innych rzadkich guzów, mikroskopia wspomagana AI może po cichu przekształcać sposób, w jaki patolodzy widzą chorobę — czyniąc ich oceny bardziej porównywalnymi i ostatecznie bardziej użytecznymi, niezależnie od miejsca leczenia pacjenta.
Cytowanie: Harazono, Y., Fukawa, Y., Iwasaki, T. et al. Multicenter clinicopathological study of odontogenic myxoma spectrum lesions using quantitative pathology. Sci Rep 16, 11221 (2026). https://doi.org/10.1038/s41598-026-42019-8
Słowa kluczowe: miozom odontogenny, guzy żuchwy, patologia cyfrowa, sztuczna inteligencja, proporcja tkanki włóknistej