Clear Sky Science · pl
Wizualizacja progresji złośliwej: śródmiejscowy test immunofluorescencyjny oparty na CD109 wyznacza przejście od raka tarczycy brodawkowatego do anaplastycznego w mikrośrodowisku guza
Dlaczego to badanie raka tarczycy jest istotne
Anaplastyczny rak tarczycy jest jednym z najbardziej śmiertelnych nowotworów u ludzi — często przekształca zwykle uleczalny guz tarczycy w chorobę szybko prowadzącą do zgonu. Lekarze wciąż nie rozumieją w pełni, jak powszechny, wolno rosnący rak brodawkowaty może nagle przemienić się w tę agresywną postać. To badanie śledzi tę transformację bezpośrednio w obrębie guza pacjenta, wykorzystując nową technikę obrazowania do obserwacji krok po kroku, jak komórki nowotworowe i ich otoczenie zmieniają się. Praca dostarcza bardziej szczegółowego obrazu tego, jak lokalne warunki w mikrośrodowisku guza mogą popychać komórki w kierunku bardziej śmiertelnego stanu, sugerując nowe sposoby spowolnienia lub zapobiegania tej przemianie.
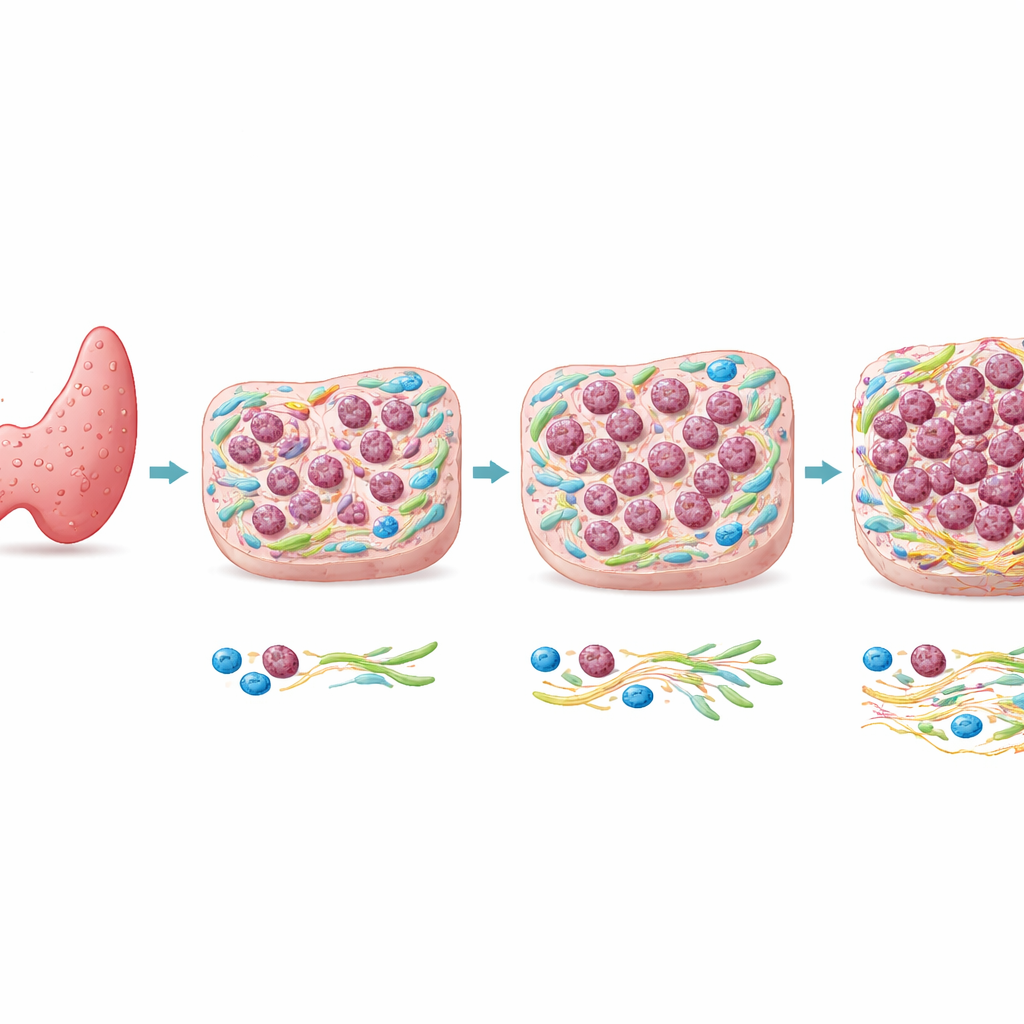
Od powszechnego guza do rzadkiego zabójcy
Większość raków tarczycy to brodawkowate raki tarczycy (PTC), które zwykle rosną wolno i mają doskonałe rokowania. Anaplastyczny rak tarczycy (ATC) jest natomiast rzadki, ale często śmiertelny w ciągu kilku miesięcy. Badania genetyczne wykazały, że ATC i sąsiednie PTC u tego samego pacjenta często dzielą wiele tych samych mutacji DNA, w tym zmiany w dobrze znanych genach rakowych. Ta podobieństwo sugeruje, że same geny mogą nie wyjaśniać, dlaczego tylko niektóre obszary guza stają się anaplastyczne. Autorzy skupili się więc na tym, co dzieje się w krajobrazie tkankowym wokół komórek — w mikrośrodowisku guza — aby sprawdzić, czy lokalne warunki przyczyniają się do tej niebezpiecznej zmiany.
Nowy sposób mapowania raka na miejscu
Zespół opracował przestrzenny test immunofluorescencyjny (SPI), rodzaj wielobarwnej mikroskopii, która mierzy intensywność określonych białek w drobnych, zdefiniowanych polach na przekroju tkanki. Metodę skupiono na CD109, białku powierzchniowym zidentyfikowanym jako marker złośliwego zachowania w tkance tarczycy, oraz CK8/18, białku charakterystycznym dla zwykłych komórek guza brodawkowatego. Poprzez obliczanie stosunku CD109 do CK8/18 w setkach małych regionów, wygenerowano mapy w kodzie kolorów, które oddzielały wyraźne obszary PTC od wyraźnych obszarów ATC i — co istotne — ujawniały strefy pośrednie, gdzie oba markery nakładały się. Zamiast ostrej granicy, przejście od raka brodawkowatego do anaplastycznego ukazało się jako stopniowy, plamisty kontinuum.
Pięć stref wzdłuż drogi przemiany
Aby lepiej zrozumieć to kontinuum, badacze podzielili tkankę na pięć regionów, od czystego PTC do w pełni rozwiniętego ATC. Następnie zbadali wiele dodatkowych białek wskazujących na tożsamość komórek, wzrost, ruch oraz tkankę podporową. W tych regionach klasyczne cechy nabłonkowe, takie jak E-kadheryna i CK8/18, stopniowo malały, podczas gdy markery związane z motoryką komórek i zmianą kształtu, takie jak wimentyna, wzrastały. Białka wskazujące na szybki podział komórek rosły w bardziej anaplastycznych strefach. Jednocześnie komórki wspierające — fibroblasty związane z rakiem — oraz komórki układu odpornościowego, w szczególności pewne makrofagi, stawały się liczniejsze i bardziej aktywowane, a zwiększała się ilość białek, które wytwarzały.
Kiedy rusztowanie guza staje się wrogie
Uderzającą zmianę zaobserwowano w rusztowaniu guza, czyli macierzy pozakomórkowej. W obszarach anaplastycznych komórkopodobne fibroblasty odkładały więcej kolagenów typu III i VI oraz białka macierzy zwanego TGFBI, a włókna te były grubsze, bardziej splątane i ułożone w wielu kierunkach zamiast w gładkie, równoległe linie. Przearanżowana sieć prawdopodobnie sprawia, że tkanka staje się mechanicznie sztywniejsza. W tych sztywniejszych strefach białko sygnalizacyjne wrażliwe na ciśnienie, zwane YAP, było bardziej aktywne zarówno w komórkach nowotworowych, jak i wspierających. Te same obszary wykazywały więcej oznak uszkodzeń DNA i formy zapalnej śmierci komórek, wraz z uwolnieniem białek S100, które mogą działać jako sygnały niebezpieczeństwa i dodatkowo zaogniać środowisko. Autorzy proponują, że to połączenie ucisku, śmierci komórek i przewlekłego zapalenia sprzyja przetrwaniu i rozprzestrzenianiu się już zmutowanych komórek nowotworowych, które potrafią wytrzymać stres i przejść coś na kształt przejścia nabłonkowo-mezenchymalnego.
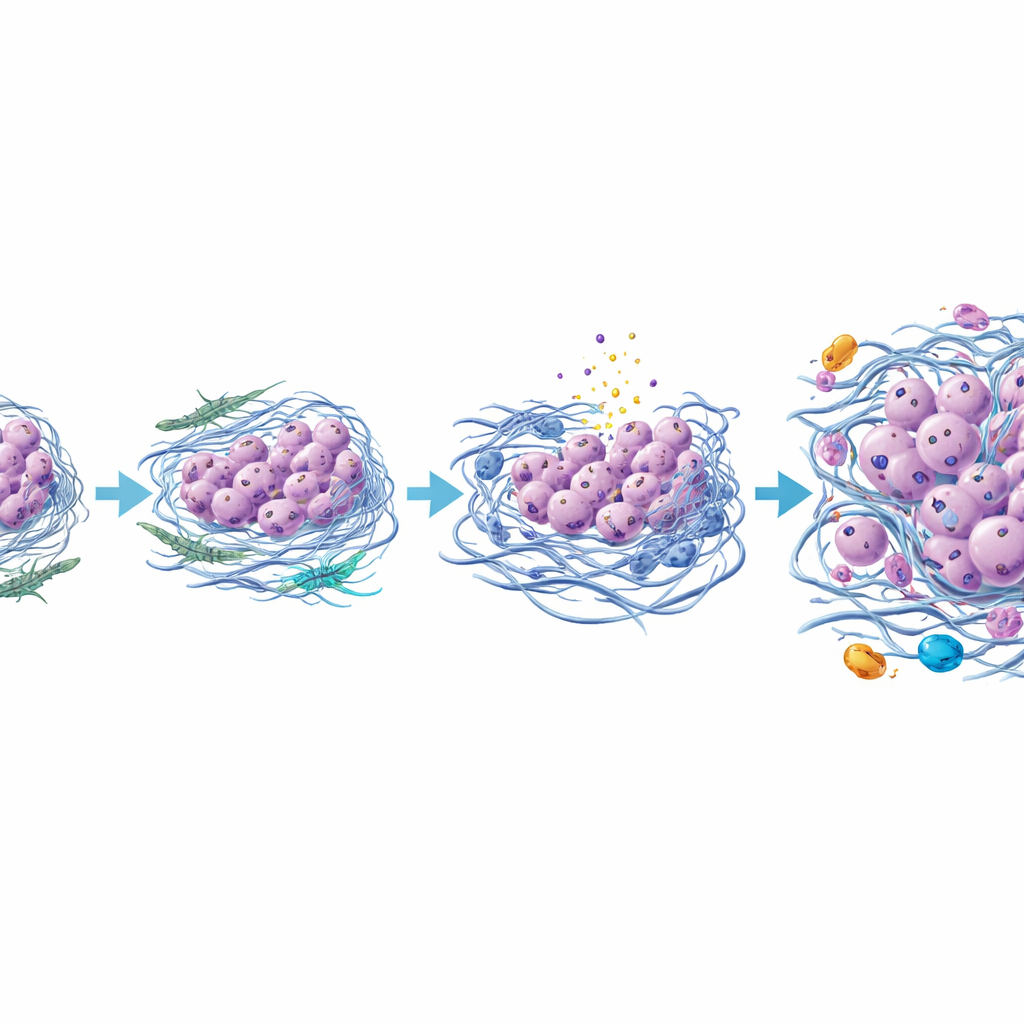
Nowy obraz tego, jak guz tarczycy staje się śmiertelny
Składając te obserwacje razem, badanie sugeruje, że anaplastyczny rak tarczycy powstaje nie tylko w wyniku dodatkowych mutacji genetycznych, lecz także w efekcie przekształconego otoczenia guza. W miarę jak komórki brodawkowatego guza i pobliskie komórki wspierające wchodzą ze sobą w interakcje, niektóre fibroblasty przekształcają się w bardziej agresywny typ, który pogrubia i usztywnia otaczającą macierz, miażdży wrażliwe komórki prowadząc do ich śmierci i przyciąga zapalne komórki odpornościowe. Przetrwałe, bardziej odporne komórki nowotworowe stopniowo tracą swoje pierwotne cechy tarczycy i przyjmują bardziej ruchliwą, inwazyjną tożsamość, ostatecznie tworząc guz anaplastyczny. Choć praca opiera się na jednym dobrze opisanym przypadku i wymaga potwierdzenia u większej liczby pacjentów, wprowadza potężne narzędzie obrazowe i szczegółowy model, w którym ukierunkowanie na komórki wspierające guz, macierz lub sygnały zapalne mogłoby pomóc zapobiec lub opóźnić jedną z najbardziej obawianych przemian w raku tarczycy.
Cytowanie: Cohen, T., Suzuki, K., Matsuda, K. et al. Visualizing malignant progression: in situ CD109-based spatial immunofluorescence assay delineates papillary to anaplastic thyroid carcinoma transformation within the tumor microenvironment. Sci Rep 16, 8682 (2026). https://doi.org/10.1038/s41598-026-41927-z
Słowa kluczowe: anaplastyczny rak tarczycy, brodawkowaty rak tarczycy, mikrośrodowisko guza, sztywność macierzy pozakomórkowej, przestrzenna immunofluorescencja