Clear Sky Science · pl
Ilościowa ocena ex vivo docelowej temperatury i czasu ablacji dla optymalizacji protokołu zabiegów ablacji mikrofalowej z termometrią MR
Obserwowanie leczenia guzów w czasie rzeczywistym
Kiedy lekarze niszczą guzy wątroby przy pomocy ciepła, chcą widzieć dokładnie, które fragmenty narządu ulegają zniszczeniu w trakcie zabiegu. Rezonans magnetyczny (MRI) pozwala „zobaczyć temperaturę” wewnątrz ciała w miarę rozchodzenia się ciepła. W badaniu tym analizowano, jak gorąco i jak długo można bezpiecznie podgrzewać tkankę wątroby podczas ablacji mikrofalowej, zachowując jednocześnie czytelne i wiarygodne mapy temperatury z MRI — ważny krok w kierunku precyzyjniejszych, mniej inwazyjnych metod leczenia nowotworów.
Dlaczego zabiegi termiczne w wątrobie potrzebują lepszej kontroli
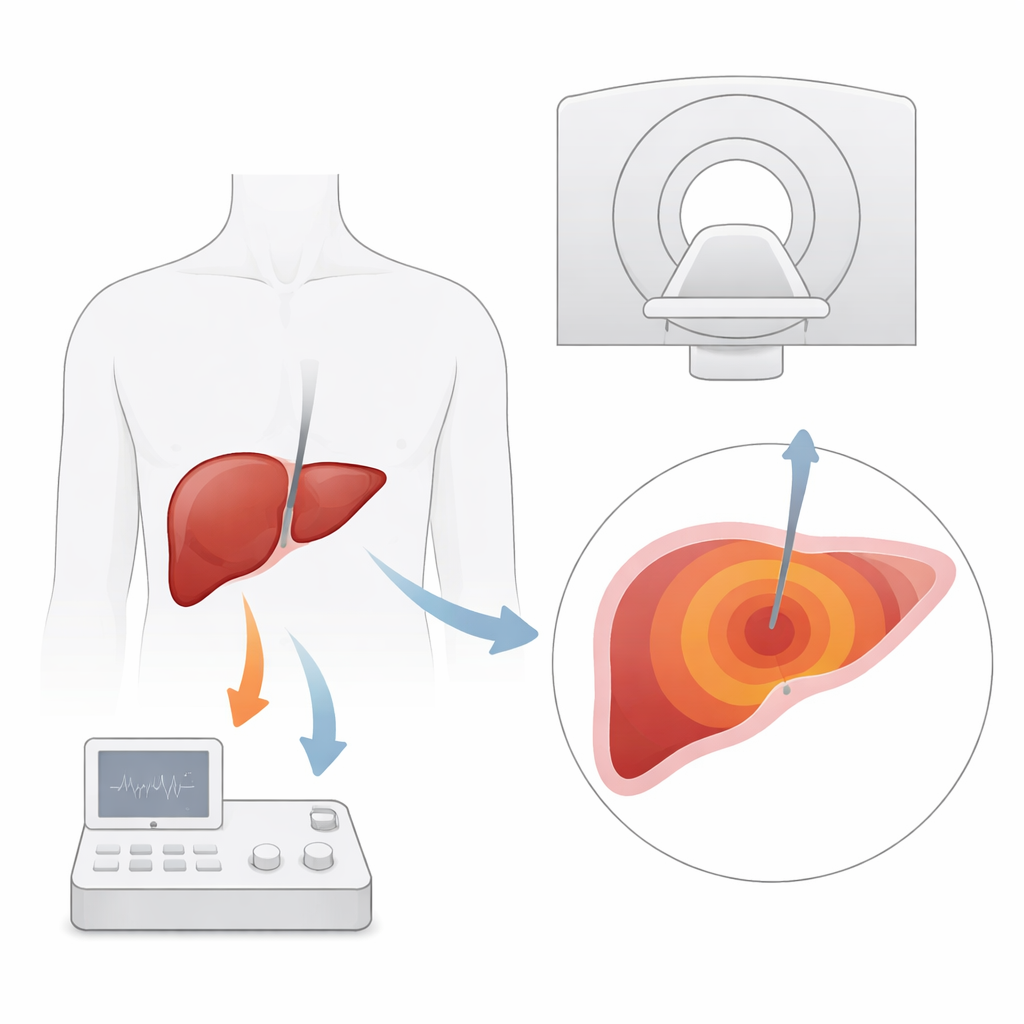
Ablacja mikrofalowa wykorzystuje cienką igłę do dostarczenia energii, która „gotuje” i niszczy tkankę guza wewnątrz wątroby. Ma to szczególne znaczenie u pacjentów z rakiem wątroby lub przerzutami, którzy nie mogą przejść operacji. Tradycyjne narzędzia obrazowe, takie jak ultrasonografia czy tomografia komputerowa, pomagają w lokalizacji igły, ale mają trudności z uwidocznieniem małych guzów lub śledzeniem zasięgu ciepła w trakcie zabiegu. MRI wyróżnia się, ponieważ potrafi nie tylko pokazać tkanki miękkie z dużą szczegółowością, lecz także zmierzyć zmiany temperatury dzięki właściwościom cząsteczek wody. W teorii pozwala to lekarzom obserwować mapę cieplną wątroby w czasie rzeczywistym i upewnić się, że cały guz wraz z bezpiecznym marginesem został zniszczony.
Kiedy zbyt wysokie temperatury zaburzają obraz
W praktyce mapy temperatury MRI mogą stać się niewiarygodne, gdy tkanka osiąga bardzo wysoką temperaturę. Przy wysokich temperaturach woda w tkance wrze, tworząc maleńkie kieszonki gazu, które zaburzają pole magnetyczne. Te zniekształcenia objawiają się jako fałszywe odczyty temperatury i dziwne kształty na mapie, utrudniając określenie rzeczywistego zasięgu ablacji. Badacze przypuszczali, że nieco niższe temperatury docelowe mogą dawać czystsze, bardziej wiarygodne mapy MRI, nawet jeśli oznaczałoby to mniejsze obszary leczenia. Ich celem było znalezienie kombinacji temperatury docelowej i czasu nagrzewania, które najlepiej równoważą czytelność obrazu z wystarczającym zniszczeniem tkanki.
Testowanie ustawień cieplnych na wątrbinach zwierzęcych dawcy
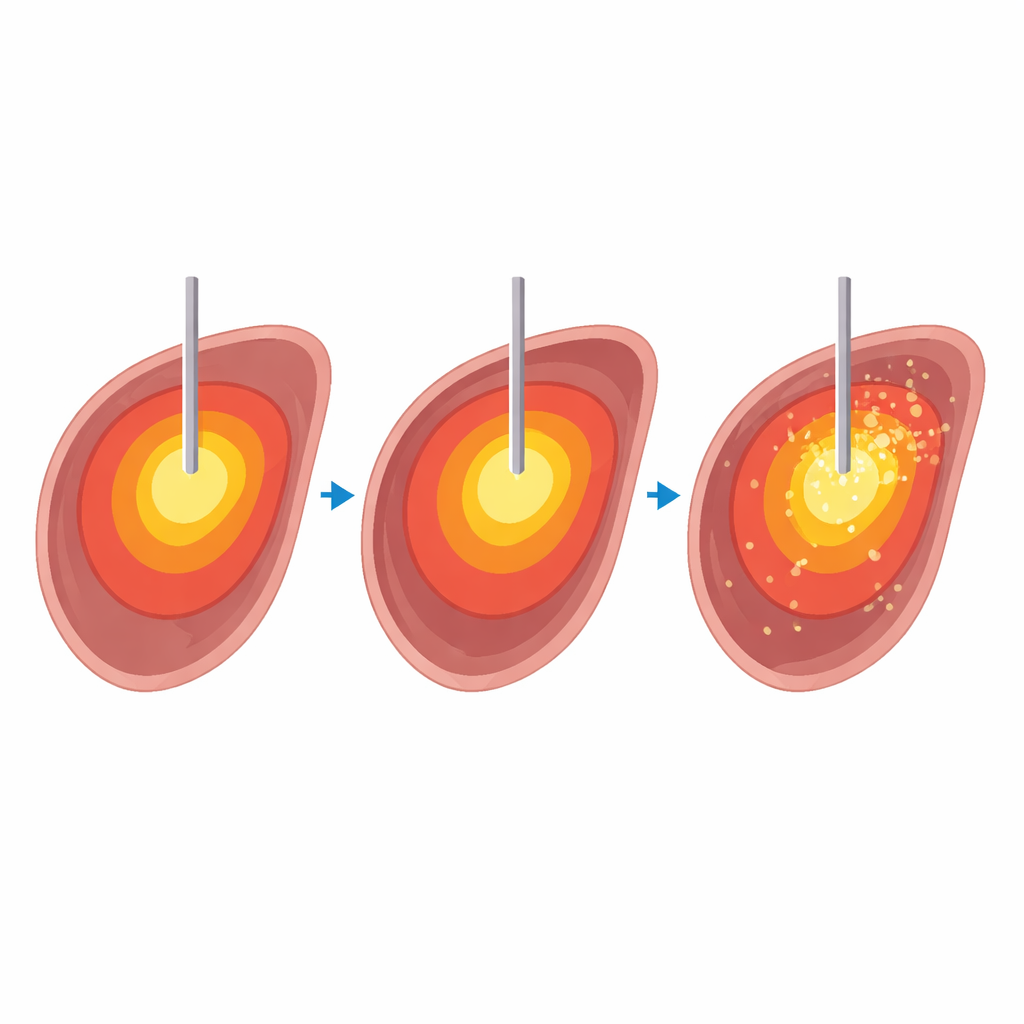
Aby zbadać to w sposób bezpieczny i precyzyjny, zespół przeprowadził 32 ablacje mikrofalowe w dziesięciu wątrbowych preparatach bydlęcych pobranych krótko po uboju. W skanerze MRI o natężeniu 1,5 tesli podgrzewano tkankę wątroby do czterech temperatur docelowych — 60, 80, 100 i 120 stopni Celsjusza — przez cztery różne okresy czasu od 5 do 15 minut. Podczas każdej ablacji szybka sekwencja MRI generowała trójwymiarowe mapy temperatury i „dawki termicznej” co kilka sekund. Po nagrzewaniu wątroby przecięto wzdłuż toru igły, a widoczne obszary martwej tkanki zmierzono i porównano z obszarami przewidzianymi przez mapy MRI. Dwóch radiologów oceniło jakość map MRI w skali pięciopunktowej, uwzględniając, na ile strefa ogrzewana była okrągła i regularna oraz jak bardzo artefakty związane z gazem i igłą przeszkadzały w odczycie.
Chłodniejsze oparzenia, czyściejsze mapy
Doświadczenia wykazały wyraźny kompromis. Wyższe temperatury powodowały większe obszary martwej tkanki, co było zgodne z oczekiwaniami, lecz mapy temperatury MRI pogarszały się znacząco powyżej 100 stopni. Przy tych wyższych ustawieniach kształty stref ablacji stawały się bardziej nieregularne, a zniekształcenia związane z gazem powodowały pozorne spadki, a nawet ujemne wartości temperatury w pobliżu igły. Natomiast przy 60 i 80 stopniach mapy MRI były gładsze, bardziej okrągłe i znacznie lepiej zgadzały się z rzeczywistymi rozmiarami zmian widocznych na przekrojach tkanki. Analizy statystyczne potwierdziły silną zgodność między obszarami wyznaczonymi przez MRI a rzeczywistą martwicą przy niższych temperaturach, przy czym korelacje osłabiały się lub znikały przy wyższych temperaturach. Wydłużenie czasu ogrzewania częściowo rekompensowało niższą temperaturę pod względem całkowitego uszkodzenia, ale nie mogło w pełni dorównać największym zmianom obserwowanym przy 120 stopniach.
Strategia dwuetapowa dla bezpieczniejszej, mądrzejszej ablacji
Na podstawie tych ustaleń autorzy proponują praktyczny kompromis dla przyszłych zabiegów prowadzonych z użyciem MRI. Pierwsza faza ogrzewania w okolicach 80 stopni Celsjusza przez 15 minut zapewniała dobre wyważenie: jakość obrazu była wysoka, strefa ablacji — rozsądnie duża, a badania tkankowe wykazały skuteczne obumieranie komórek. W przypadkach wymagających jeszcze większych stref leczenia sugerują podejście dwuetapowe: rozpocząć od fazy o niższej temperaturze, aby uzyskać czystą mapę termiczną i zweryfikować pokrycie, a następnie, gdy ustawienie i marginesy będą satysfakcjonujące, zwiększyć temperaturę w drugiej fazie w celu poszerzenia obszaru zniszczenia, akceptując, że mapa temperatury będzie mniej wiarygodna podczas tego końcowego doładowania.
Co to oznacza dla przyszłej opieki nad pacjentem
Dla laika kluczowy wniosek jest taki, że „trochę obniżyć temperaturę” może tak naprawdę uczynić zabiegi termiczne przeciwnowotworowe bezpieczniejszymi i bardziej precyzyjnymi — przynajmniej w kontrolowanych warunkach laboratoryjnych. Niższe temperatury docelowe dały znacznie czytelniejsze mapy temperatury MRI, co ułatwiało rozpoznanie, gdzie tkanka rzeczywiście została zniszczona. Minusem jest to, że chłodniejsze oparzenia tworzą mniejsze zmiany, więc lekarze mogą potrzebować dłuższych lub wieloetapowych zabiegów, by pokryć duże guzy. Ponieważ badania przeprowadzono na nieżywych wątrobach zwierzęcych bez przepływu krwi i ruchu oddechowego, konieczne są dalsze prace u pacjentów. Mimo to badanie wskazuje na protokoły leczenia, które wykorzystują MRI nie tylko do skierowania igły, lecz także do obserwacji i precyzyjnego dostrajania ogrzewania w czasie rzeczywistym, co może poprawić wyniki u osób z guzami wątroby.
Cytowanie: Nardone, L., Tan, A.S.M., Bour, P. et al. Quantitative ex vivo assessment of target temperature and ablation duration for protocol optimization of microwave ablation procedures with mr thermometry. Sci Rep 16, 8153 (2026). https://doi.org/10.1038/s41598-026-41656-3
Słowa kluczowe: ablacja mikrofalowa, termometria MRI, rak wątroby, ablacja termiczna, terapia prowadzona obrazowo