Clear Sky Science · pl
Synteza i charakteryzacja nanocząstek CuFe2O4 domieszkowanych Mg pod kątem potencjalnych zastosowań przeciwnowotworowych
Dlaczego maleńkie magnesy mogą mieć znaczenie w onkologii
Chemioterapia i radioterapia mogą uszkadzać tkanki zdrowe obok nowotworów. Naukowcy poszukują bardziej inteligentnych terapii, które uderzają silniej w komórki nowotworowe niż w normalne. W tym badaniu analizowano ultramiękkie magnetyczne cząstki z żelaza, miedzi i magnezu, zaprojektowane tak, by trafiać do komórek nowotworowych i uruchamiać ich wewnętrzne programy samobójcze. Wyniki sugerują, że staranne dobranie składu i rozmiaru tych cząstek może uczynić je szczególnie zabójczymi dla komórek guzowych przy jednoczesnym oszczędzaniu komórek zdrowych.
Tworzenie inteligentnych cząstek metalicznych
Naukowcy wytworzyli rodzinę „nanoferrytów” – maleńkich kryształów zawierających żelazo – przez połączenie miedzi i magnezu w różnych proporcjach z żelazem i tlenem. Cząstki te, o rozmiarach około 17–30 miliardowych części metra, są na tyle małe, że mogą wnikać do wnętrza komórek. Zespół zastosował kilka zaawansowanych mikroskopów i technik rentgenowskich, aby potwierdzić prawidłową strukturę krystaliczną, czystość chemiczną i tendencję do tworzenia w przybliżeniu kulistych agregatów. Stwierdzono, że mieszana wersja z równymi ilościami miedzi i magnezu dała najmniejsze cząstki, co zwiększa powierzchnię i zwykle podnosi ich reaktywność chemiczną.
Testowanie cząstek na komórkach nowotworowych
Zespół następnie sprawdził toksyczność poszczególnych rodzajów cząstek na hodowlach ludzkich komórek nowotworowych, w tym raka prostaty (PC‑3), jelita grubego (Caco‑2), piersi (MCF‑7) i wątroby (HepG‑2), porównując je z normalnymi komórkami jelitowymi jako kontrolą bezpieczeństwa. Wszystkie trzy formuły uszkadzały komórki nowotworowe w sposób zależny od dawki, lecz nie w równej mierze. Mieszane cząstki miedź‑magnez okazały się ogólnie najsilniejsze, zwłaszcza wobec komórek raka prostaty i jelita grubego, gdzie zabijały połowę komórek przy stosunkowo niskich dawkach. Co ważne, komórki normalne tolerowały wyższe dawki, co sugeruje pewien stopień selektywności istotny dla przyszłych terapii.
Wymuszanie kontrolowanej samodestrukcji komórek nowotworowych
Aby zrozumieć mechanizm działania nanocząstek, badacze przyjrzeli się apoptozie — uporządkowanej formie śmierci komórkowej, w której uszkodzone komórki rozkładają się, zamiast pękać. Za pomocą cytometrii przepływowej wykazali, że traktowane komórki raka prostaty i jelita grubego silnie przesunęły się ze stanu zdrowego do wczesnych i późnych etapów apoptozy. Ponownie, mieszane cząstki miedź‑magnez miały najsilniejszy efekt, zwiększając całkowitą apoptozę wielokrotnie w porównaniu z komórkami nietraktowanymi. Zauważono także umiarkowany wzrost martwicy, bardziej chaotycznej formy śmierci komórkowej, co sugeruje zaangażowanie kilku ścieżek uszkodzeń.
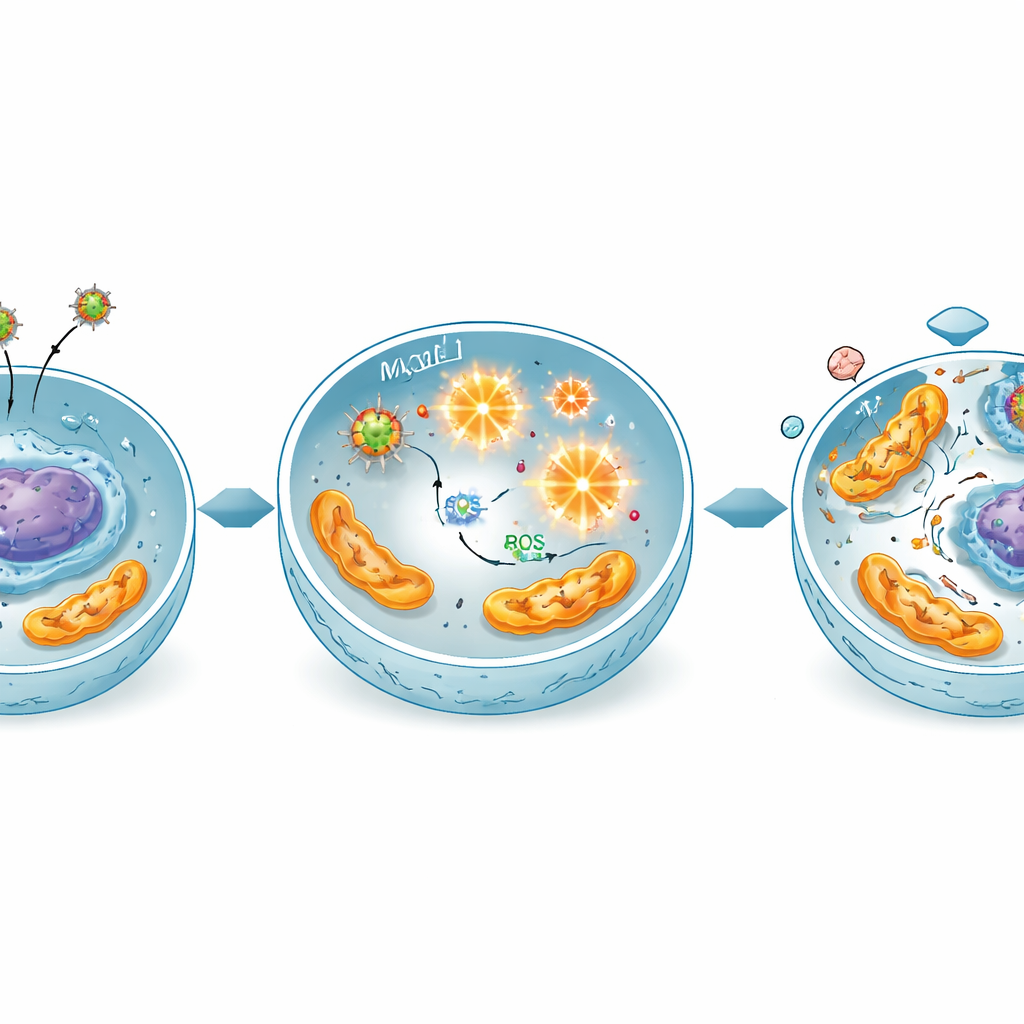
Przeciążenie komórek nowotworowych szkodliwą chemią tlenową
Badanie wskazuje na reakcję łańcuchową chemiczną jako sedno tego efektu. Te cząstki na bazie żelaza mogą działać jak mikrokatalizatory, przekształcając naturalny nadtlenek wodoru w komórkach w wysoko reaktywne formy tlenu. Pomiary wykazały, że traktowane komórki nowotworowe wytwarzały znacznie więcej tych reaktywnych form tlenu, szczególnie pod wpływem mieszaniny miedź‑magnez. Ten oksydacyjny wzrost uszkadza składniki komórkowe, w szczególności mitochondria produkujące energię i DNA. Testy ekspresji genów potwierdziły, że kluczowe geny „strażnicze” i „kat” związane z samobójstwem komórkowym zostały włączone, podczas gdy geny odpowiedzialne za przeżycie i cykl komórkowy zostały stłumione, co odpowiada obrazu stresowo‑zależnej apoptozy zależnej od mitochondriów.
Co to może znaczyć dla przyszłej opieki onkologicznej
Podsumowując, praca pokazuje, że przez staranny wybór metali oraz dostrojenie rozmiaru i struktury nanoferrytów można stworzyć cząstki, które silnie skłaniają komórki nowotworowe do samodestrukcji, będąc jednocześnie łagodniejszymi dla komórek normalnych. Wersja o równych proporcjach miedzi i magnezu wyróżniała się jako najbardziej skuteczna, najpewniej dlatego, że jej niewielki rozmiar i mieszana chemia metali zwiększają zdolność wejścia do komórek i generowania reaktywnych form tlenu. Chociaż wyniki dotyczą jedynie hodowli komórkowych i są dalekie od zastosowań klinicznych, wskazują obiecującą ścieżkę ku bardziej precyzyjnym, opartym na nanotechnologii terapiom przeciwnowotworowym, które polegałyby na uruchamianiu wewnętrznych mechanizmów zabijania guza, zamiast zatruwania organizmu nieselektywnymi lekami.
Cytowanie: Ali, M., Zein, N., Abdo, M.A. et al. Synthesis, characterization of Mg doped CuFe2O4 nanoparticles for potential anticancer applications. Sci Rep 16, 8276 (2026). https://doi.org/10.1038/s41598-026-41540-0
Słowa kluczowe: nanocząstki, terapia przeciwnowotworowa, reaktywne formy tlenu, apoptoza, ferryt