Clear Sky Science · pl
Fenotypy krążących komórek układu odpornościowego powiązane z biomarkerami zapalnymi u uczestników bez demencji z kohorty potomków Framingham Heart Study
Dlaczego twój układ odpornościowy ma znaczenie dla zdrowia mózgu
W miarę starzenia się często utrzymuje się u nas niski, przewlekły poziom zapalenia, który może po cichu zwiększać ryzyko chorób serca, cukrzycy i problemów z pamięcią. Naukowcy wiedzą, że komórki odpornościowe we krwi napędzają te sygnały zapalne, ale większość badań obejmowała tylko kilka typów komórek lub garść markerów krwi jednocześnie. W tej pracy wykorzystano szczegółowe pomiary krwi u setek dorosłych pozbawionych demencji uczestników długoletniego badania Framingham Heart Study, aby zobrazować, jak różne rodzaje komórek odpornościowych wiążą się z dziesiątkami białek związanych z zapaleniem. Praca pomaga ujawnić, jak wygląda „zaspalony” układ odpornościowy u przeciętnych ludzi i jak może się to wiązać ze starzeniem oraz przyszłym zdrowiem mózgu. 
Dogłębne spojrzenie na krew i układ odpornościowy
Naukowcy oparli się na danych od 873 mężczyzn i kobiet ze średnią wieku 61 lat, którzy byli częścią kohorty potomków Framingham i nie mieli demencji. Przeanalizowali zamrożone komórki krwi i osocze pobrane około roku 2000. Przy użyciu metody laboratoryjnej zwanej cytometrią przepływową rozdzielili komórki odpornościowe krwi na 77 specyficznych typów, w tym wiele odmian komórek T, B i monocytów pełniących różne role w obronie i naprawie. Równolegle zmierzyli 68 białek związanych z zapaleniem, takich jak cząsteczki sygnałowe i czynniki wzrostu, przy użyciu panelu wysokoprzepustowego. Dało to szczegółowy obraz zarówno „strony komórkowej”, jak i „strony białkowej” układu odpornościowego u tych samych osób.
Łączenie typów komórek z sygnałami zapalnymi
Dysponując tym bogatym zbiorem danych, zespół badał, jak każdy typ komórki odpornościowej wiązał się z każdym białkiem, uwzględniając przy tym czynniki takie jak wiek, płeć i zakażenie cytomegalowirusem, powszechnym wirusem trwającym przez całe życie, który przekształca układ odpornościowy. Użyto także modeli statystycznych biorących pod uwagę relacje rodzinne w kohorcie i skorygowano wyniki pod kątem dużej liczby porównań. Jednym z najczytelniejszych wzorców była grupa komórek zwana CD8 naïve T — „świeże” komórki cytotoksyczne T, które nie były jeszcze mocno zaangażowane w walkę z infekcjami. Osoby z mniejszą liczbą tych naiwnych komórek miały tendencję do wyższych poziomów wielu białek zapalnych, w tym kilku chemokin i klasycznych mediatorów zapalenia. Innymi słowy, profil krwi pokazujący mniej naiwnych komórek CD8 szedł w parze z bardziej aktywnym środowiskiem zapalnym.
Sygnały aktywacji odporności i starzenia
Kolejne kluczowe odkrycie dotyczyło białka zwanego rozpuszczalnym łańcuchem alfa CD8, które odzwierciedla aktywność komórek CD8 dodatnich. Wyższe poziomy tego białka wiązały się z większą liczbą cytotoksycznych i efektorowych komórek CD8 oraz z podzbiorem komórek T produkujących interferon‑gamma, co wskazuje na układ odpornościowy przesunięty w stronę doświadczonych, „bohaterskich” komórek. Jednocześnie osoby z większą liczbą B‑komórek o cechach naiwnych miały zwykle niższe poziomy tego białka związanego z CD8, sugerując kompromis między utrzymaniem rezerw młodych komórek a posiadaniem bardziej gotowej odpowiedzi. Badacze zaobserwowali także istotne powiązania między pewnymi podtypami komórek B i monocytów a białkami zaangażowanymi w migrację komórek, naprawę tkanek i uszkodzenia zapalne. Wzorce tych skojarzeń były szczególnie silne u uczestników powyżej 60. roku życia i u mężczyzn, a wiele z nich utrzymywało się nawet po uwzględnieniu chorób serca, funkcji nerek i tradycyjnych czynników ryzyka sercowo‑naczyniowego. 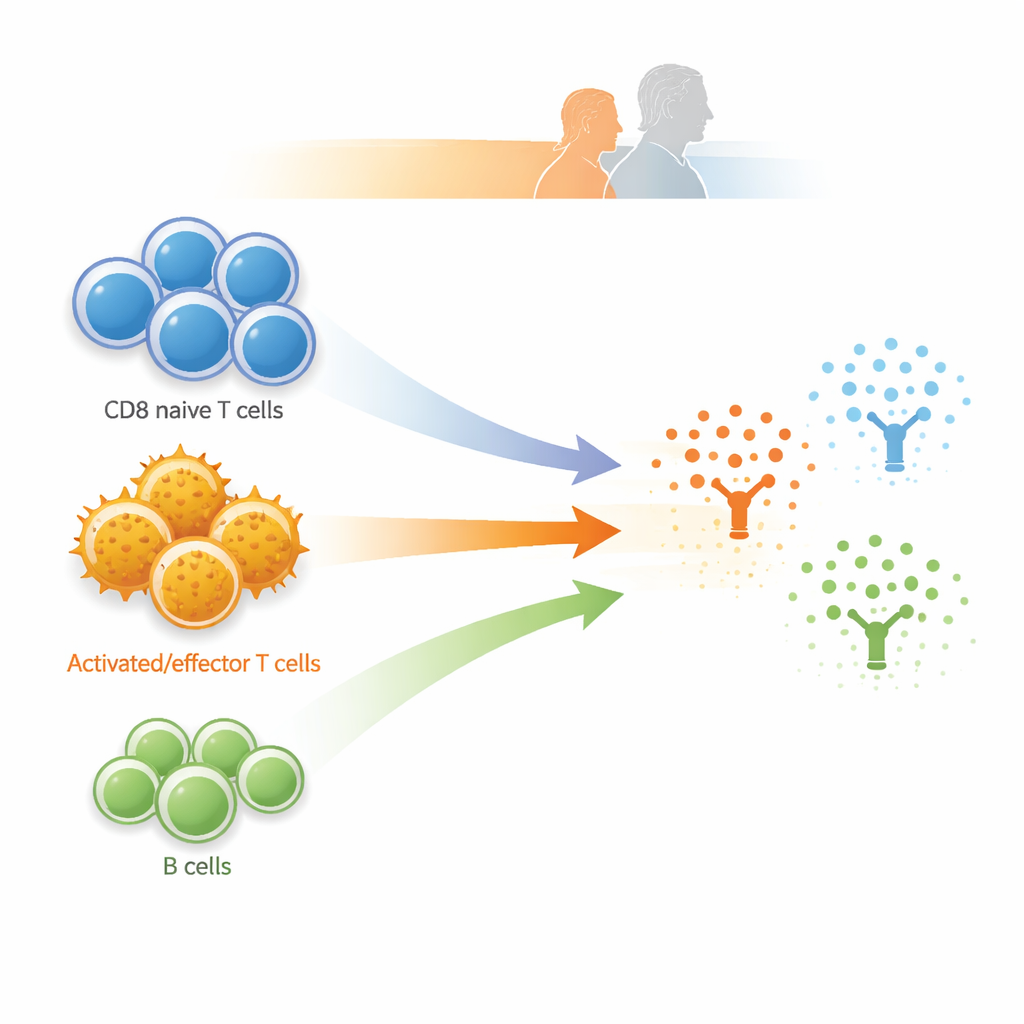
Postrzeganie sieci odpornościowej jako całości
Aby wyjść poza porównania „po jednym”, zespół zbudował mapę sieci, która uwydatniła, które komórki i białka miały tendencję do poruszania się razem. W tej sieci białko związane z CD8 zajmowało centralne miejsce w węźle cech związanych z komórkami T, podczas gdy naiwny CD8 łączył się silnie z kilkoma chemokinami zapalnymi, a konkretne grupy komórek B były powiązane z białkami pomagającymi w ich migracji lub dojrzewaniu. To zintegrowane spojrzenie pokazało, że wyniki parowe nie były przypadkowe: tworzyły spójne klastry zgodne z znaną biologią, taką jak stopniowe przechodzenie od komórek naiwnych do pamięci i efektorów T oraz przemieszczanie się komórek pamięci B do zapalnych tkanek. Ogólny wzorzec pasował do koncepcji „inflammaging”, w której przewlekła, niskopoziomowa aktywacja układu odpornościowego staje się bardziej powszechna z wiekiem i różni się między mężczyznami a kobietami.
Co to oznacza dla starzejących się mózgów
Choć to badanie nie może dowieść przyczynowości ani dokładnie ujawnić, co dzieje się w czasie, dostarcza jednej z najbardziej szczegółowych map na poziomie populacji tego, jak krążące komórki odpornościowe i białka zapalne odnoszą się do siebie u starszych dorosłych bez demencji. Autorzy zauważają, że kilka białek najsilniej powiązanych ze wzorcami komórek odpornościowych w tej pracy wiązało się również z funkcjami poznawczymi i ryzykiem demencji w ich wcześniejszych badaniach. Razem, te obserwacje sugerują, że przesunięcia równowagi między komórkami naiwnymi a bardziej doświadczonymi oraz towarzyszące im sygnały zapalne mogą być częścią łańcucha łączącego starzenie, choroby przewlekłe i późniejsze problemy z mózgiem. Śledzenie tych wzorców odpornościowo‑zapalnych w czasie i w bardziej zróżnicowanych populacjach może pomóc wykryć wczesne sygnały ostrzegawcze i wskazać przyszłe cele interwencji, które pomogą utrzymać zdrowie ciała i mózgu wraz z wiekiem.
Cytowanie: Chen, J., Doyle, M.F., Cao, Y. et al. Circulating immune cell phenotypes are associated with inflammatory biomarkers in dementia-free participants from the Framingham Heart Study Offspring cohort. Sci Rep 16, 11313 (2026). https://doi.org/10.1038/s41598-026-41423-4
Słowa kluczowe: starzenie się układu odpornościowego, przewlekłe zapalenie, komórki T i B, biomarkery we krwi, spadek funkcji poznawczych