Clear Sky Science · pl
Wytłumaczalne i bezpieczne uczenie federacyjne dla prywatnej klasyfikacji raka skóry z użyciem lekkiej wieloskalowej sieci CNN
Dlaczego ważne są inteligentniejsze badania pod kątem raka skóry
Rak skóry jest najczęstszym rodzajem raka na świecie, a wczesne wykrycie może uratować życie. Mimo to dokładna diagnoza wciąż w dużej mierze zależy od specjalistów, którzy uważnie oceniają zdjęcia znamion i zmian skórnych. Wiele placówek nie dysponuje taką wiedzą, a udostępnianie dużych zbiorów zdjęć pacjentów w celu trenowania lepszych narzędzi komputerowych budzi poważne obawy o prywatność. Niniejsze badanie przedstawia nowy sposób umożliwiający szpitalom współpracę przy treningu wydajnego systemu do wykrywania raka skóry bez udostępniania surowych obrazów pacjentów, a jednocześnie dostarczający lekarzom przejrzystych wizualnych wyjaśnień tego, co system „widzi”.
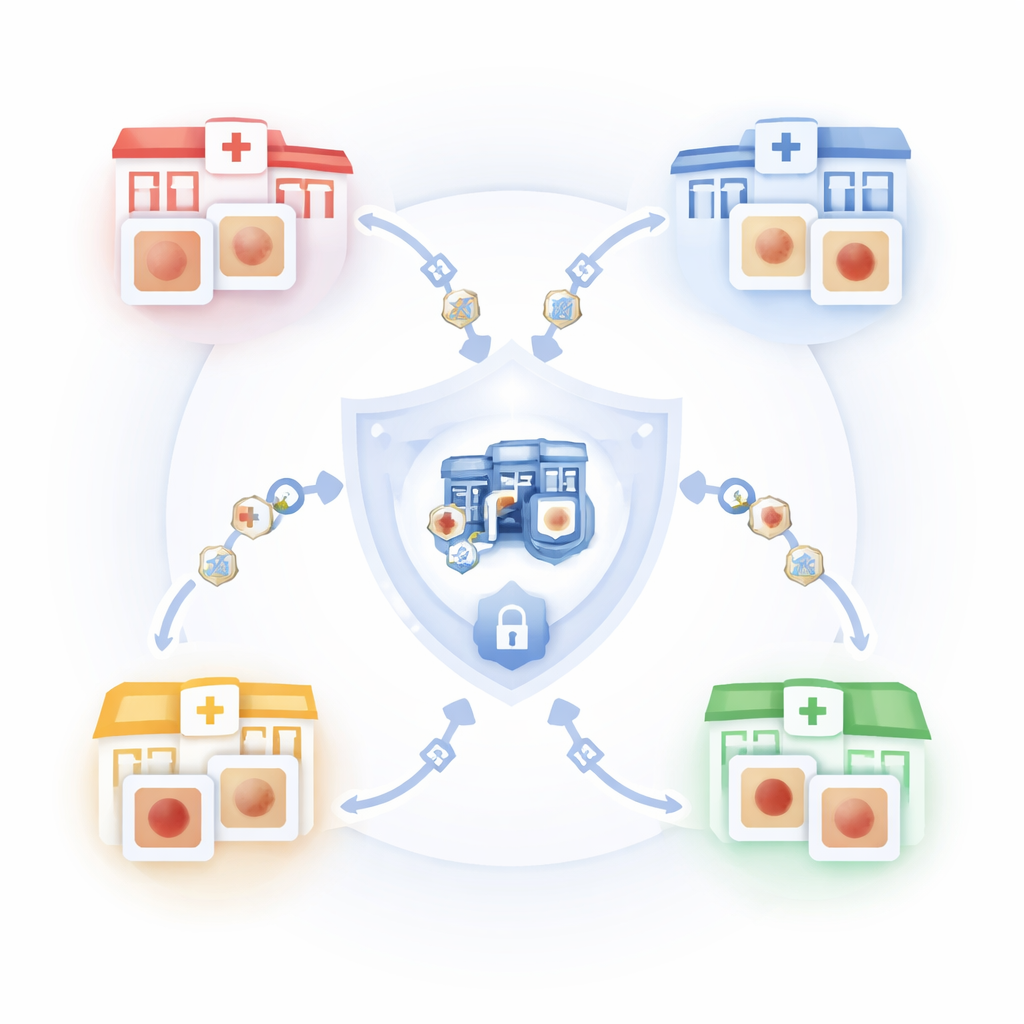
Współpraca bez ujawniania sekretów
Główną ideą jest metoda treningu zwana uczeniem federacyjnym. Zamiast wysyłać zdjęcia skóry do centralnego serwera, każdy szpital przechowuje swoje obrazy lokalnie i trenuje lokalną kopię tego samego modelu komputerowego. Tylko wyuczone „know‑how” (aktualizacje modelu) jest przesyłane do serwera centralnego, gdzie łączy się je w lepszy model globalny, a następnie rozsyła z powrotem do wszystkich placówek. W tej pracy autorzy symulują kilka współpracujących szpitali na dużym publicznym zbiorze zmian skórnych, dzięki czemu model korzysta z zróżnicowanych przypadków, podczas gdy zdjęcia pacjentów nigdy nie opuszczają ich macierzystej instytucji.
Szczupły, ale wnikliwy czytnik obrazów
Aby uczynić tę współpracę praktyczną, zespół zaprojektował nową lekką wieloskalową splotową sieć neuronową (LWMS‑CNN). Wiele popularnych modeli obrazowych jest ogromnych i wolnych do przesyłania przez sieci szpitalne; w przeciwieństwie do nich ten model wykorzystuje poniżej miliona trenowalnych parametrów, co stanowi ułamek wymagań znanych architektur. Jego struktura przetwarza każdy obraz skóry na kilku poziomach szczegółu równolegle — od drobnych krawędzi i faktur po szersze wzorce — a następnie łączy te wskazówki. Ta kompaktowa konstrukcja okazała się zarówno dokładna, jak i wydajna, przewyższając lub dorównując cięższym modelom, takim jak ResNet i DenseNet, w standardowych miarach takich jak dokładność, precyzja i F1‑score, przy jednoczesnym znacznie mniejszym rozmiarze i szybszym działaniu — co ma znaczenie przy użyciu na skromniejszych serwerach szpitalnych lub nawet urządzeniach brzegowych.
Zabezpieczanie prywatności za pomocą szyfrowania
Chociaż uczenie federacyjne unika przesyłania surowych obrazów, udostępniane aktualizacje modelu nadal mogą wyciekać informacji przy zaawansowanych atakach. Aby zamknąć tę lukę, autorzy objęli całą wymianę szyfrowaniem homomorficznym, techniką kryptograficzną, która pozwala serwerowi dodawać i uśredniać aktualizacje modelu, pozostając przy tym zaszyfrowanym. Szpitale szyfrują swoje zmiany modelu przed wysłaniem; serwer widzi jedynie zaszyfrowane liczby, a mimo to może obliczyć skombinowaną aktualizację. Tylko zaufany podmiot może odszyfrować zebrany wynik. Testy wykazały, że dodanie tej ochrony niemal nie wpłynęło na wydajność: dokładność spadła jedynie o około 0,3 punktu procentowego (z 98,62% do 98,34%), niewielka cena za znacząco zwiększoną prywatność i zgodność z surowymi regulacjami dotyczącymi danych medycznych.
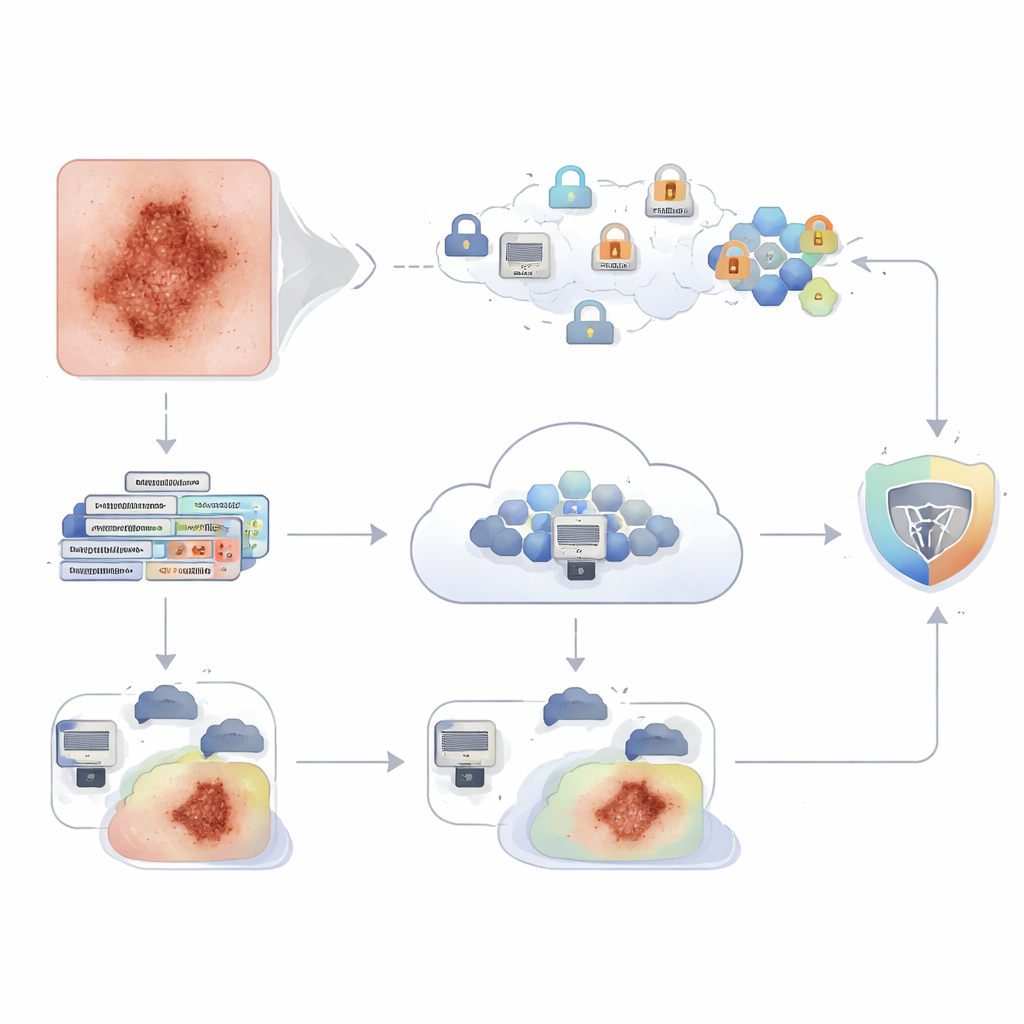
Otwarcie czarnej skrzynki dla klinicystów
Sama wysoka dokładność nie wystarcza w medycynie; klinicyści muszą rozumieć, dlaczego algorytm podjął daną decyzję. W związku z tym badanie dodaje narzędzia wytłumaczalnej AI na szczycie wytrenowanego modelu. Jedno z narzędzi, SHAP, podkreśla, które części obrazu najbardziej wpłynęły na decyzję, traktując każdy fragment piksela jako „gracza” w grze głosowania. Inne, Grad‑CAM, nakłada mapę cieplną na zmianę, pokazując, gdzie sieć skupiła uwagę, gdy na przykład oceniła zmianę jako złośliwą lub łagodną. Razem te widoki pozwalają dermatologom sprawdzić, czy model patrzy na sensowne struktury — takie jak nieregularne brzegi czy zróżnicowanie koloru — zamiast na włosy, artefakty oświetleniowe czy tło skóry, oraz dokładnie przeanalizować przypadki niepewne lub błędne.
Od testów laboratoryjnych do realnych klinik
Szyfrowany federacyjny system LWMS‑CNN był trenowany i oceniany na zbiorze zmian skórnych HAM10000, a następnie testowany na dwóch dodatkowych kolekcjach, ISIC 2019 i PAD‑UFES‑20, które różnią się aparatami, typami zmian i populacjami pacjentów. Osiągnął wysokie dokładności we wszystkich trzech, co sugeruje, że podejście dobrze uogólnia się poza pojedyncze źródło danych. Autorzy zbadali również trudniejsze, bardziej realistyczne ustawienia, w których różne „szpitale” obserwują różne mieszanki przypadków, oraz porównali kilka sposobów łączenia aktualizacji modelu; standardowa metoda FedAvg sprawdziła się najlepiej. Chociaż eksperymenty przeprowadzono w symulowanym środowisku wieloklienckim, a nie na fizycznie odseparowanych szpitalach, wyniki pokazują, że kompaktowy model, prywatne szkolenie i przejrzyste wizualne wyjaśnienia można połączyć w jedną ramę. Dla pacjentów oznacza to perspektywę przyszłych badań pod kątem raka skóry, które będą bardziej dokładne, szerzej dostępne i bardziej poszanowujące prywatność, przy jednoczesnym zachowaniu lekarzy w roli decyzyjnej.
Cytowanie: Sayeed, A.S.M., Birahim, S.A., Ullah, M.S. et al. Explainable and secure federated learning for privacy-enhancing skin cancer classification using a lightweight multi-scale CNN. Sci Rep 16, 11414 (2026). https://doi.org/10.1038/s41598-026-41360-2
Słowa kluczowe: wykrywanie raka skóry, uczenie federacyjne, prywatność danych medycznych, wytłumaczalna sztuczna inteligencja, szyfrowanie homomorficzne