Clear Sky Science · pl
Ocena metagenomiki długich odczytów do diagnostyki zakażeń krwi: badanie pilotażowe z tajskiego szpitala trzeciego stopnia
Dlaczego szybsze testy na zakażenia krwi mają znaczenie
Gdy bakterie przedostają się do krwi, każda godzina ma znaczenie. Lekarze muszą szybko wybrać właściwy antybiotyk, podczas gdy dzisiejsze badania laboratoryjne mogą zajmować kilka dni, zanim zidentyfikują sprawcę i określą, które leki prawdopodobnie nie zadziałają. To badanie z dużego tajskiego szpitala bada nowy sposób przyspieszenia procesu poprzez jednoczesne odczytywanie materiału genetycznego wszystkich mikrobów w próbce krwi za pomocą przenośnego sekwencjonera DNA. Celem jest skrócenie oczekiwania z dni do szczegółowego obrazu zakażenia w czasie jednej zmiany roboczej.
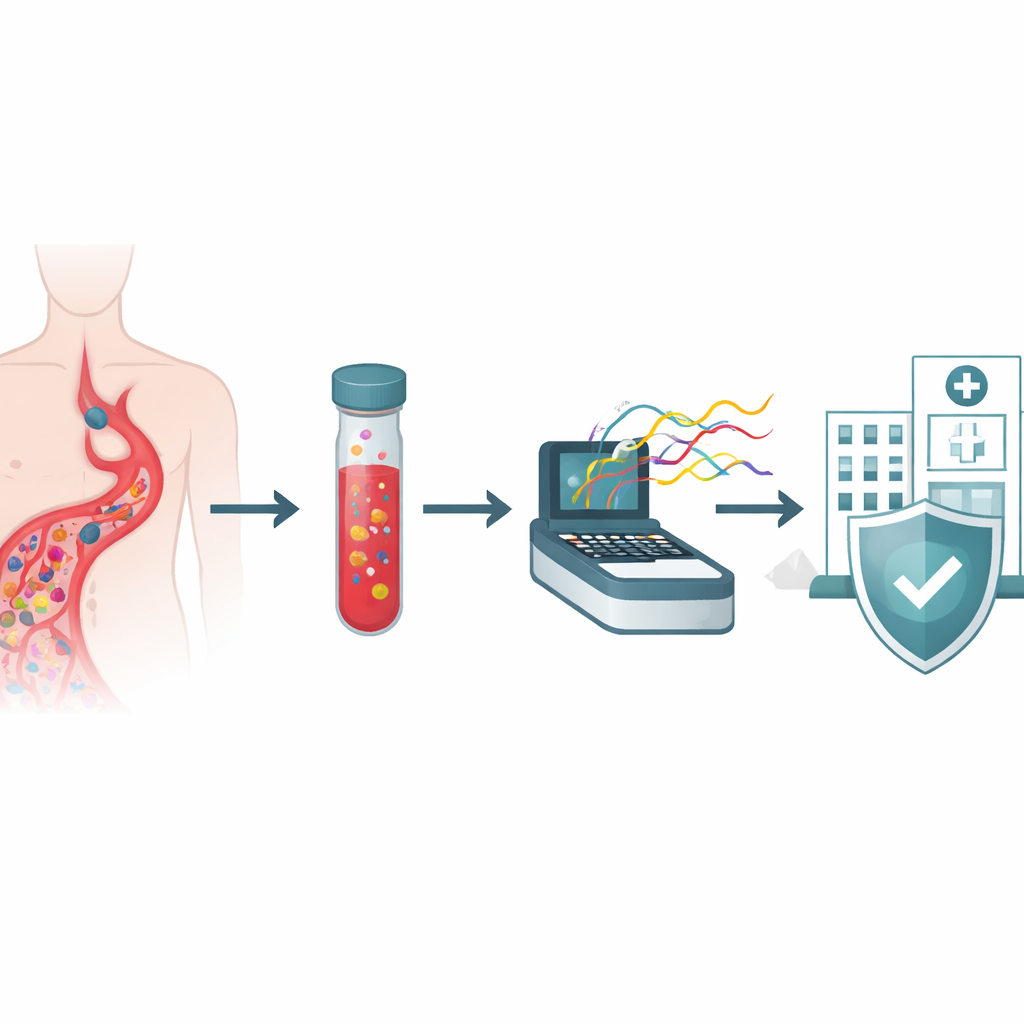
Nowy sposób „czytania” drobnoustrojów we krwi
Naukowcy skupili się na pacjentach, u których standardowe butelki do hodowli krwi wskazały już na wzrost bakterii — są one rutynowo używane w szpitalach na całym świecie. Zamiast namnażać każdą bakterię na oddzielnych płytkach i wykonywać serię testów chemicznych, pobrali płyn bezpośrednio z 40 dodatnich butelek hodowlanych i wyizolowali całą DNA drobnoustrojów. Ten materiał genetyczny poddano sekwencjonowaniu na urządzeniu Oxford Nanopore, które przeciąga długie nici DNA przez maleńkie pory i odczytuje ich sekwencję w czasie rzeczywistym. Ponieważ metoda nie polega na oddzielnym namnażaniu organizmów, w zasadzie może wykrywać wiele gatunków, ich cechy oporności na leki i czynniki wirulencji w jednym uproszczonym procesie.
Co wykryto w zakażeniach krwi w Tajlandii
Konwencjonalne badania tych samych 40 próbek dały 45 izolatów bakteryjnych, co odzwierciedla, że u kilku pacjentów występowało zakażenie więcej niż jednym gatunkiem. Standardowy szpitalny system VITEK wykazał, że dwa znane bakterie jelitowe, Escherichia coli i Klebsiella pneumoniae, odpowiadały za prawie 40% tych zakażeń, a wiele tych szczepów było opornych na wiele leków. Podejście nanopore w dużym stopniu potwierdziło ten obraz, identyfikując 43 odrębne genomy bakteryjne i potwierdzając dominację członków grupy Enterobacterales. Wykryło też kilka rzadkich lub błędnie sklasyfikowanych gatunków, takich jak środowiskowa bakteria Ralstonia mannitolilytica czy Campylobacter jejuni — bakteria żołądkowo‑jelitowa — których metody rutynowe pominęły lub określiły tylko ogólnie. W niektórych mieszanych zakażeniach sekwencjonowanie miało jednak trudności z pełnym rozdzieleniem blisko spokrewnionych drobnoustrojów, gdy jeden był obecny na znacznie niższym poziomie niż drugi.
Wgląd w mechanizmy oporności i taktyki ukrywania się
Dzięki odczytom długich fragmentów DNA nowa metoda potrafi zrobić więcej niż tylko nazwać bakterie: może ujawnić genetyczne mechanizmy, które pomagają im opierać się antybiotykom i wywoływać chorobę. Zespół przeszukał genomy pod kątem znanych genów oporności oraz genów „wirulencji”, które pomagają drobnoustrojom przyczepiać się do tkanek, tworzyć ochronne biofilmy, pozyskiwać żelazo czy wytwarzać toksyny. E. coli i K. pneumoniae nosiły wiele takich genów, w tym te unieszkodliwiające kluczowe grupy antybiotyków, takie jak beta‑laktamy i aminoglikozydy. Sekwencjonowanie uwypukliło też silne pakiety oporności w gatunkach uodpornionych na warunki szpitalne, takich jak Acinetobacter baumannii i Pseudomonas aeruginosa, których genomy były bogate w systemy pompujące leki i inne mechanizmy obronne. Jednocześnie niektóre rzadsze bakterie krwi miały stosunkowo skromniejsze arsenały, sugerując niższe, ale wciąż istotne zagrożenie. 
Śledzenie oporności na ruchomym DNA
Kolejną zaletą sekwencjonowania długich odczytów jest możliwość złożenia całych chromosomów bakteryjnych wraz z kolistymi cząstkami DNA zwanymi plazmidami, które mogą przeskakiwać między bakteriami i rozprzestrzeniać geny oporności. W tym badaniu badacze skatalogowali dziesiątki typów plazmidów. Niektóre były silnie powiązane z określonymi gatunkami, inne występowały w kilku rodzajach bakterii, co sugeruje trwającą wymianę genów w środowisku szpitalnym. Wiele niosło znane czynniki prowadzące do nieskuteczności leczenia, takie jak beta‑laktamazy o rozszerzonym spektrum działania i karbapenemazy — enzymy osłabiające działanie jednych z najważniejszych antybiotyków. Mapowanie tych elementów mobilnych pomaga zespołom kontroli zakażeń zrozumieć, jak niebezpieczne cechy przemieszczają się po szpitalu w czasie.
Przyspieszanie odpowiedzi dla lekarzy i szpitali
Czas to obszar, w którym nowe podejście pokazuje naj wyraźniejszą przewagę. Standardowe ścieżki często zajmują pięć do siedmiu dni od momentu, gdy hodowla krwi staje się dodatnia, do chwili uzyskania pełnej identyfikacji i wyników wrażliwości na leki. W przeciwieństwie do tego, konfiguracja nanopore w tym badaniu pilotażowym dawała wczesne identyfikacje gatunków w ciągu dwóch do czterech godzin od rozpoczęcia sekwencjonowania i wskazywała kluczowe geny oporności w ciągu sześciu do ośmiu godzin. Dłuższe przebiegi sekwencjonowania poprawiały kompletność genomów, ale nie zmieniały głównych wniosków klinicznych. Choć było to małe, wstępne badanie, które jeszcze nie powiązało wyników z losami pacjentów ani nie oceniło kosztów, sugeruje, że integracja metagenomicznego sekwencjonowania długich odczytów w laboratoriach szpitalnych mogłaby dostarczać szybsze, bogatsze informacje do prowadzenia terapii, wspierać racjonalne stosowanie antybiotyków i wzmacniać regionalne monitorowanie zakażeń odpornych na leki.
Co to znaczy dla opieki nad pacjentem
Dla laika wniosek jest taki, że lekarze wkrótce mogą otrzymać genetyczne „snapshot” zakażenia krwi tego samego dnia, w którym hodowla staje się dodatnia, zamiast czekać prawie tydzień. Ten obraz nie tylko identyfikuje drobnoustrój, lecz także uwypukla wiele jego słabych punktów i potencjał do przenoszenia oporności na inne bakterie. Mimo że potrzeba większych badań na większych grupach pacjentów, lepszej kontroli skażeń i analiz kosztów, tajski pilotaż pokazuje, że kieszonkowe sekwencjonery DNA mogą przybliżać nas do szybkiej, opartej na genomie opieki w przypadku zagrażających życiu zakażeń krwi.
Cytowanie: Yaikhan, T., Wongsurawat, T., Jenjaroenpan, P. et al. Evaluating long-read metagenomics for bloodstream infection diagnostics: a pilot study from a Thai Tertiary Hospital. Sci Rep 16, 9330 (2026). https://doi.org/10.1038/s41598-026-41247-2
Słowa kluczowe: zakażenie krwi, oporność na leki przeciwbakteryjne, sekwencjonowanie metagenomiczne, technologia nanopore, mikrobiologia kliniczna