Clear Sky Science · pl
Mediator podłoża Cullin 3 (MtCSP1) moduluje nodulację przez interakcję z GTPazą ARFA1
Jak fasola wytwarza własny nawóz
Współczesne rolnictwo w dużym stopniu polega na nawozach azotowych, które zwiększają plony, ale mają koszty dla środowiska. Rośliny strączkowe, takie jak koniczyna, groch czy lucerna, oferują naturalną alternatywę: goszczą pożyteczne bakterie glebowe w specjalnych strukturach korzeniowych zwanych guzami, gdzie azot z powietrza jest przekształcany w pożywienie dla roślin. Badanie to ujawnia, jak wcześniej nieopisane białko roślinne, MtCSP1, pomaga kontrolować formowanie tych guzków przez precyzyjne regulowanie wewnątrzkomórkowego ruchu i recyklingu kluczowych molekularnych przełączników w komórkach korzeni.
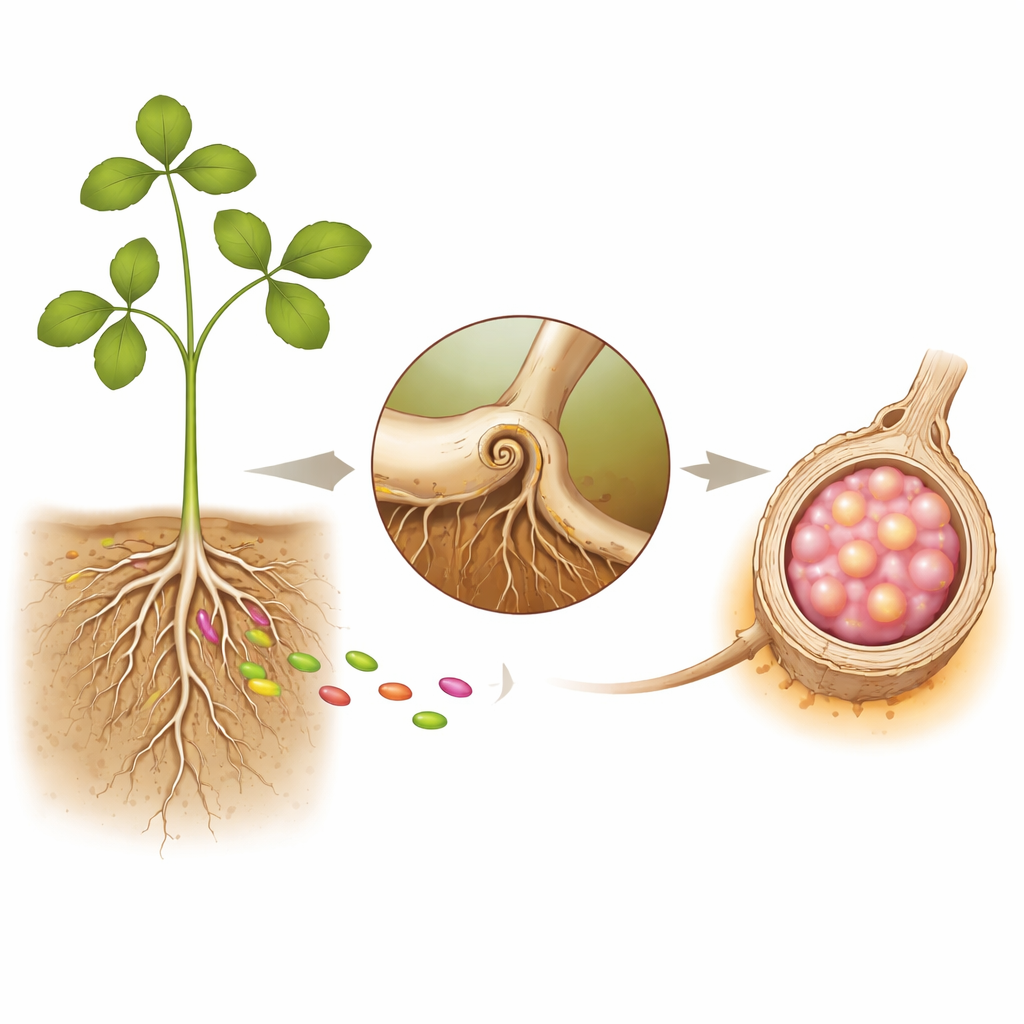
Korzenie roślin i ich bakteryjni lokatorzy
Rośliny strączkowe współpracują z rhizobiami, bakteriami glebowymi zdolnymi zamieniać azot atmosferyczny w formy użyteczne, takie jak amoniak. Aby bezpiecznie pomieścić te bakterie, korzenie tworzą guzki — małe „fabryki” na powierzchni korzenia. Proces zaczyna się, gdy bakterie przyczepiają się do włosków korzeniowych, które zwijają się i tworzą wąski tunel zwany nicią infekcyjną. Przez ten tunel bakterie przemieszczają się do głębszych tkanek korzenia, gdzie zaczyna rosnąć nowy organ — guzek. W dojrzałym guzku bakterie zostają otoczone błonami wytworzonymi przez roślinę i przekształcają się w wyspecjalizowane „bakteroidy”, które wiążą azot dla rośliny w zamian za cukry i energię.
Komórkowi strażnicy ruchu wewnątrz komórek korzeni
Budowa nici infekcyjnych i guzków wymaga intensywnego przebudowywania błon komórkowych roślin. Ta przebudowa zależy od pęcherzyków — małych pęcherzyków błonowych, które transportują materiały wewnątrz komórek. Ich ruch i czasowanie kontrolują małe molekularne przełączniki znane jako GTPazy. Jednym z takich przełączników jest ARFA1, który kształtuje i kieruje pęcherzyki w wielu organizmach. W kontekście guzków wiążących azot nie było jednak jasne, jak ARFA1 jest regulowany i jak długo pozostaje aktywny, zanim zostanie usunięty.
Nowe ogniwo między ruchem a recyklingiem
Naukowcy poszukiwali białek roślinnych, które fizycznie oddziałują z ARFA1 w modelowej roślinie strączkowej Medicago truncatula. Wykorzystując testy systemu drożdżowego (yeast two-hybrid) i próby interakcji białek w liściach roślin, zidentyfikowali MtCSP1 — białko należące do rodziny adaptorów łączących określone cele z komórkowym „niszczarką” zwana układem ubikwityny. MtCSP1 zawiera domenę BTB/POZ, charakterystyczny motyw białek rekrutujących wybrane partnery do kompleksów opartych na Cullin 3, które znakują białka do degradacji. Obrazowanie fluorescencyjne wykazało, że MtCSP1 i ARFA1 spotykają się na pęcherzykach zlokalizowanych w późnych endosomach — komórkowych stacjach, które często kierują ładunek ku degradacji.
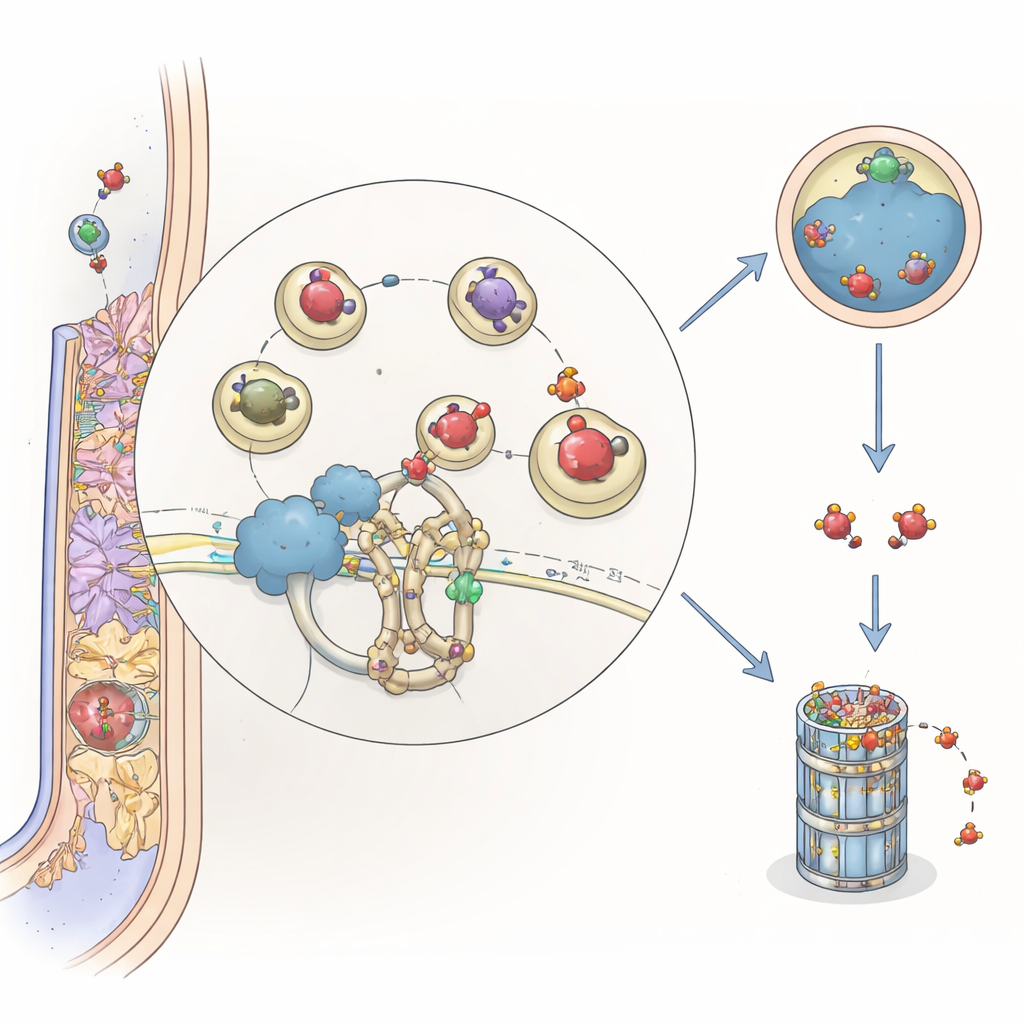
Kiedy i gdzie działa nowy gracz
Aby ustalić, kiedy MtCSP1 jest wykorzystywany, zespół śledził aktywność jego promotora, switcha DNA kontrolującego produkcję białka. Stwierdzili, że MtCSP1 jest włączony w czubkach korzeni, w powstających korzeniach bocznych oraz w kluczowych obszarach rozwijających się i dojrzałych guzków, szczególnie w merystemie (strefie wzrostu) i regionach infekcji. Publiczne zbiory danych ekspresji genów wykazały, że MtCSP1 i ARFA1 są często aktywowane równocześnie, co sugeruje, że roślina koordynuje obecność przełącznika (ARFA1) i adaptorа (MtCSP1) podczas formowania organów korzeniowych.
Dostrajanie liczby guzków i przebiegu infekcji
Naukowcy następnie zmienili poziomy MtCSP1 w korzeniach. Gdy MtCSP1 został wyciszony za pomocą interferencji RNA, rośliny tworzyły z czasem mniej guzków, a wiele nici infekcyjnych zatrzymywało się w włoskach korzeniowych zamiast docierać do wewnętrznych warstw korzenia. Jednak utworzone guzki miały normalny rozmiar, co wskazuje, że MtCSP1 wpływa głównie na inicjację i postęp infekcji, a nie na późniejszy wzrost. Z drugiej strony, nadprodukcja MtCSP1 powodowała rozwój większej liczby guzków i zmiany w przebiegu zdarzeń infekcyjnych, ponownie bez istotnych zmian wielkości czy kształtu guzków. Wyniki te wskazują, że MtCSP1 nie jest niezbędny do zapoczątkowania nici infekcyjnych, ale jest kluczowy dla ich prawidłowego przebiegu i skutecznego powstawania nowych guzków.
Recykling przełączników kontroluje symbiozę
Składając elementy w całość, autorzy proponują, że MtCSP1 działa jako przewodnik, który przenosi ARFA1, w formie aktywnej lub nieaktywnej, do maszyny ubikwitynowej opartej na Cullin 3 na pęcherzykach późnych endosomów. Tam ARFA1 może zostać oznaczony i skierowany albo do wakuoli na degradację, albo do proteasomu, co pomaga wyłączyć lub dostroić transport pęcherzykowy po wykonaniu jego zadania. Regulując czas dostępności ARFA1, MtCSP1 pozwala roślinie precyzyjnie sterować skomplikowaną choreografią nici infekcyjnych i formowania guzków. Dla laika przekaz jest taki: rośliny strączkowe używają wewnętrznego systemu recyklingu, by kontrolować maleńkie molekularne światła drogowe w swoich korzeniach — zapewniając, że ich naturalne fabryki nawozu powstają wydajnie i we właściwym czasie.
Cytowanie: Rípodas, C., Cretton, M., Eylenstein, A. et al. Cullin 3 substrate-adaptor protein 1 (MtCSP1) modulates nodulation through interaction with the GTPase ARFA1. Sci Rep 16, 8938 (2026). https://doi.org/10.1038/s41598-026-41112-2
Słowa kluczowe: wiążące azot, guzki roślin strączkowych, degradacja białek, transport pęcherzykowy, symbioza roślina–mikrob