Clear Sky Science · pl
Toksyczne dla komórek działanie nanokompozytu chitozan/selen zmodyfikowanego kwasem glicyryzynowym na linię komórkową osteosarcomy
Nowa nadzieja w leczeniu raka kości
Osteosarcoma, najczęstszy rak kości u nastolatków i młodych dorosłych, jest znany z trudności leczenia bez uszkadzania zdrowych tkanek. W tym badaniu opisano nowy rodzaj precyzyjnie zaprojektowanych, bardzo małych cząstek, które mają atakować komórki nowotworowe w sposób bardziej ukierunkowany, oszczędzając komórki kostne. Łącząc pierwiastek mineralny niezbędny organizmowi, naturalny polimer cukrowy i związek z lukrecji, badacze stworzyli inteligentne „nano‑opakowanie”, zaprojektowane tak, by skłaniać komórki nowotworowe do czystego samobójstwa komórkowego zamiast wywoływać chaotyczną śmierć i stan zapalny.
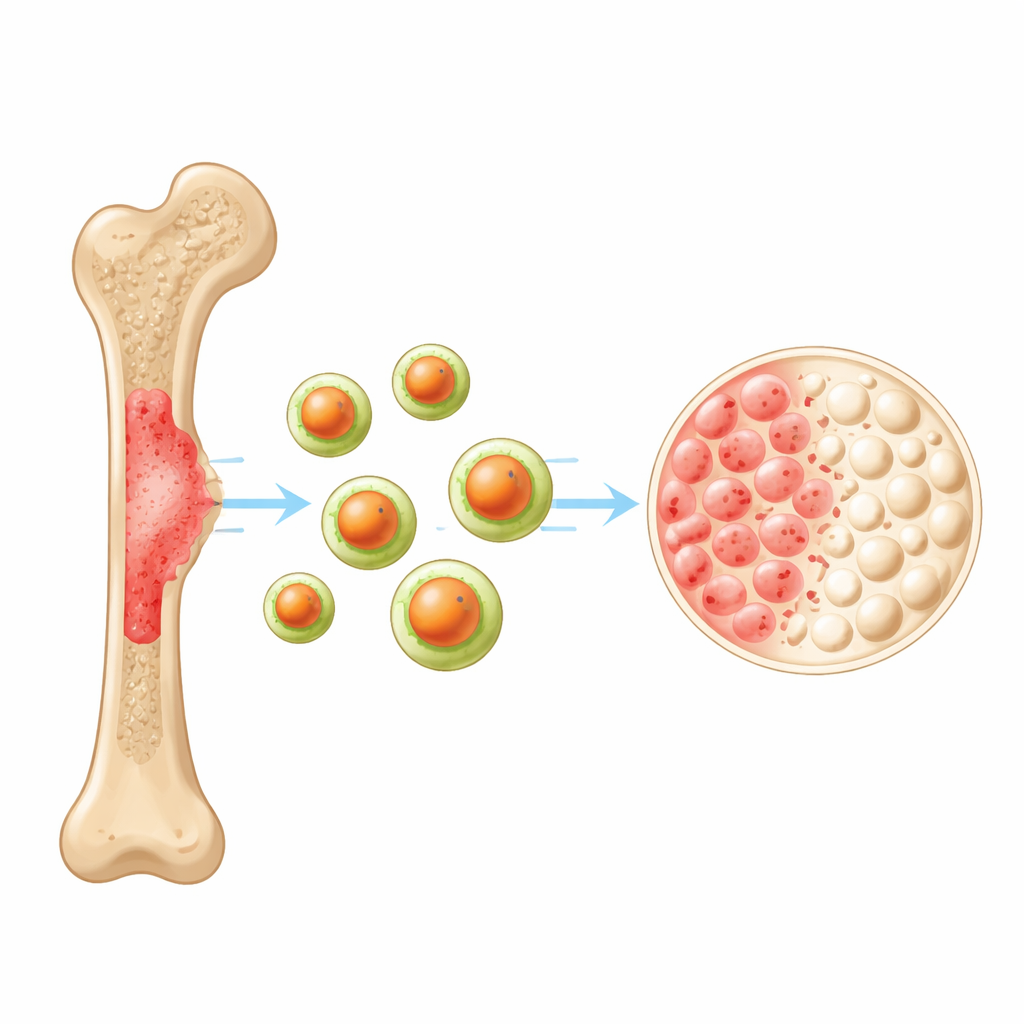
Budowa maleńkiego, trójwarstwowego „wojownika”
Zespół opracował nanocząstki z trzema głównymi składnikami. W rdzeniu znajduje się selen, pierwiastek śladowy znany z działania uszkadzającego komórki nowotworowe poprzez zwiększanie ilości reaktywnych form tlenu wewnątrz nich. Ten rdzeń otoczono chitozanem — biopolimerem pochodzenia naturalnego, np. z pancerzy skorupiaków — który stabilizuje cząstki w wodzie i poprawia ich zdolność do wnikania do komórek. Powierzchnię zmodyfikowano kwasem glicyryzynowym, związkiem z korzenia lukrecji o właściwościach przeciwnowotworowych i przeciwzapalnych. Dzięki mikroskopii elektronowej i innym testom strukturalnym badacze potwierdzili, że cząstki są niemal sferyczne, mają około 100–200 nanometrów średnicy i są równomiernie pokryte — zakres wielkości uznawany za optymalny do przemieszczania się po organizmie i przenikania do tkanek nowotworowych.
Stabilna konstrukcja i dobre „zachowanie” w organizmie
Pomiary ładunku powierzchniowego wykazały, że zarówno podstawowe cząstki chitozan–selen, jak i wersja zmodyfikowana lukrecją mają umiarkowanie dodatni ładunek, wystarczający, by się odpychać i utrzymywać równomierne rozproszenie, a nie zbrylanie. Analizy w podczerwieni i rentgenowskie wykazały, że kwas glicyryzynowy jest trwale związany z powłoką chitozanową, nie zakłócając przy tym krystalicznej struktury rdzenia selenowego. Takie połączenie sugeruje solidną strukturę zdolną do krążenia, oddziaływania z powierzchniami komórek i stopniowego uwalniania składników czynnych. Powłoka z chitozanu poprawia też zgodność z tkankami żywymi i wspiera kontrolowane uwalnianie selenu, co potencjalnie redukuje skutki uboczne w porównaniu z wolnymi lekami lub niestabilnymi cząstkami.
Mocniejsze uderzenie w komórki nowotworowe niż w zdrowe
Cząstki testowano na ludzkich komórkach osteosarcomy oraz na normalnych komórkach zrębu szpiku kostnego hodowanych w warunkach laboratoryjnych. Wszystkie trzy badane formuły — sam kwas glicyryzynowy, cząstki chitozan–selen oraz pełny trójskładnikowy nanokompozyt — obniżały przeżywalność komórek nowotworowych wraz ze wzrostem dawki. Najbardziej agresywne były cząstki chitozan–selen, nanokompozyt zmodyfikowany lukrecją działał nieco łagodniej, a sam kwas glicyryzynowy najsłabiej. Co istotne, żadna z formuł nie osiągnęła w tym samym zakresie stężeń dawki uszkadzającej normalne komórki szpiku, co sugeruje obiecującą selektywność wobec komórek nowotworowych. Barwienia rozróżniające uporządkowaną samobójczą śmierć komórki (apoptozę) od chaotycznego rozpadu (nekrozy) wykazały, że nanokompozyt przesuwał komórki nowotworowe w stronę apoptozy i z dala od nekrozy, w przeciwieństwie do niemodyfikowanych cząstek selenowych, które powodowały więcej destrukcyjnej śmierci nekrotycznej.
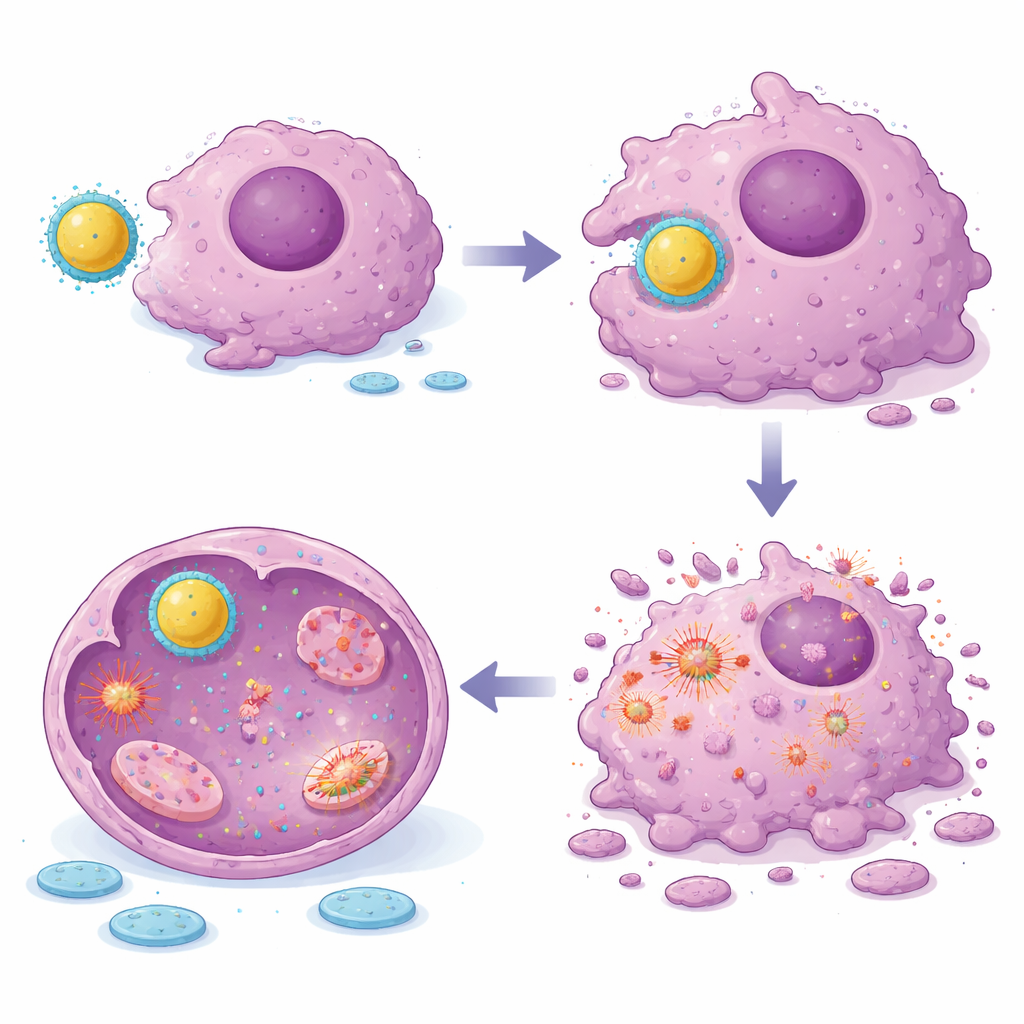
Wywoływanie „czystych” sygnałów samobójczych wewnątrz komórek guza
Aby zrozumieć, jak te cząstki zabijają komórki nowotworowe, badacze zmierzyli kluczowe wewnętrzne sygnały kontrolujące decyzje o życiu i śmierci komórki. Nanokompozyt zmodyfikowany lukrecją silnie zwiększał ekspresję genów i białek promujących apoptozę, takich jak Bax i supresor guza p53, jednocześnie obniżając poziomy Bcl‑2 — cząsteczki zwykle chroniącej komórki przed śmiercią. Ten wzorzec jest charakterystyczny dla dobrze regulowanego programu samobójstwa komórkowego zależnego od mitochondriów, a nie przypadkowych uszkodzeń. Mikroskopia białek znakowanych fluorescencyjnie potwierdziła wyższe poziomy Bax i p53 oraz niższe Bcl‑2 w leczonych komórkach osteosarcomy, szczególnie po zastosowaniu nanokompozytu. Zmiany te pasują do koncepcji, że selen w rdzeniu generuje stres oksydacyjny, podczas gdy kwas glicyryzynowy dopracowuje szlaki zapalne i przetrwania, dając skoordynowany impuls prowadzący do zaprogramowanej śmierci komórek nowotworowych.
Co to może znaczyć dla przyszłej opieki nad rakiem kości
Dla laika kluczową informacją jest to, że badacze stworzyli maleńką, trójwarstwową cząstkę, która potrafi nakłonić komórki raka kości do kontrolowanej śmierci, pozostawiając w dużej mierze nienaruszone pobliskie komórki normalne — przynajmniej w hodowlach laboratoryjnych. Łącząc działanie stresujące komórki nowotworowe przez selen, łagodne właściwości dostarczające chitozanu oraz przeciwnowotworowy, łagodzący wpływ związku z lukrecji, konstrukcja ta ma na celu maksymalizację zabijania guza i minimalizację szkodliwego zapalenia czy uszkodzeń sąsiednich tkanek. Chociaż wyniki są wstępne i ograniczone do kultur komórkowych, wskazują na przyszłe podejście w nanomedycynie, w którym inteligentne cząstki mogłyby uzupełniać lub udoskonalać istniejące terapie osteosarcomy, czyniąc leczenie bardziej celowanym, skutecznym i potencjalnie mniej toksycznym.
Cytowanie: El-ghannam, G., Elfeky, S.A., Abo-Elfadl, M.T. et al. The cytotoxic effects of glycyrrhizic acid-modified chitosan/selenium nanocomposite on osteosarcoma cancer cell line. Sci Rep 16, 9677 (2026). https://doi.org/10.1038/s41598-026-41099-w
Słowa kluczowe: osteosarcoma, nanoparticles, selenium, chitosan, glycyrrhizic acid