Clear Sky Science · pl
Wzrost in situ heterogenicznego Au na nanoszczepinach MoS2 do detekcji SERS miR-210-3p i miR-9-3p pochodzących z raka piersi
Przekształcanie drobnych sygnałów raka w wyraźne ostrzeżenia
Lekarze od dawna wiedzą, że komórki nowotworowe uwalniają do krwi drobne fragmenty materiału genetycznego, jednak wiarygodne wykrywanie tych słabych „szeptów” choroby było trudne. W tym badaniu wprowadzono nowy nanoskalowy sensor, który wykorzystuje specjalne połączenie złota i dwuwymiarowego materiału zwanego dwusiarczkiem molibdenu (MoS2) do wzmocnienia tych słabych sygnałów. Celem jest ułatwienie wykrywania mikroRNA związanych z rakiem piersi — krótkich fragmentów RNA powiązanych z rozwojem i przerzutami guza — przy użyciu łagodnej techniki opartej na świetle, która pewnego dnia mogłaby wspierać wcześniejszą i bardziej precyzyjną diagnostykę.
Dlaczego te drobne cząsteczki mają znaczenie
MicroRNA to niezwykle krótkie nici kodu genetycznego, które pomagają kontrolować zachowanie komórek. W raku niektóre microRNA stają się nadmiernie obfite lub zubożałe, co czyni je silnymi biomarkerami do diagnostyki i prognozy. Problem polega na tym, że występują na bardzo niskich poziomach, często wymieszane w złożonych płynach biologicznych, takich jak krew czy ekstrakty komórkowe. Konwencjonalne narzędzia, takie jak PCR i sekwencjonowanie, potrafią je wykrywać, lecz wymagają specjalistycznych laboratoriów, wyszkolonego personelu i czasochłonnych procedur. Badacze postawili sobie za cel zbudowanie bardziej bezpośredniej platformy detekcyjnej, która w zasadzie mogłaby być prostsza w użyciu, zachowując jednocześnie bardzo wysoką czułość i zdolność rozróżniania wielu celów microRNA jednocześnie.
Budowa nanoszuflady wzmacniającej światło
Aby to osiągnąć, zespół opracował materiał hybrydowy z cienkich nanoszczepin MoS2 ozdobionych nanocząstkami złota. MoS2 to materiał w postaci arkusza o grubości zaledwie kilku atomów, oferujący dużą powierzchnię do adsorpcji cząsteczek oraz silną interakcję z metalami. Zamiast dodawać uprzednio uformowane cząstki złota, złoto hodowano bezpośrednio na powierzchni MoS2 w roztworze. Wzrost in situ dał celowo heterogeniczny krajobraz cząstek złota — przeważnie kulistych, ale także trójkątnych i o nieregularnych kształtach — rozłożonych po powierzchni i wzdłuż krawędzi arkuszy MoS2. Mikroskopia i spektroskopia potwierdziły, że złoto i MoS2 utworzyły stabilny kompozyt, ze złotem mocno zakotwiczonym w miejscach bogatych w defekty na arkuszach. Ta nieregularna, „szorstka” architektura jest kluczowa, ponieważ naturalnie tworzy liczne drobne szczeliny i ostre elementy, gdzie światło może być silnie skoncentrowane.
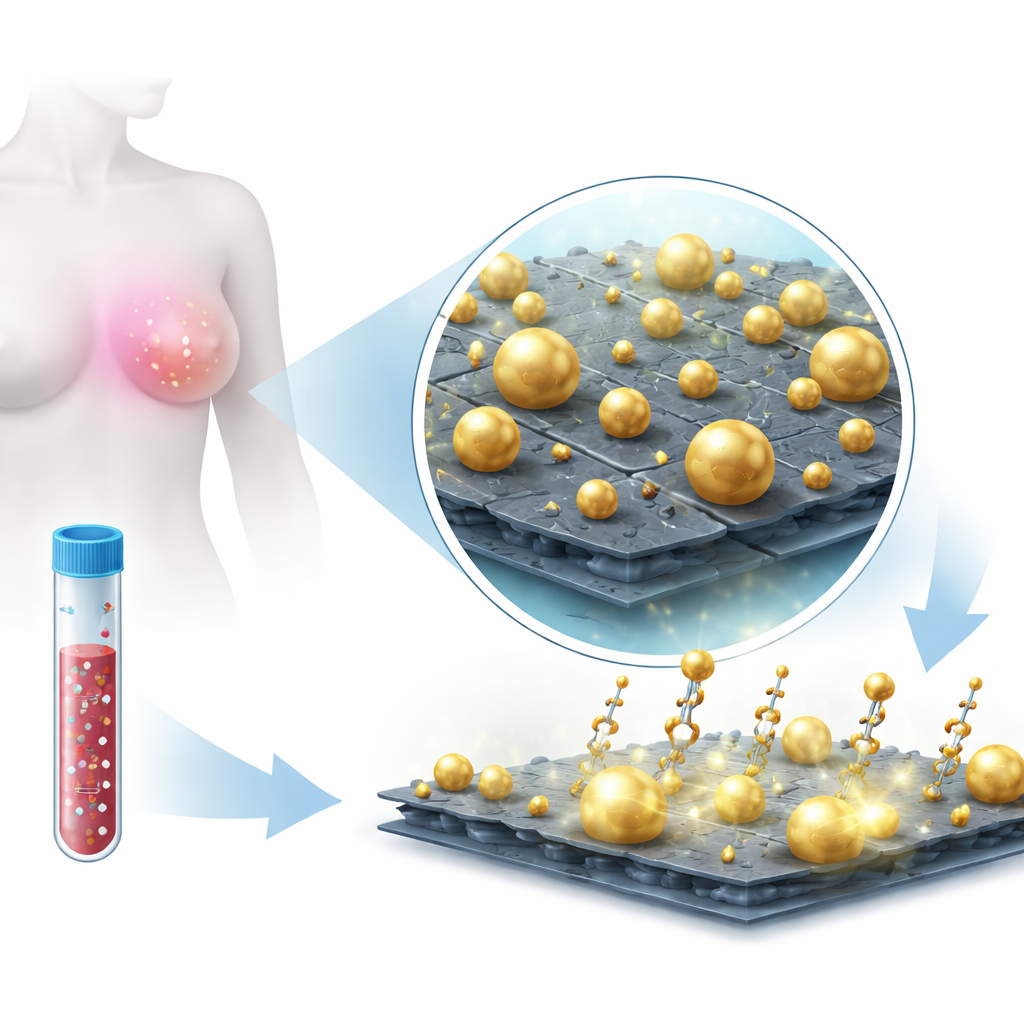
Wykorzystanie światła do odczytu molekularnych odcisków palców
Platforma działa przy użyciu wzmocnionego rozproszenia Ramana na powierzchni (SERS), techniki, w której światło laserowe rozprasza się na cząsteczkach i zwraca widmowy „odcisk palca”. Samo microRNA jest zbyt małe i „ciche”, by zostać łatwo usłyszane w ten sposób. Badacze zamiast tego użyli krótkich sond podobnych do DNA, zwanych zablokowanymi nukleinowymi kwasami (LNA), które wiążą się z określonymi sekwencjami microRNA związanymi z rakiem piersi, w szczególności miR-210-3p i miR-9-3p. Te sondy niosły jasne barwniki (Cy3 i Cy5.5), które dają silne sygnatury Ramana, gdy znajdują się blisko złoto-ozdobionej powierzchni MoS2. Gdy docelowe microRNA łączy się z odpowiadającą sondą LNA, barwnik zostaje umieszczony wewnątrz złotych „hotspotów”, gdzie lokalne pole świetlne jest znacznie wzmocnione przez skoordynowane działanie nanocząstek metalu i arkusza MoS2. Przy użyciu niskoenergetycznego lasera w bliskiej podczerwieni zespół mógł rejestrować wyraźne spektra Ramana z odrębnymi pikami odzwierciedlającymi ilość obecnego microRNA.
Od syntetycznych celów do prawdziwych komórek nowotworowych
Po potwierdzeniu struktury i stabilności ich nanokompozytu, badacze przetestowali go za pomocą syntetycznych sekwencji microRNA w celu kalibracji i walidacji wydajności. Stwierdzili, że różne piki widmowe każdego barwnika reagowały czułe i liniowo w szerokich zakresach stężeń, co pozwoliło obliczyć granice detekcji sięgające kilku bilionowych części mola (poziomy pikomolowe). Co istotne, nie polegano na pojedynczym piku, lecz zastosowano analizę wielopikową, by zwiększyć niezawodność, zwłaszcza w złożonych próbkach. Platformę przetestowano następnie na microRNA wyizolowanych z agresywnej linii komórek raka piersi. Niezależne pomiary PCR wykazały, że jedno microRNA, miR-210-3p, było znacznie bardziej obfite niż miR-9-3p w tych komórkach. Korzystając z tego samego układu SERS, sensor MoS2–złoto potrafił wykryć pochodzące z komórek miR-210-3p i miR-9-3p do około 0,1 nanomola i 0,018 nanomola, odpowiednio, przy zachowaniu delikatnego RNA dzięki łagodnemu oświetleniu.
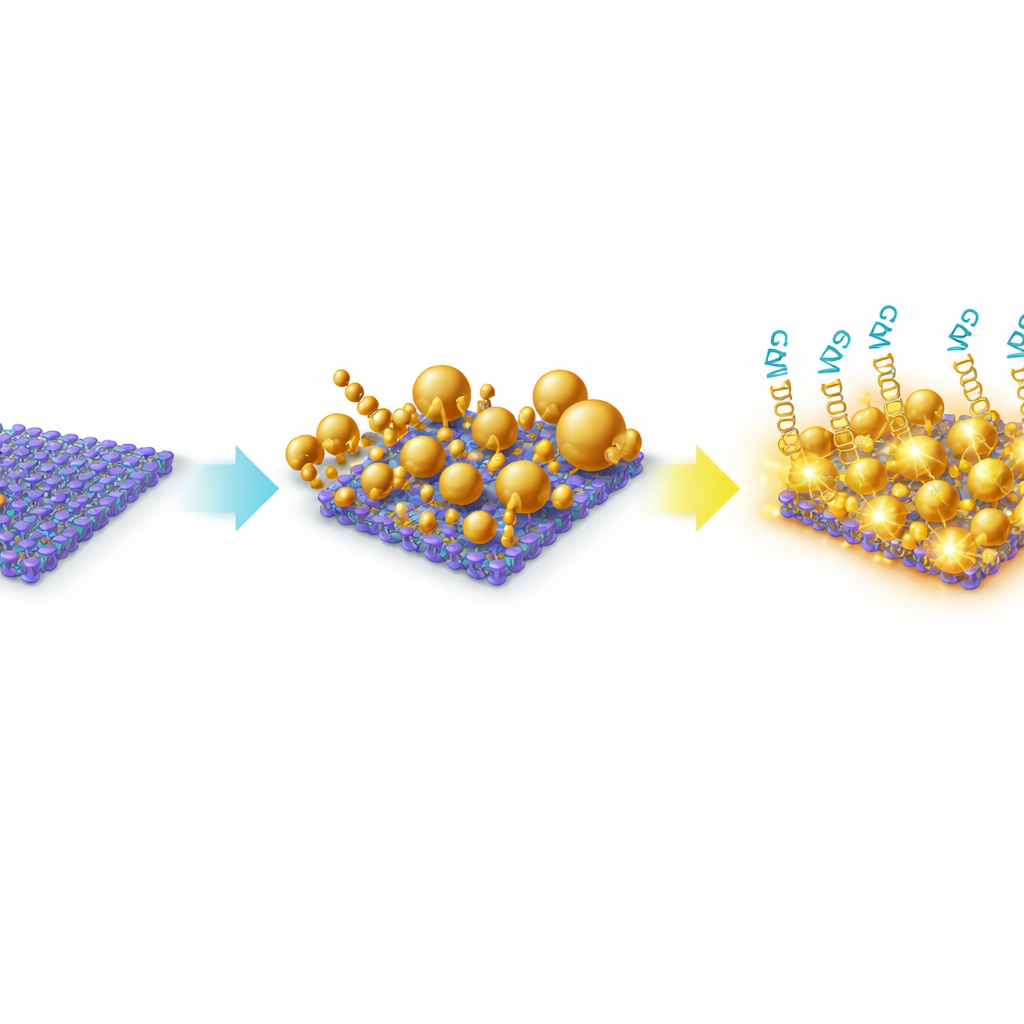
Co to może oznaczać dla przyszłych testów na raka
Choć prace te znajdują się nadal na etapie laboratoryjnym, wytyczają jasną ścieżkę przekształcenia starannie zaprojektowanej nanosurfacy w praktyczne narzędzie diagnostyczne. Poprzez celowe hodowanie złota o różnych kształtach i rozmiarach na MoS2, badacze stworzyli gęstą sieć wzmacniających światło hotspotów, które potrafią odczytać obecność specyficznych microRNA za pomocą ich znakowanych barwnikami. Umiarkowane, lecz dobrze kontrolowane wzmocnienie sygnału, w połączeniu z analizą wielopikową, umożliwia ilościową detekcję w szerokim zakresie stężeń zarówno w próbkach czystych, jak i biologicznie złożonych. W dłuższej perspektywie podejście to mogłoby wspierać kompaktowe, multiplikowane testy monitorujące jednocześnie kilka microRNA powiązanych z rakiem, dostarczając klinicystom pełniejszy obraz stanu guza z niewielkich próbek i potencjalnie wspomagając bardziej spersonalizowane decyzje terapeutyczne.
Cytowanie: Zablon, F.M., Pathiraja, G., Dellinger, K. et al. In-situ growth of heterogeneous Au on MoS2 nanosheets for SERS detection of breast cancer-derived miR-210-3p and miR-9-3p. Sci Rep 16, 8902 (2026). https://doi.org/10.1038/s41598-026-41084-3
Słowa kluczowe: biomarkery raka piersi, detekcja microRNA, nanosensory SERS, kompozyty nanocząstek złota, biosensowanie oparte na MoS2