Clear Sky Science · pl
Prognozowanie przerzutów raka jelita grubego do wątroby za pomocą modelu radiomicznego z MRI
Dlaczego to badanie ma znaczenie
Rak jelita grubego jest jednym z głównych zabójców na świecie, przede wszystkim dlatego, że często rozprzestrzenia się do wątroby przed lub po pierwszym zabiegu chirurgicznym. Wczesne wykrycie tego rozsiewu może diametralnie zmienić rokowania pacjenta, jednak dzisiejsze skany i badania krwi są dalekie od doskonałości. W tym badaniu sprawdzono, czy komputery potrafią „czytać między pikselami” rutynowych badań MRI pierwotnego guza jelita, by przewidzieć, którzy pacjenci są najbardziej narażeni na rozwój przerzutów do wątroby — na długo zanim przerzuty staną się widoczne.
Widzimy więcej niż oko
Standardowe obrazowanie medyczne jest zwykle interpretowane przez ludzkie oko, które świetnie radzi sobie z wykrywaniem oczywistych mas, ale mniej dostrzega subtelne wzory. Radiomika to nowe podejście, które traktuje każde badanie jako kopalnię mierzalnych danych. Przekształcając odcienie szarości, kształty i tekstury w setki cech numerycznych, radiomika pozwala komputerom wykrywać wzorce związane z agresywnością guza. W tej pracy badacze skoncentrowali się na dwóch powszechnych sekwencjach MRI stosowanych przy raku jelita grubego: obrazach T2 z ważeniem, które pokazują anatomię i płyny, oraz obrazach z ważeniem dyfuzyjnym, które odwzorowują ruch wody w tkankach i są wrażliwe na gęstość komórek nowotworowych.
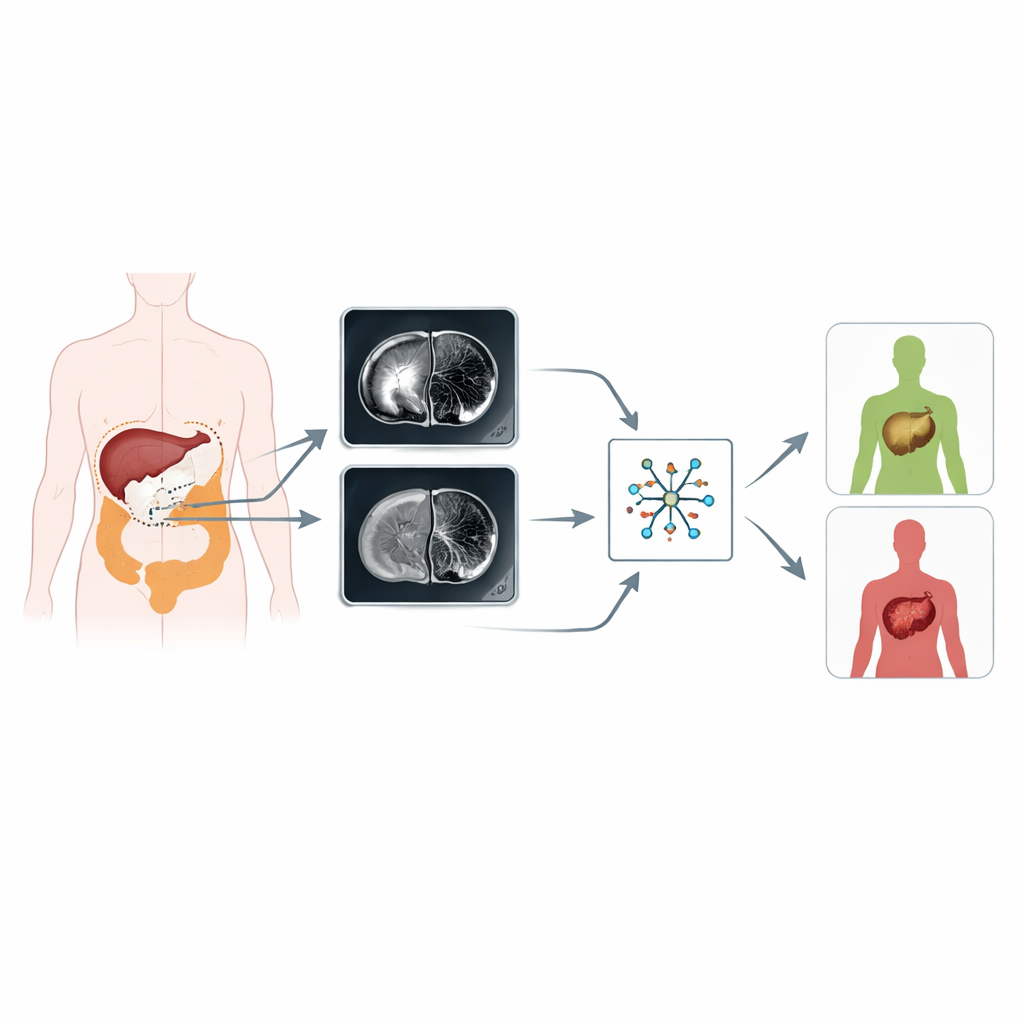
Jak przeprowadzono badanie
Zespół przeanalizował 194 pacjentów z patologicznie potwierdzonym rakiem jelita grubego z dwóch szpitali. Wszyscy pacjenci mieli wykonane MRI przed rozpoczęciem leczenia i byli obserwowani przez co najmniej rok, aby ustalić, u których rozwinęły się przerzuty do wątroby. Za pomocą specjalistycznego oprogramowania radiolodzy starannie odrysowali każdy guz pierwotny na obrazach T2 i obrazach z ważeniem dyfuzyjnym, warstwa po warstwie, unikając gazu, torbieli i otaczającej tkanki tłuszczowej. Z tych obszarów komputer wyekstrahował 352 cechy radiomiczne opisujące kształt guza i jego wewnętrzną teksturę. Następnie zastosowano techniki statystyczne, aby sprawdzić, czy te pomiary są wiarygodne między różnymi obserwatorami i skanerami, odfiltrować redundantne informacje i zawęzić listę do najbardziej informatywnych cech.
Tworzenie i testowanie modeli predykcyjnych
Mając najbardziej użyteczne cechy, badacze zbudowali kilka modeli predykcyjnych. Jeden opierał się wyłącznie na prostych informacjach klinicznych, takich jak wiek i markery nowotworowe we krwi; inne wykorzystywały osobno radiomikę z obrazów T2 lub z obrazów dyfuzyjnych. Połączony model radiomiczny scalał cechy z obu sekwencji MRI, a ostateczny „model unii” łączył te cechy obrazowe z czynnikami ryzyka ze sfery klinicznej. Zespół trenował te modele na większej grupie pacjentów z jednego szpitala, a następnie testował je na niezależnej grupie z drugiego szpitala, sprawdzając, jak dokładnie każdy model potrafi rozróżnić pacjentów, u których wystąpiły przerzuty do wątroby, od tych, u których ich nie było.
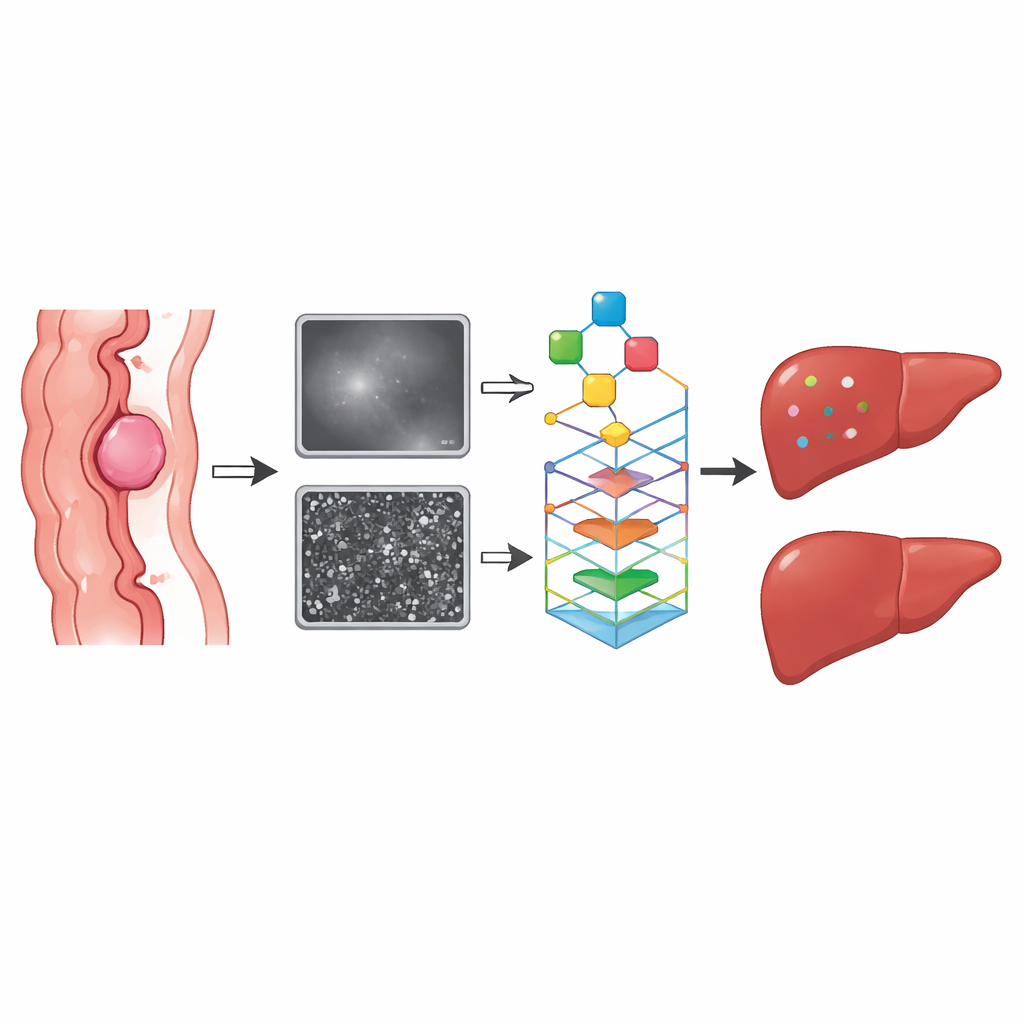
Co ujawniły modele
Najlepiej wypadł połączony model obrazowo-kliniczny. Zarówno w zbiorze treningowym, jak i w walidacyjnym przewyższał modele oparte wyłącznie na danych klinicznych lub na pojedynczej sekwencji MRI. Jego zdolność do oddzielenia pacjentów o wysokim i niskim ryzyku, mierzona polem pod krzywą ROC, mieściła się w wysokim zakresie „dobrym”. Szczególnie istotne okazały się cechy opisujące teksturę i kształt guza: guzy bardziej nieregularne i heterogenne były częściej związane z późniejszym rozsiewem do wątroby. Marker krwi zwany antygenem karcinoembrionalnym (CEA) ujawnił się jako niezależny czynnik ryzyka klinicznego i dodatkowo zwiększał dokładność modelu po zintegrowaniu z cechami radiomicznymi.
Otwieranie czarnej skrzynki
Aby uczynić ten złożony model bardziej przejrzystym, badacze zastosowali metodę znaną jako SHAP, która przypisuje każdej cesze udział w konkretnej predykcji. Analiza ta wykazała, że szczególna cecha teksturalna z obrazów dyfuzyjnych miała najsilniejszy wpływ na to, czy model oznaczył pacjenta jako wysokiego ryzyka. Wskazując, które wzory obrazu mają największe znaczenie, narzędzia interpretowalności mogą zwiększyć zaufanie klinicystów do stosowania predykcji opartych na sztucznej inteligencji w praktyce.
Co to oznacza dla pacjentów
Badanie sugeruje, że rutynowo wykonywane skany MRI pierwotnego guza jelita grubego zawierają ukryte wskazówki dotyczące tego, czy komórki nowotworowe prawdopodobnie zasieją w wątrobie. Łącząc te subtelne sygnatury obrazowe ze standardowymi badaniami krwi, model radiomiczny mógłby pomóc lekarzom wcześniej identyfikować pacjentów wysokiego ryzyka, dostosować harmonogramy kontroli i wybierać bardziej intensywne lub ukierunkowane leczenie, gdy zajdzie taka potrzeba. Chociaż nadal konieczne są większe, prospektywne badania, zanim podejście to będzie mogło być szeroko stosowane, wskazuje ono na przyszłość, w której komputery pomogą uwolnić dodatkową moc prognostyczną z obrazów już wykonywanych, bez narażania pacjentów na dodatkowe procedury.
Cytowanie: Wu, YK., Wang, X., Du, PZ. et al. Prediction of colorectal cancer liver metastasis through an MRI radiomic model. Sci Rep 16, 11148 (2026). https://doi.org/10.1038/s41598-026-40970-0
Słowa kluczowe: rak jelita grubego, przerzuty do wątroby, radiomika MRI, predykcja raka, obrazowanie medyczne