Clear Sky Science · pl
Klasyfikacja przekrojów mrożonych w skali całego raka za pomocą wizjonera Transformer z miękką mieszanką ekspertów w warunkach słabej nadzorności
Dlaczego to ma znaczenie na sali operacyjnej
Kiedy chirurdzy usuwają podejrzany guz, często mają zaledwie kilka minut, by ustalić, czy cały nowotwór został usunięty. Patolodzy spieszą się, by zbadać szybko zamrożony wycinek tkanki i udzielić odpowiedzi, gdy pacjent wciąż leży na stole operacyjnym. Ten działający pod presją czasową proces może być utrudniony przez rozmazane preparaty, subtelne zmiany nowotworowe oraz zwykłe ograniczenia czasowe. Opisane tutaj badanie analizuje, jak system sztucznej inteligencji (AI) może pomóc patologom szybko i niezawodnie odróżniać tkanki niegroźne od złośliwych w wielu narządach, wykorzystując sprzęt realistyczny dla codziennych warunków szpitalnych.
Szybkie badanie z wbudowanymi wyzwaniami
Analiza przekrojów mrożonych to standard współczesnej chirurgii: cienki fragment tkanki jest zamrażany, krojony, barwiony i oglądany pod mikroskopem, aby ocenić, czy jest łagodny czy złośliwy oraz czy margines chirurgiczny jest czysty. W przeciwieństwie do preparatów utrwalonych, przekroje mrożone często cierpią na pęknięcia, fałdy i nierównomierne barwienie. Różni patolodzy mogą mieć odmienne opinie w przypadkach granicznych, a zegar zawsze tyka. Problemy te są szczególnie dotkliwe w mniejszych lub zatłoczonych szpitalach, gdzie kilku specjalistów musi obejmować wiele typów nowotworów. Autorzy argumentują, że odporny asystent oparty na komputerze mógłby uczynić decyzje dotyczące przekrojów mrożonych bardziej spójnymi, szybszymi i szerzej dostępnymi.
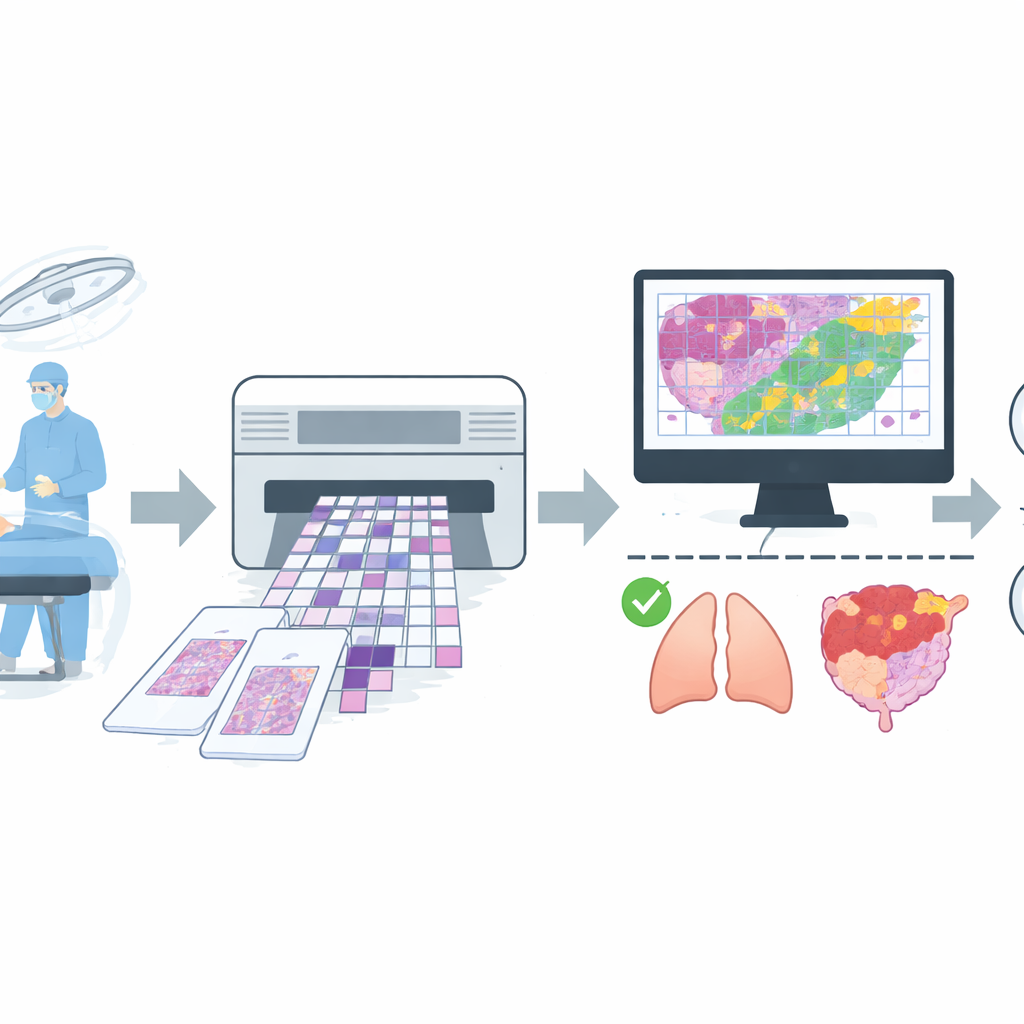
Budowanie szerokiego, realistycznego zbioru obrazów
Aby wytrenować takiego asystenta, zespół zgromadził dużą kolekcję obrazów cyfrowych pochodzących z rutynowych operacji w dużym szpitalu. Zebrano 4 754 całopreparatowych obrazów przekrojów mrożonych od ponad 2 600 pacjentów, a następnie zastosowano surowe reguły jakościowe, aby usunąć preparaty z ciężkimi artefaktami lub niepewnymi diagnozami. Końcowy zbiór zawierał 4 667 skanów, z których każdy był oznaczony w prosty sposób jako łagodny lub złośliwy na podstawie zgodności między szybką oceną mrożoną a późniejszym, bardziej wnikliwym raportem z preparatu utrwalonego. Preparaty obejmowały typowe lokalizacje, takie jak płuca, pierś, tarczyca, węzły chłonne i narządy rozrodcze żeńskie, oraz grupę mieszanych, mniej częstych lokalizacji, jak żołądek, wątroba i skóra. Dane zostały podzielone na osobne zbiory do treningu, strojenia i testów końcowych, z zachowaniem ostrożności, aby obrazy od tego samego pacjenta nie pojawiały się w więcej niż jednej grupie.
Jak AI uczy się ze słabych wskazówek
Naukowcy zbudowali swój model na klasie sieci neuronowych zwanych Vision Transformer, które świetnie radzą sobie ze znajdowaniem wzorców w dużych obrazach. Każdy olbrzymi obraz tkanki był automatycznie dzielony na wiele mniejszych kafelków i fragmentów, aby mógł być przetwarzany na standardowym sprzęcie graficznym. Kluczową innowacją było zastąpienie części sieci „miękką mieszanką ekspertów” — zbiorem wielu małych, wyspecjalizowanych gałęzi, z których każda skupia się na różnych wzorcach wizualnych. Zamiast włączać i wyłączać ekspertów, system płynnie miesza ich wkład, co stabilizuje uczenie i lepiej wykorzystuje ograniczone dane. Ponieważ patolodzy nie rysowali konturów guzów, model musiał uczyć się ze słabej nadzorności: znał tylko, czy cały preparat jest łagodny czy złośliwy. Strategia uczenia wieloinstancyjnego promowała najbardziej podejrzane fragmenty w preparacie złośliwym jako przykłady pozytywne, pozwalając sieci stopniowo skoncentrować się na najbardziej informatywnych obszarach.
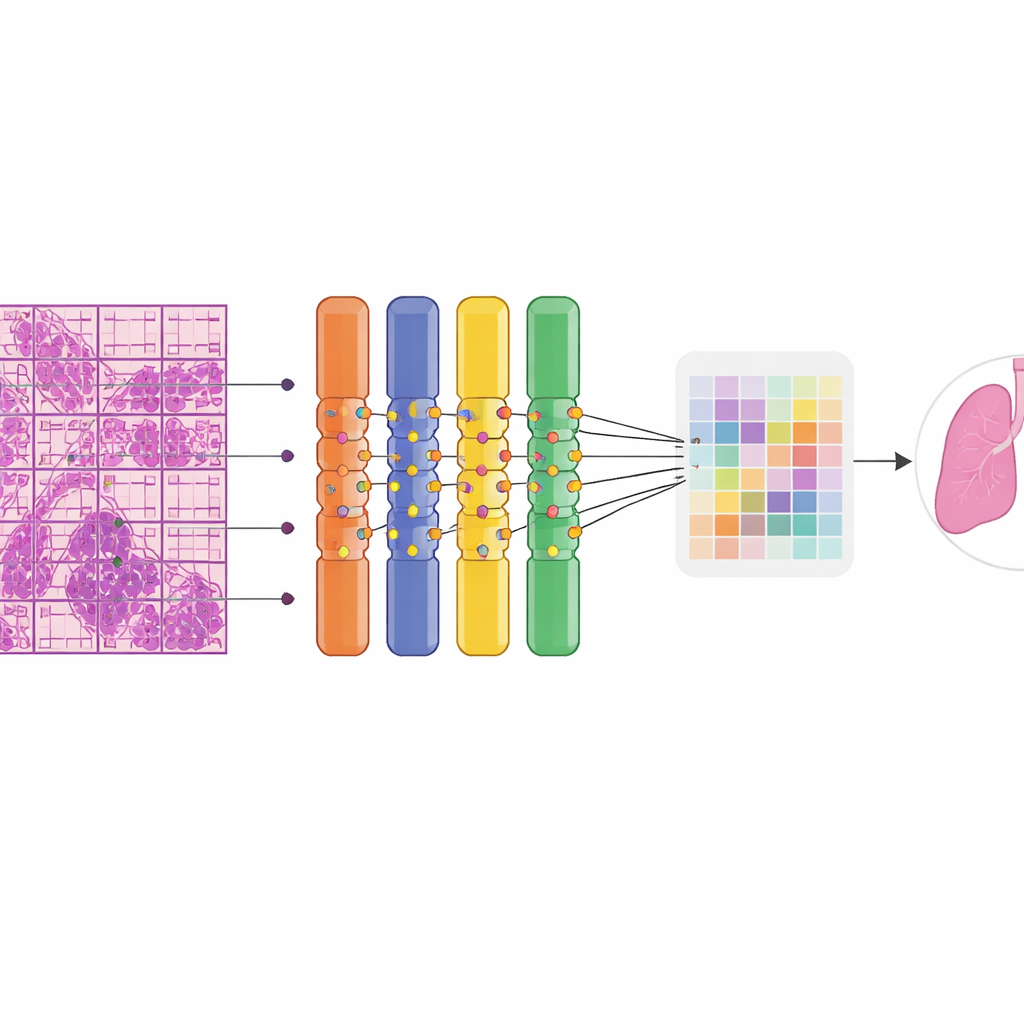
Jak system sprawdza się w praktyce
Testowany na 669 niewidzianych wcześniej preparatach, system AI odróżniał tkanki łagodne od złośliwych z wysoką dokładnością. Prawidłowo sklasyfikował około 90% przypadków ogółem i wykazał doskonałą zdolność rozdzielenia obu grup przy różnych progach prawdopodobieństwa. Czułość, czyli szansa wykrycia naprawdę złośliwego preparatu, wynosiła około czterech na pięć, podczas gdy specyficzność, czyli prawdopodobieństwo poprawnego zaklasyfikowania preparatu łagodnego jako łagodny, była nawet wyższa. Co ważne, wydajność utrzymywała się na wysokim poziomie w różnych narządach: system doskonale wykrył wszystkie złośliwe przypadki płuc i piersi w zbiorze testowym oraz dobrze poradził sobie z rzadszymi grupami, takimi jak guzy przydatków żeńskich i mieszane „inne” narządy. Kolorowe mapy cieplne nałożone na skany ujawniły, że uwaga modelu koncentrowała się na obszarach rozpoznawanych przez ekspertów jako guz, w tym ogniskach przerzutowych w węzłach chłonnych, podczas gdy w dużej mierze ignorowała struktury normalne. System działał wydajnie, potrzebując mniej niż 5 GB pamięci, co czyni go odpowiednim do użycia na powszechnie dostępnych kartach graficznych, a nie na drogich klastrach.
Ograniczenia, potknięcia i pole do poprawy
Autorzy zbadali również miejsca, w których AI popełniała błędy. Wyniki fałszywie negatywne często dotyczyły bardzo rzadkich komórek nowotworowych, rozmazanych obszarów skanu lub silnego zapalenia, które maskowało skupiska złośliwe. Fałszywe pozytywy zwykle pojawiały się w stanach łagodnych naśladujących raka w mikroskopie, takich jak reaktywne przerosty lub zniekształcone tkanki mrożone. Ponieważ rutynowy przebieg pracy chirurgicznej nie obejmuje szczegółowych obrysów regionów nowotworowych, zespół nie mógł dokładnie zmierzyć, jak dobrze mapy cieplne zgadzają się z oznaczeniami ekspertów, polegając zamiast tego na jakościowej ocenie. Niektóre typy narządów, jak język czy niektóre guzy tkanek miękkich, wciąż były niedoreprezentowane, co sugeruje, że potrzeba większych, wieloośrodkowych kolekcji, aby rozszerzyć zasięg systemu.
Co to może znaczyć dla pacjentów i szpitali
Podsumowując, badanie pokazuje, że starannie zaprojektowany system AI może dokładnie i w sposób interpretowalny wspierać podstawowe zadanie patologii chirurgicznej: decydowanie w czasie rzeczywistym, czy tkanka jest łagodna czy złośliwa w różnych typach narządów. Działając tylko na poziomie etykiet preparatu, pracując na powszechnie dostępnym sprzęcie i wskazując podejrzane obszary do weryfikacji przez człowieka, model oferuje praktyczną drogę do bardziej spójnych decyzji dotyczących przekrojów mrożonych. Dla pacjentów może to przełożyć się na lepiej uzasadnione decyzje chirurgiczne wykonywane podczas jednej operacji; dla szpitali, zwłaszcza tych z ograniczoną liczbą ekspertów, wskazuje na przyszłość, w której zaawansowane narzędzia cyfrowe pomagają dostarczać wysokiej jakości opiekę onkologiczną w sposób bardziej sprawiedliwy.
Cytowanie: Wu, J., Yang, M., Li, J. et al. Pan-cancer frozen section classification using a soft mixture of experts vision transformer under weak supervision. Sci Rep 16, 10297 (2026). https://doi.org/10.1038/s41598-026-40924-6
Słowa kluczowe: przekrój mrożony, patologia cyfrowa, diagnoza raka, vision transformer, słabo nadzorowane uczenie