Clear Sky Science · pl
mikroRNA pochodząca z eksonu 4 amelogeniny reguluje tworzenie szkliwa przez kontrolę splicingu eksonu 4 i ekspresji amelogeniny
Dlaczego maleńkie RNA ma znaczenie dla mocnych zębów
Szkliwo zęba jest najtwardszą substancją w ludzkim ciele, a mimo to może być zaskakująco kruche, gdy jego tworzenie przebiega niewłaściwie. W tym badaniu odkryto, jak bardzo mały fragment materiału genetycznego, mikroRNA zwane miR‑exon4, pomaga komórkom tworzącym zęby w budowie odpowiednio utwardzonego szkliwa. Pokazując, że to mikroRNA precyzyjnie dostraja zarówno główny białkowy składnik szkliwa, jak i czas odkładania minerałów, praca łączy subtelne przetwarzanie RNA w komórkach z widocznymi wadami szkliwa podobnymi do obserwowanych w dziedzicznej chorobie zwanej amelogenesis imperfecta.
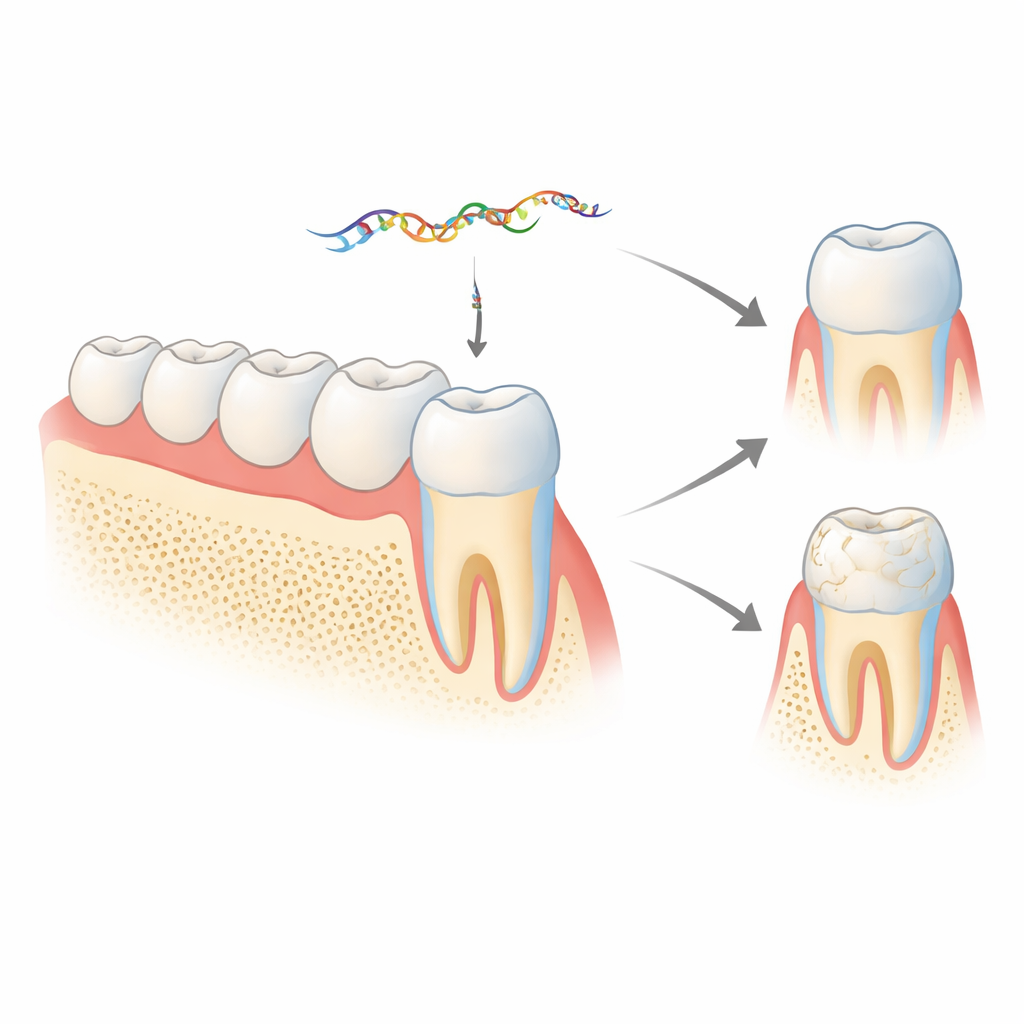
Ukryte przesłanie w genie szkliwa
Szkliwo jest w dużej mierze zbudowane z białka nazywanego amelogeniną, wytwarzanego przez komórki zwane ameloblastami. Gen amelogeniny (Amelx u myszy) może być wycinany i sklejany na różne sposoby, tworząc kilka wersji białka potrzebnych na różnych etapach rozwoju zęba. Jeden krótki segment, zwany eksonem 4, zwykle zostaje usunięty z ostatecznej wiadomości kodującej białko. Wcześniejsze prace tej grupy wykazały, że wyrzucony ekson 4 nie jest odpadkiem: jest przetwarzany na mikroRNA, miR‑exon4, które może regulować inne geny ważne dla kości i szkliwa. Nowe badanie pyta, co się dzieje u żywych zwierząt, gdy to mikroRNA jest zredukowane lub zablokowane, i czy ono samo zwrotnie kontroluje sposób składania amelogeniny.
Łańcuch regulacyjny w komórkach tworzących ząb
Naukowcy najpierw potwierdzili w mysim szkliwie, że miR‑exon4 uczestniczy w łańcuchu regulacyjnym, który wcześniej zmapowali w hodowlach komórkowych. W normalnych narządach szkliwnych miR‑exon4 utrzymuje w ryzach dwa geny nadrzędne, Nfia i Prkch. Gdy są one utrzymywane na niskim poziomie, rosną poziomy kluczowego czynnika transkrypcyjnego RUNX2. Używając myszy, które albo nie miały genu amelogeniny, otrzymały dodatkowe miR‑exon4, albo były leczone blokerem miR‑exon4, zespół wykazał, że obniżenie miR‑exon4 podnosi Nfia i Prkch oraz obniża RUNX2, podczas gdy dodanie miR‑exon4 działa odwrotnie. Potwierdziło to, że szlak miR‑exon4–Nfia/Prkch–RUNX2 działa in vivo w rozwijających się zębach.
Od zaburzonych sygnałów do osłabionego szkliwa
Aby sprawdzić, jak te molekularne przesunięcia wpływają na rzeczywiste szkliwo, naukowcy zahamowali miR‑exon4 u mysich szczeniąt przez tydzień w okresie aktywnego tworzenia zębów. Trójwymiarowe obrazowanie rentgenowskie ujawniło, że zwierzęta poddane zabiegowi miały wyraźny spadek wysoko zmineralizowanego szkliwa zarówno w siekaczach, jak i zębach trzonowych. Mapy cieplne i barwione przekroje pokazały, że początek odkładania minerałów wzdłuż warstwy szkliwa został opóźniony, a wczesna faza mineralizacji skrócona, co prowadziło do chropowatych powierzchni i zatartych granic między szkliwem a leżącymi pod nim tkankami. Jednocześnie poziomy białka RUNX2 w ameloblastach spadły, podczas gdy białko amelogeniny — w tym formy zawierające ekson 4 — wzrosło. Ten wzorzec odzwierciedla wcześniejsze modele, w których nadprodukcja długiej formy amelogeniny z eksonem 4 prowadzi do defektów szkliwa, sugerując, że nadmiar tej izoformy, wywołany utratą miR‑exon4, może bezpośrednio zaburzać normalną mineralizację.
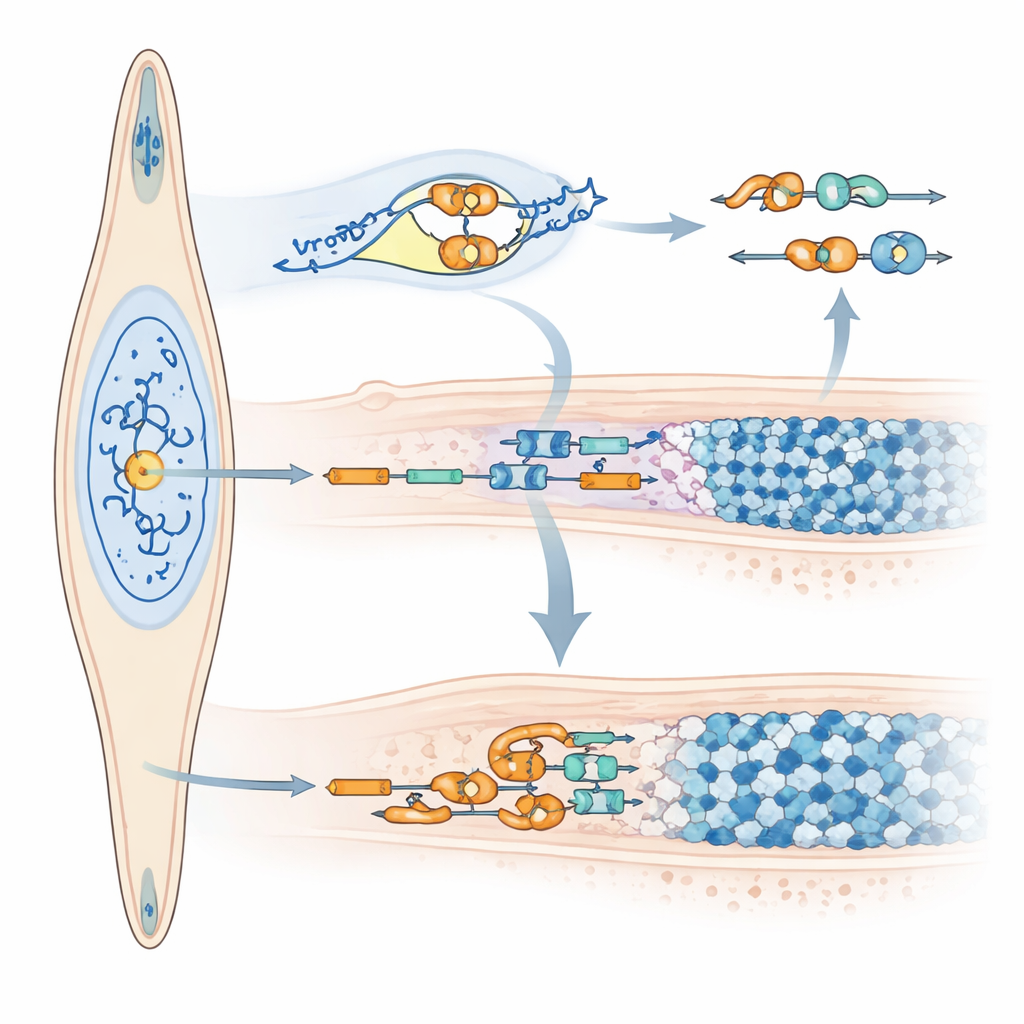
Jak mikroRNA zmienia informację o amelogeninie
Ponad wpływem na ilość wytwarzanej amelogeniny, miR‑exon4 zmienia także sposób, w jaki informacja o amelogeninie jest cięta i składana. Krótkotrwałe zablokowanie miR‑exon4 zmniejszyło cząsteczki RNA wciąż zawierające ekson 4, nie zmieniając całkowitych poziomów amelogeniny, co wskazuje, że ekson 4 był częściej usuwany. Związały to zespół ze zmianami w kilku genach regulatorów splicingu (SRSF), z których niektóre były podniesione, a inne obniżone po redukcji miR‑exon4. W modelach komórkowych niosących specjalnie zmodyfikowaną wersję genu amelogeniny, która produkuje mniej miR‑exon4, ekson 4 również był częściej pomijany. Co istotne, samo mikroRNA znaleziono w jądrze komórkowym, gdzie zachodzi splicing, a testy biochemiczne wykazały, że wiąże się ono z prekursorem RNA amelogeniny w konkretnym punkcie kontrolnym w sąsiednim intronie. Te ustalenia wspierają podwójną rolę miR‑exon4: pośrednie kształtowanie wyboru eksonu przez regulację czynników splicingu oraz bezpośrednie wiązanie w pobliżu eksonu 4, wpływając na to, czy zostanie on zachowany, czy usunięty.
Co to znaczy dla zdrowia szkliwa
Podsumowując, badanie przedstawia miR‑exon4 jako małego, lecz centralnego koordynatora tworzenia szkliwa. Gdy występuje na odpowiednim poziomie, wspiera prawidłową aktywność RUNX2, utrzymuje równowagę produkcji amelogeniny i pomaga zapewnić, że ekson 4 jest włączany lub wyłączany we właściwych etapach. Gdy miR‑exon4 jest nieobecne lub zredukowane, ta równowaga zostaje zaburzona: ścieżki sygnałowe zostają naruszone, ekson 4 jest nieprawidłowo przetwarzany, izoformy amelogeniny ulegają przemieszczeniu, a wczesna mineralizacja szkliwa ulega osłabieniu. Te wnioski pomagają wyjaśnić, jak niektóre mutacje w genie amelogeniny mogą powodować dziedziczne zaburzenia szkliwa i podkreślają znaczenie jądrowych mikroRNA jako istotnych uczestników kształtujących najtwardszą tkankę w ciele.
Cytowanie: Shemirani, R., Duong, T., Kim, R. et al. A splicing-derived microRNA from amelogenin exon4 regulates enamel formation via control of exon4 splicing and amelogenin expression. Sci Rep 16, 11044 (2026). https://doi.org/10.1038/s41598-026-40706-0
Słowa kluczowe: szybkość szkliwa, amelogenina, microRNA, składanie RNA (splicing), amelogenesis imperfecta