Clear Sky Science · pl
ABE9 połączony z nickazą SpRY Cas9 umożliwia precyzyjne tworzenie mysich modeli wolnych od efektów "bystander"
Bardziej precyzyjne narzędzia do budowy lepszych modeli chorób
Wiele poważnych chorób wynika z pojedynczych literówek w naszym DNA. Aby zrozumieć i ostatecznie leczyć te schorzenia, naukowcy często tworzą myszy noszące te same mutacje co pacjenci. Jednak tak precyzyjna korekta DNA okazuje się zaskakująco trudna: starsze metody mogą zostawiać blizny w genomie, wprowadzać dodatkowe mutacje i zniekształcać wyniki eksperymentów. W tym badaniu przedstawiono usprawnione narzędzie do edycji genów, nazwane ABE9‑SpRY, zaprojektowane do zmiany jednej konkretnej litery DNA przy minimalnym wpływie na sąsiadujące litery — i na resztę genomu.
Od agresywnych cięć do delikatnych korekt DNA
Tradycyjna edycja CRISPR‑Cas9 działa jak molekularne nożyce, przecinając obie nici DNA. Komórki naprawiają te przerwy niedokładnie, często pozostawiając małe insercje lub delecje, które nieprzewidywalnie zakłócają działanie genów. To bywa użyteczne do wyłączania genów, ale nie do odtworzenia precyzyjnej mutacji wywołującej chorobę. Edytory zasad, w przeciwieństwie do tego, nie tną DNA. Zamiast tego chemicznie przekształcają jedną literę DNA w inną — tutaj A w G — zachowując strukturę podwójnej helisy. Takie podejście znacząco ogranicza duże delecje i przearanżowania, ale wcześniejsze edytory adeniny wciąż miały trzy główne wady: czasem modyfikowały pobliskie „bystanderowe” litery, mogły działać tylko przy sąsiedztwie określonych krótkich znaczników sekwencji oraz od czasu do czasu wprowadzały zmiany w niezamierzonych miejscach genomu.
Projektowanie bardziej selektywnego „pióra molekularnego”
Naukowcy postanowili jednocześnie rozwiązać wszystkie trzy ograniczenia. Rozpoczęli od ABE9, nowszego wariantu edytora zasad, który skupia swoją aktywność na bardzo wąskim odcinku DNA, znacząco zawężając „okno edycji”, dzięki czemu znacznie mniej sąsiednich liter jest przypadkowo zmienianych. Następnie połączyli ABE9 z inżynieryjną nickazą Cas9 nazwaną SpRY. W odróżnieniu od standardowego Cas9, który wymaga ścisłego znacznika „NGG” obok miejsca docelowego, SpRY rozpoznaje znacznie szerszy zestaw sekwencji DNA. Dzięki temu możliwe jest dotarcie do pozycji związanych z chorobami, które wcześniej były poza zasięgiem. Powstałe narzędzie ABE9‑SpRY ma być zarówno wysoce precyzyjne, jak i znacznie bardziej elastyczne pod względem możliwych celów.
Testowanie nowego edytora w komórkach i embrionach
Aby sprawdzić, czy ABE9‑SpRY spełnia założenia projektu, zespół porównał go z szeroko stosowanym, bardziej agresywnym edytorem o nazwie ABE8e‑SpRY. Skoncentrowali się na czterech pozycjach związanych z chorobami w genach kodujących kanały jonowe (TPC1, TPC2 i TRPM4), które odgrywają ważną rolę w funkcjonowaniu serca i wątroby. W hodowanych w laboratorium mysich komórkach nerwowych ABE8e‑SpRY edytował docelową literę bardziej wydajnie, ale także zmieniał wiele pobliskich zasad. ABE9‑SpRY w zamian wprowadzał mniej zmian w ogóle, lecz odsetek „czystych” rezultatów — odczytów, w których zmieniono tylko zamierzoną literę bez dodatkowych mutacji w lokalnym regionie — był znacznie wyższy. Ten sam wzorzec zaobserwowano w embrionach mysich. Po wstrzyknięciu składników edytujących do zapłodnionych jaj ABE8e‑SpRY często konwertował niemal wszystkie kopie docelowego genu, ale z wieloma zmianami typu bystander. ABE9‑SpRY edytował mniej kopii ogółem, jednak tam, gdzie działał, sekwencja DNA była zazwyczaj skorygowana dokładnie tak, jak planowano.
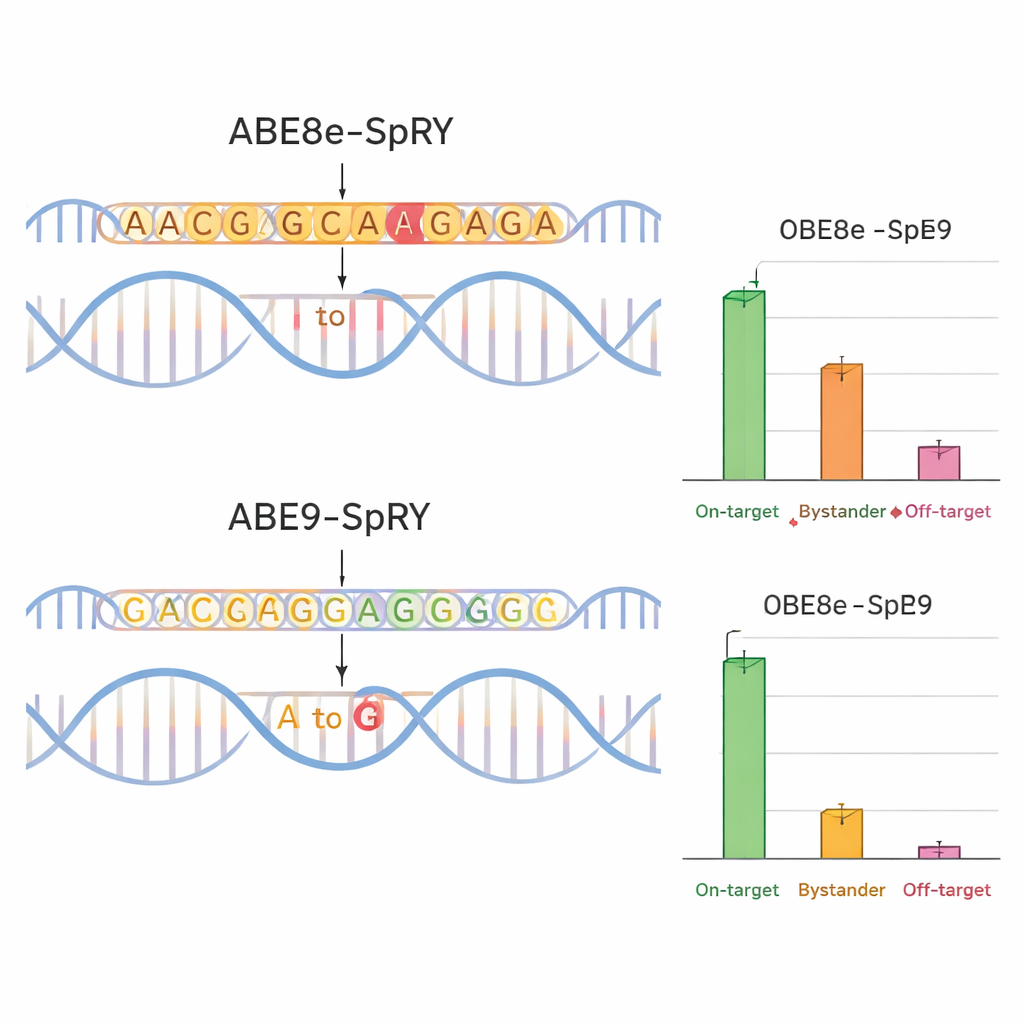
Czystsze edycje, mniej skutków ubocznych
Precyzja to nie tylko lokalne otoczenie DNA. Zespół sprawdził również, czy ich edytor modyfikuje odległe regiony genomu. Korzystając z predykcji komputerowych i selektywnego sekwencjonowania, zmierzyli zmiany poza celem w prawdopodobnych miejscach podobnych sekwencyjnie w embrionach mysich. ABE8e‑SpRY często wprowadzał niezamierzone zmiany A→G w tych lokalizacjach, czasem na zaskakująco wysokim poziomie. ABE9‑SpRY wykazywał znacznie mniej takich zdarzeń, z jedynie rzadkimi zmianami poza celem i bez wykrywalnej aktywności w specjalistycznym teście na uszkodzenia DNA niezależne od Cas9. Co ważne, gdy ABE9‑SpRY był używany pojedynczo — nie w testach zbiorczych — do wprowadzenia dwóch konkretnych mutacji u myszy, wygenerował wielu założycielskich osobników, w których pożądana edycja występowała na wysokim poziomie i była niezawodnie przekazywana potomstwu, ponownie przy minimalnych zmianach bystander lub niewielkich insercjach i delecjach.
Rozszerzanie precyzyjnej edycji na ludzkie komórki macierzyste
Ponieważ komórki macierzyste pochodzące od pacjentów są coraz częściej wykorzystywane do badania chorób i testowania leków, badacze przetestowali też ABE9‑SpRY w ludzkich indukowanych pluripotencjalnych komórkach macierzystych. Celowali w ludzką wersję genu TPC1 w pozycji odpowiadającej jednej z mysich. Korzystając z fluorescencyjnego markera do wzbogacenia komórek poddanych edycji, stwierdzili, że ABE8e‑SpRY osiągał wyższe surowe wskaźniki edycji, ale ponownie modyfikował wiele pobliskich zasad. ABE9‑SpRY edytował mniej alleli ogółem, lecz odsetek idealnie zmodyfikowanych odcinków — jednej zamierzonej zmiany i niczego więcej — był wyraźnie wyższy, z mniejszą liczbą zakłócających insercji lub delecji. W pracy z komórkami macierzystymi, gdzie pojedyncze klony są rozszerzane do szczegółowych badań, tego rodzaju „czysta” edycja jest zwykle bardziej wartościowa niż brutalna wydajność.
Dlaczego to ma znaczenie dla przyszłych badań nad chorobami
Dla naukowców próbujących zrozumieć, jak pojedyncza zmiana litery DNA prowadzi do choroby, dodatkowe niezamierzone mutacje mogą być głęboko mylące. To badanie pokazuje, że ABE9‑SpRY, choć nieco mniej wydajny w surowych wskaźnikach edycji, potrafi zapisać pojedyncze zmiany liter w genomach myszy i ludzkich komórek macierzystych z uderzającą dokładnością i szeroką elastycznością celowania. Czyni to z niego obiecujące narzędzie do tworzenia wiernych modeli zwierzęcych i komórkowych ludzkich chorób genetycznych, zwłaszcza w sytuacjach, gdzie nawet jedna przypadkowa mutacja mogłaby zmylić badania biologiczne lub storpedować potencjalną terapię.
Cytowanie: Ong, J.K., Bhunia, S., Hilbert, B. et al. ABE9 fused to SpRY Cas9 nickase enables precise generation of bystander free mouse models. Sci Rep 16, 7463 (2026). https://doi.org/10.1038/s41598-026-40642-z
Słowa kluczowe: edytowanie zasad adeniny, modele chorób CRISPR, genetyka myszy, efekty poza celem, edytowanie genów w hiPSC