Clear Sky Science · pl
Wariant chymotrypsyny C (CTRC) związany z zapaleniem trzustki p.R240Q selektywnie upośledza degradację trypsynogenu przez zakłócenie długozasięgowych oddziaływań elektrostatycznych
Dlaczego to ma znaczenie dla zdrowia trzustki
Przewlekłe zapalenie trzustki to bolesne, długotrwałe zapalenie tego narządu, które może prowadzić do cukrzycy, zaburzeń trawienia i znaczącego pogorszenia jakości życia. Badanie wyjaśnia, dlaczego niektórzy ludzie są bardziej podatni z powodu niewielkich dziedzicznych zmian w enzymach trawiennych. Skupiając się na pojedynczym wariancie genetycznym w jednym enzymie ochronnym, autorzy pokazują, jak subtelna zmiana molekularna może przesunąć równowagę od ochrony w kierunku uszkodzenia wewnątrz trzustki.
Wbudowany system zabezpieczeń w trawieniu
Nasza trzustka produkuje silne enzymy rozkładające białka, które zwykle są uwalniane do jelita w nieaktywnej formie. Jeden z tych proenzymów, trypsynogen, może czasem aktywować się za wcześnie, w samym narządzie. Gdy tak się dzieje, zaczyna trawić trzustkę od wewnątrz i wywołuje zapalenie. Aby temu zapobiegać, organizm stosuje mechanizmy ochronne, w tym białkowy inhibitor (SPINK1) oraz inny enzym trawienny, chymotrypsynę C (CTRC). CTRC pełni podwójną rolę: wspomaga aktywację enzymów trawiennych wtedy i tam, gdzie są potrzebne, ale też rozcina nadmiar trypsynogenu, zanim ten przekształci się w aktywną trypsynę i wyrządzi szkody. Osoby z odziedziczonymi osłabionymi formami CTRC mają udokumentowanie wyższe ryzyko przewlekłego zapalenia trzustki.
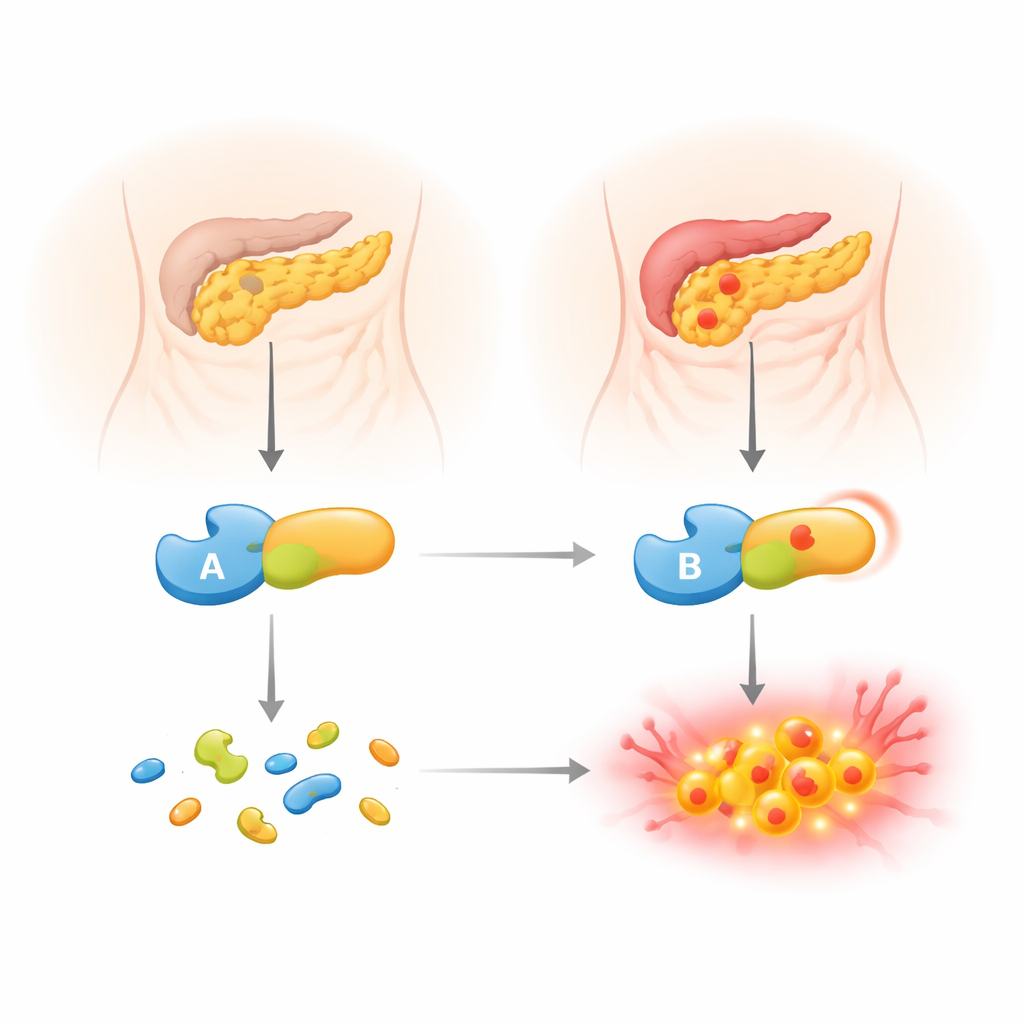
Rzadka zmiana genetyczna pod mikroskopem
Zespół skupił się na rzadkim wariancie CTRC nazwanym p.R240Q, znalezionym u chłopca ze Słowacji z dziecięcą postacią przewlekłego zapalenia trzustki oraz u jego chorego ojca. Wariant ten zmienia jeden budulec na powierzchni enzymu, zamieniając jednostkę dodatnio naładowaną na obojętną. Duże bazy genetyczne klasyfikują go jako prawdopodobnie niegroźny, lecz pojawiał się on u kilku młodych pacjentów z chorobą. Aby ustalić jego rzeczywisty wpływ, autorzy połączyli dane rodzinne z szczegółowymi eksperymentami laboratoryjnymi. Porównali wariantowy enzym bezpośrednio z normalnym CTRC, badając jego produkcję i wydzielanie przez komórki, aktywność na standardowych podłożach testowych oraz interakcję z trypsynogenem — kluczowym substratem, którym ma on sterować.
Normalna siła, lecz nietrafiony cel
Po pierwsze, badacze wykazali, że komórki syntetyzują i wydzielają enzym p.R240Q równie dobrze jak wersję normalną, więc wariant nie powoduje nieprawidłowego fałdowania ani upośledzenia produkcji. W testach probówkowych wykorzystujących mały syntetyczny peptyd i białko mleka (beta-kazeinę) wariant działał tak samo dobrze, a nawet nieco lepiej niż normalna CTRC. Oznacza to, że jego zdolność tnąca jest zachowana. Niespodzianka pojawiła się, gdy zbadano reakcję najistotniejszą dla zapalenia trzustki: rozkład ludzkiego kationowego trypsynogenu. W tym przypadku enzym z wariantem był znacznie mniej skuteczny — około cztery do pięciu razy wolniejszy w rozcinaniu trypsynogenu i znacznie słabszy w zapobieganiu jego autoaktywacji do trypsyny. W eksperymentach autoaktywacji potrzeba było znacznie więcej wariantowej CTRC, aby utrzymać poziomy trypsyny pod kontrolą w porównaniu z enzymem normalnym.
Zakłócony elektrostatyczny „tractor beam”
Aby wyjaśnić, dlaczego tak się dzieje, autorzy sięgnęli do modeli strukturalnych CTRC. Wokół rowka, w którym CTRC chwyta swoje substraty, znajduje się pierścień dodatniego ładunku elektrycznego utworzony przez kilka naładowanych aminokwasów, w tym miejsce zmienione w p.R240Q. Regiony trypsynogenu, które CTRC musi przeciąć, są silnie ujemne, więc dodatnio naładowany pierścień działa jak długozasięgowy „tractor beam”, kierując trypsynogen we właściwe położenie. Neutralizacja jednej z tych dodatnich pozycji przez wariant p.R240Q osłabia to oddziaływanie na odległość. Enzym wciąż jest „ostry”, ale uszkodzony system prowadzenia sprawia, że trypsynogen nie wiąże się tak efektywnie, więc mniej z niego jest bezpiecznie degradowane. Inne substraty, które w mniejszym stopniu polegają na tym wzorcu ładunku, są przetwarzane normalnie, co tłumaczy wysoce selektywny defekt zaobserwowany w eksperymentach.
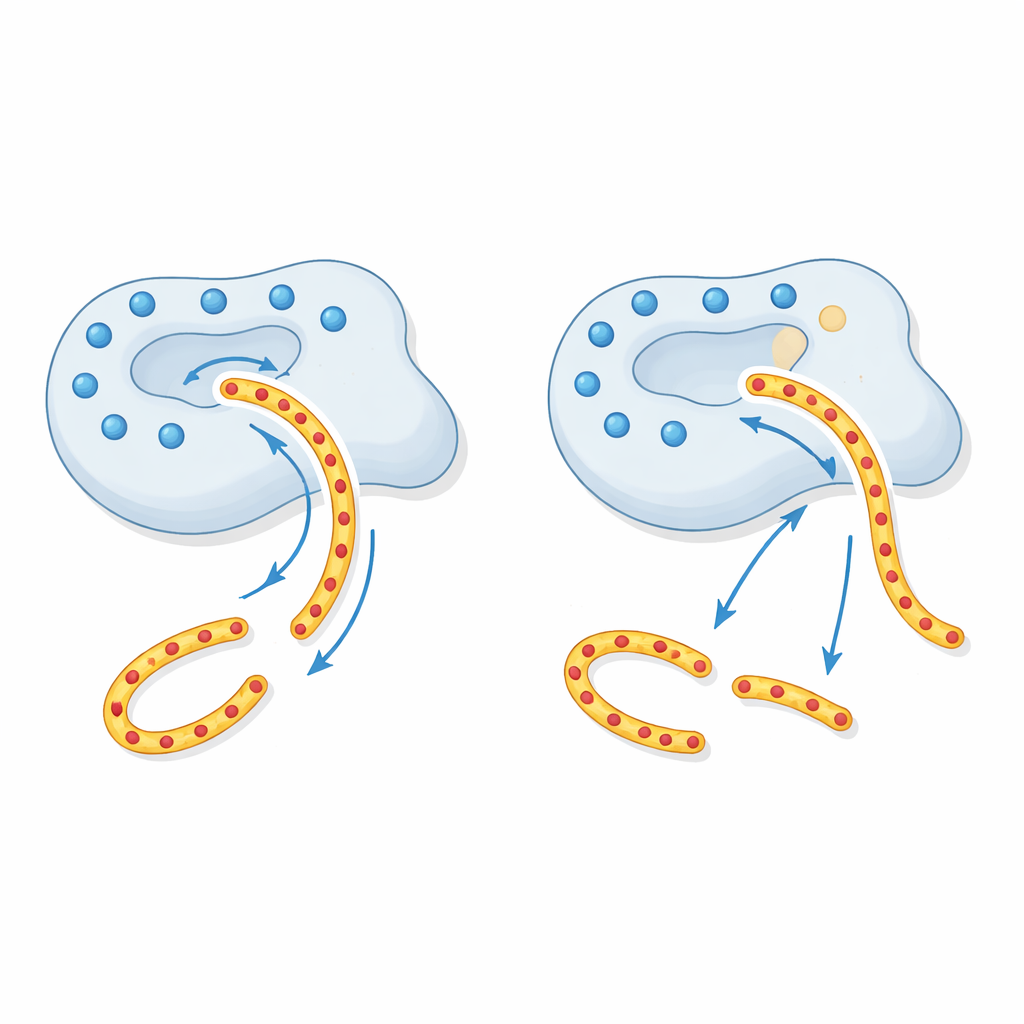
Co to oznacza dla pacjentów i diagnostyki
W obrazie klinicznym chłopiec i jego ojciec mieli również drugi uszkadzający wariant CTRC, a ojciec miał dodatkowe czynniki ryzyka związane ze stylem życia, takie jak intensywne spożycie alkoholu. Pasuje to do koncepcji, że przewlekłe zapalenie trzustki często wynika z nałożenia kilku uderzeń genetycznych i środowiskowych. Praca pokazuje, że wariant, który wydaje się nieszkodliwy dla powszechnych narzędzi predykcyjnych, może być wąsko niebezpieczny w specyficzny sposób. Dla badań genetycznych przesłanie jest jasne: przy ocenie, czy wariant CTRC zwiększa ryzyko zapalenia trzustki, naukowcy muszą przetestować jego wpływ na rzeczywisty cel — trypsynogen — a nie tylko na ogólne substraty laboratoryjne. W codziennym rozumieniu badanie ujawnia, jak drobna zmiana na „powierzchni prowadzącej” enzymu może cicho podkopać jedno z kluczowych zabezpieczeń trzustki, popychając podatne osoby w kierunku przewlekłego zapalenia.
Cytowanie: Nagy, Z.A., Sándor, M., Hegyi, E. et al. Pancreatitis-associated chymotrypsin C (CTRC) variant p.R240Q selectively impairs trypsinogen degradation through disruption of long-range electrostatic interactions. Sci Rep 16, 8937 (2026). https://doi.org/10.1038/s41598-026-40633-0
Słowa kluczowe: przewlekłe zapalenie trzustki, chymotrypsyna C, trypsynogen, wariant genetyczny, enzymy trawienne