Clear Sky Science · pl
Słabe powinowactwo przeciwciała przeciw B7-H3 klonu MJ18 do mysiej B7-H3 nie wywołuje regresji guza
Dlaczego ma to znaczenie dla badań nad rakiem
Immunoterapia nowotworów często opiera się na przeciwciałach — laboratoryjnie wytworzonych białkach zaprojektowanych tak, by przyczepiać się do komórek nowotworowych i pomagać układowi odpornościowemu je niszczyć. Obiecującym celem jest cząsteczka zwana B7-H3, obecna w dużych ilościach w wielu ludzkich nowotworach, a rzadko występująca w zdrowych tkankach. Artykuł ten dokładnie przygląda się powszechnie stosowanemu przeciwciału badawczemu MJ18, które miało blokować B7-H3 w badaniach na myszach. Autorzy wykazują, że MJ18 ledwo wiąże się ze swoim zamierzonym celem i nie hamuje wzrostu guza, co rodzi wątpliwości co do interpretacji wcześniejszych doświadczeń zwierzęcych z użyciem tego narzędzia.
Obietnica „flag” nowotworu na komórkach guza
B7-H3 zyskał duże zainteresowanie, ponieważ działa jak molekularna tarcza: guzy bogate w to białko mają zazwyczaj mniej agresywnych komórek odpornościowych w swoim wnętrzu i są powiązane z gorszymi wynikami u pacjentów. W kilku modelach mysich usunięcie genu kodującego B7-H3 w komórkach nowotworowych uwalnia silniejszy atak immunologiczny i może powodować kurczenie się lub znikanie guzów. Obserwacje te pobudziły prace nad lekami, inżynierią komórek odpornościowych oraz koniugatami przeciwciało–lek skierowanymi przeciw B7-H3 w nowotworach ludzkich. Jednak dokładny sposób, w jaki B7-H3 tłumi odporność — a nawet który receptor na komórkach odpornościowych z nim współdziała — pozostaje niepewny, zwłaszcza że mysia i ludzka wersja B7-H3 różnią się strukturalnie.
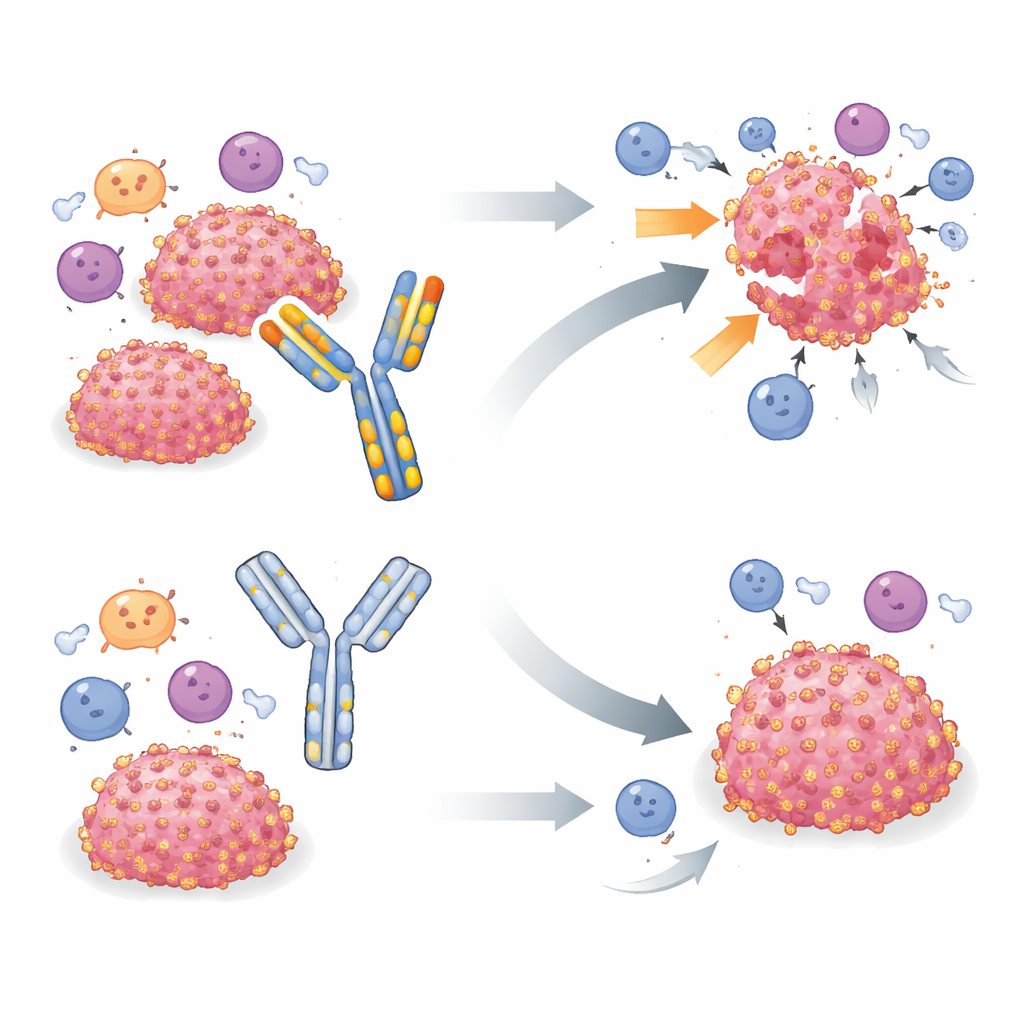
Powszechnie stosowane narzędzie pod lupą
Do badania B7-H3 in vivo wiele grup polegało na jednym przeciwciele pochodzenia szczurzego o nazwie MJ18, które miało rozpoznawać mysie B7-H3 i blokować jego immunosupresyjne działanie. Wcześniejsze prace z MJ18 w różnych modelach chorobowych, w tym nowotworowych, często raportowały spowolnienie wzrostu guzów i lepsze przeżycie. Zespół autorów początkowo testował MJ18 w mysim modelu rabdomiosarcomy, dziecięcego nowotworu tkanki miękkiej, gdzie B7-H3 już wcześniej wskazywano jako istotny mechanizm ucieczki. Gdy MJ18 nie poprawiło kontroli guza, badacze rozszerzyli testy na dwa inne typy nowotworów pozytywnych pod względem B7-H3 — trzustkowy i gruczołu sutkowego — które wyraźnie reagują na usunięcie genu B7-H3. We wszystkich trzech modelach wyeliminowanie B7-H3 w komórkach nowotworowych zdecydowanie opóźniało lub usuwało guzy, ale leczenie myszy MJ18 w dawkach i schematach podobnych do publikowanych nie miało wykrywalnego wpływu na wzrost guza ani przeżywalność.
Sprawdzanie, czy MJ18 naprawdę trafia w cel
Autorzy postawili podstawowe pytanie, które zaskakująco nigdy nie było rygorystycznie zbadane: czy MJ18 rzeczywiście wiąże mysie B7-H3 i jak silnie? Używając cytometrii przepływowej porównali MJ18 z innym przeciwciałem, EPNCIR122, znanym z wykrywania B7-H3. Na kilku mysich liniach komórek nowotworowych EPNCIR122 dawało wyraźny sygnał, który znikał po usunięciu genu B7-H3, potwierdzając jego specyficzność. MJ18 natomiast nie wykazało przekonującego wiązania nawet przy wysokich stężeniach. Przy badaniu komórek odpornościowych ze śledziony MJ18 wiązało się, lecz wzór nie odpowiadał rozkładowi B7-H3, a EPNCIR122 nie wykrywało w ogóle B7-H3 na tych komórkach, co sugeruje, że MJ18 przyczepiało się do czegoś innego.
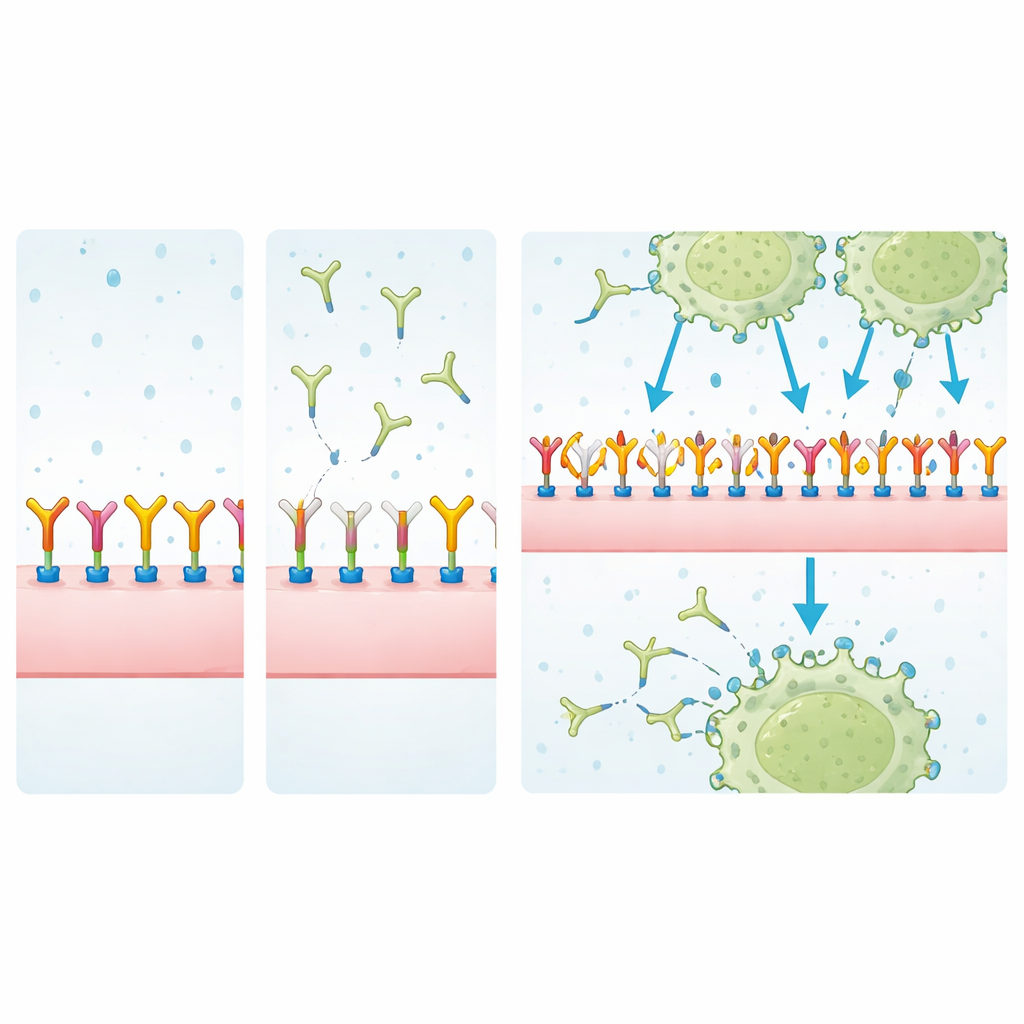
Dociekanie, z czym się wiąże
Aby ustalić, co MJ18 faktycznie rozpoznaje, badacze wyizolowali białka z powierzchni komórek przy użyciu MJ18 lub EPNCIR122 i przeanalizowali je metodą spektrometrii masowej, filtrując jednocześnie typowe zanieczyszczenia tła. W komórkach nowotworowych EPNCIR122 silnie wzbogaciło B7-H3 ponad innymi białkami, potwierdzając, że jest to wysoce specyficzny odczynnik. MJ18 natomiast wyciągało mieszankę białek, w której B7-H3 pojawiało się tylko słabo i na poziomach podobnych do niespecyficznych wiązań. Pomiar za pomocą rezonansu plazmonów powierzchniowych, czułej techniki ilościowego badania interakcji molekularnych, uwypuklił sprawę: powinowactwo MJ18 do mysiej B7-H3 było około 7 000 razy słabsze niż EPNCIR122 — daleko poniżej typowego poziomu dla przeciwciał terapeutycznych.
Kiedy przeciwciała są „złapane” przez niewłaściwe komórki
Historia nie zakończyła się na słabym wiązaniu. W komórkach śledziony dodatkowe testy wykazały, że MJ18 i podobne przeciwciała szczurzego pochodzenia były rozpoznawane przez mysie receptory Fc — cząsteczki na komórkach odpornościowych, które naturalnie wiążą ogon przeciwciała. Zablokowanie tych receptorów znacząco zmniejszyło sygnał MJ18, co sugeruje, że duża część pozornego wiązania wynikała z tego, że komórki odpornościowe „chwytały” samo przeciwciało, zamiast MJ18 celować w specyficzne białko powierzchniowe. Próby zidentyfikowania unikatowego partnera białkowego MJ18 na komórkach odpornościowych ujawniły jedynie kandydatów na poziomach nierozróżnialnych od szumu tła. Łącznie dane sugerują, że MJ18 zachowuje się w dużej mierze jak przeciwciało o niskim powinowactwie i niespecyficzne, którego interakcje są zdominowane przez angażowanie receptorów Fc, a nie precyzyjne rozpoznawanie B7-H3.
Co to oznacza na przyszłość
Dla niespecjalistów przesłanie jest proste: choć B7-H3 pozostaje przekonującym celem w wielu nowotworach, przeciwciało MJ18 nie jest niezawodną strzałą. Wiaże się z mysim B7-H3 tylko słabo i nie odtwarza silnej kontroli guza zaobserwowanej po usunięciu genu B7-H3. Wcześniejsze badania na myszach, które opisywały dramatyczne korzyści z MJ18, mogły zatem odzwierciedlać inne efekty — na przykład sposób, w jaki ogon przeciwciała angażował receptory komórek odpornościowych — zamiast rzeczywistej blokady B7-H3. Autorzy argumentują, że w tej dziedzinie pilnie potrzeba dobrze zwalidowanych, wysokoprzewiązywalnych przeciwciał przeciw mysiej B7-H3 oraz że badacze powinni rutynowo potwierdzać specyficzność i siłę takich narzędzi. Tylko z wiarygodnymi odczynnikami wnioski z modeli zwierzęcych mogą być zaufane przy opracowywaniu kolejnej generacji terapii skierowanych przeciw B7-H3 dla pacjentów.
Cytowanie: Gulyás, D., Nammor, T., Frizzell, J. et al. Low-affinity binding of anti-B7-H3 clone MJ18 to murine B7-H3 fails to induce tumor regression. Sci Rep 16, 9519 (2026). https://doi.org/10.1038/s41598-026-40628-x
Słowa kluczowe: B7-H3, immunoterapia nowotworów, walidacja przeciwciał, punkty kontroli układu odpornościowego, modele nowotworowe