Clear Sky Science · pl
Duże zróżnicowanie całkowitej i allelicznej ekspresji transkryptów niezależne od mutacji chorobowej
Dlaczego to ma znaczenie dla osób z mukowiscydozą
Mukowiscydoza (CF) często bywa przedstawiana jako typowe „schorzenie jednogenowe”, jednak osoby noszące dokładnie tę samą mutację mogą mieć diametralnie różne objawy i przebieg życia. To badanie stawia pozornie proste, lecz dalekosiężne pytanie: nawet jeśli wadliwy gen jest taki sam, czy pacjenci faktycznie wytwarzają różne ilości jego przekazu (mRNA) i czy może to wyjaśniać, dlaczego choroba przebiega tak różnie — oraz jak dobrze reagują na nowoczesne leki?
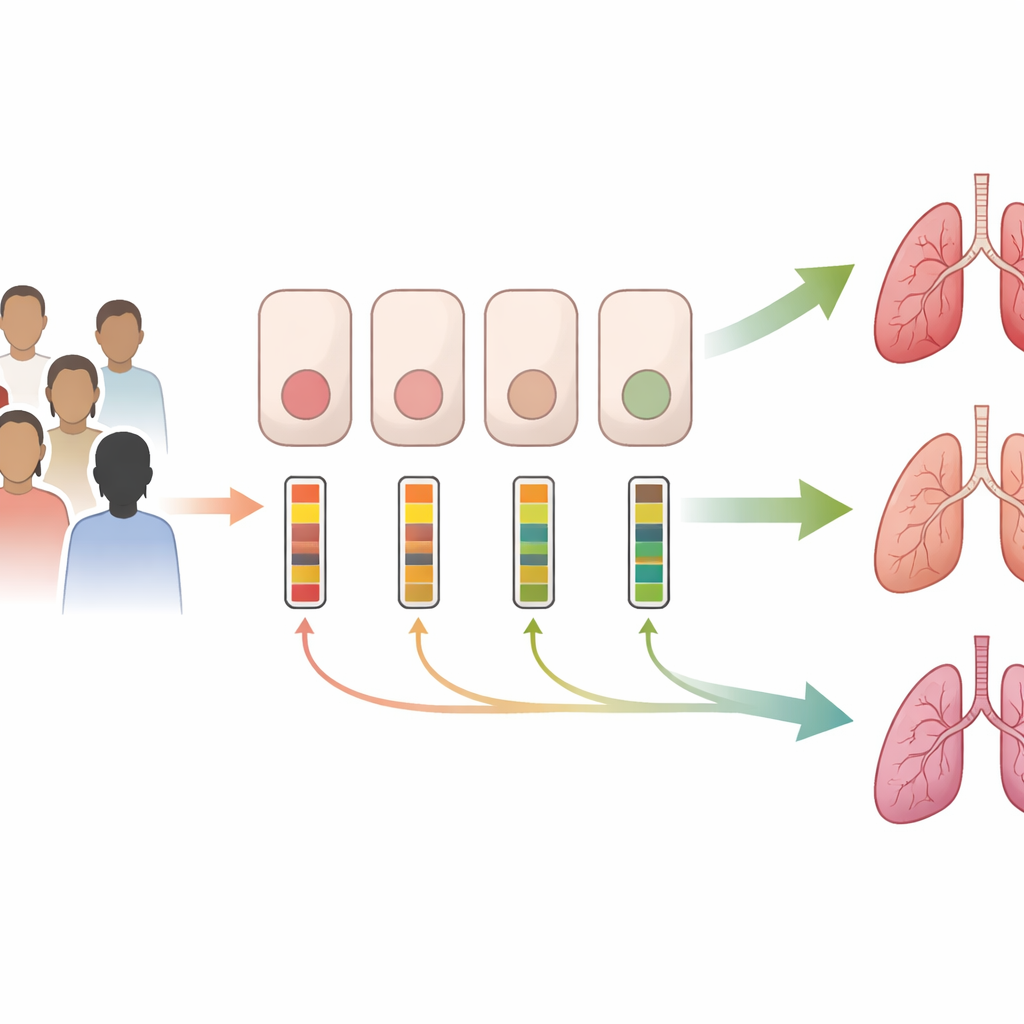
Różni pacjenci, ta sama mutacja, bardzo różna aktywność genu
Naukowcy skupili się na genie CFTR, którego wadliwe wersje powodują CF. Zamiast analizować jedynie zmiany w DNA, zmierzyli, ile mRNA CFTR — roboczego „scenariusza” genu do produkcji białka — występuje w komórkach dróg oddechowych zebranych delikatnym wymazem z nosa. W ciągu pięciu lat zebrali próbki od dzieci i dorosłych chorych na CF oraz niewielkiej grupy osób zdrowych. Wielu pacjentów miało powszechną mutację F508del, albo w obu kopiach genu, albo w jednej kopii w połączeniu z inną wadą. Nawet w obrębie tych grup poziomy mRNA CFTR różniły się bardzo — wielokrotnie między osobami. Ochotnicy bez CF również wykazywali duże zróżnicowanie, co sugeruje, że ekspresja CFTR naturalnie różni się między osobami i że ta wrodzona zmienność przenosi się także na osoby z CF.
Gdy dwie kopie genu nie pracują równomiernie
U pacjentów z dwiema różnymi mutacjami CFTR — zazwyczaj F508del i innym wariantem — zespół poszedł krok dalej. Przy użyciu wysoce specyficznych testów molekularnych policzyli, ile mRNA pochodziło z każdej kopii genu osobno. Zamiast oczekiwanego mniej więcej po połowie z każdej alleli, często stwierdzali silne odchylenie, czyli „przechylenie”: allel niebędący F508del zwykle produkował znacznie więcej mRNA niż allel F508del. U niektórych pacjentów kopia z F508del wnosiła jedynie niewielką część całkowitej wiadomości CFTR. Ta nierównomierność występowała nawet wśród osób mających ten sam zestaw mutacji, co sugeruje, że dodatkowe zmiany w pobliżu genu lub szersze mechanizmy regulacyjne wpływają na to, ile transkryptu produkuje każda kopia.
Badania na komórkach potwierdzają wrodzoną zmienność
Aby wyeliminować część rzeczywistych komplikacji związanych z infekcjami i stanem zapalnym w drogach oddechowych, naukowcy hodowali też w laboratorium komórki nosowe i oskrzelowe pobrane od pacjentów. Tam również zaobserwowali duże różnice w całkowitym poziomie mRNA CFTR między osobami o tym samym składzie genetycznym. W części hodowanych komórek od pacjentów z heterozygotycznymi mutacjami złożonymi, ekspresja obu alleli była bliższa równowadze niż w świeżych próbkach z nosa, podkreślając, że warunki hodowli i środowisko organizmu mogą zmieniać aktywność genów. Razem te obserwacje wspierają pogląd, że zarówno całkowita produkcja CFTR, jak i względny wkład każdej alleli są cechami elastycznymi, a nie w pełni zdeterminowanymi jedynie przez sekwencję głównych mutacji DNA.
Nowoczesne leki na CF przesuwają równowagę między kopiami genu
W badaniu przeanalizowano też niewielką grupę pacjentów przed i po rozpoczęciu powszechnie stosowanych terapii „modulatorami” CFTR, w tym potrójnego zestawu elexacaftor–tezacaftor–ivacaftor oraz terapii dwuskładnikowej. Zaskakująco, leki te nie podnosiły ani nie obniżały konsekwentnie całkowitej ilości mRNA CFTR w komórkach nosowych. Zamiast tego przesuwały, która allela wnosi większy udział. Po leczeniu allel F508del często produkował większy odsetek całkowitego transkryptu CFTR, w niektórych przypadkach stając się dominującym źródłem. Zmiana tej równowagi allelicznej zachodziła równolegle z oczekiwanymi poprawami klinicznymi, takimi jak lepsza funkcja płuc i niższe stężenie soli w pocie, co sugeruje, że zwiększenie produkcji przekazu z uratowanego białka mutantowego może uzupełniać znane efekty tych leków na fałdowanie i funkcję białka.
Co to oznacza dla spersonalizowanego leczenia
Dla osób żyjących z mukowiscydozą wyniki te podkreślają, że mutacje w DNA to tylko część historii. To, ile mRNA CFTR produkuje dana osoba — i jak ta produkcja rozkłada się między dwiema kopiami genu — może znacznie się różnić i nie da się tego w pełni przewidzieć tylko na podstawie typu mutacji. Ta zmienność może pomagać wyjaśniać, dlaczego pacjenci o tym samym genotypie doświadczają różnego nasilenia choroby i różnie reagują na terapie. Sugeruje to również, że przyszłe podejścia spersonalizowane mogą wymagać pomiaru nie tylko tego, jakie mutacje CFTR nosi pacjent, ale też jak aktywnie każda kopia genu jest używana, zarówno przed leczeniem, jak i w jego trakcie. Zrozumienie i ostateczne kontrolowanie tej ukrytej warstwy aktywności genowej mogłoby pomóc w precyzyjnym dostrojeniu terapii dla CF i innych chorób jednogenowych.
Cytowanie: Freyberg, M., Bewig, M., Bampi, G.B. et al. Large variations in total and allele-specific transcript expression in a disease mutation-independent manner. Sci Rep 16, 7831 (2026). https://doi.org/10.1038/s41598-026-40624-1
Słowa kluczowe: mukowiscydoza, CFTR, ekspresja genów, nierównowaga alleliczna, modulatory CFTR