Clear Sky Science · pl
Stabilność strukturalna symetrycznych przeciwciał bispecyficznych: studium przypadku pokazujące potencjalne osłabienie w pobliżu regionów łącznikowych
Dlaczego drobne łączniki w nowych lekach przeciwnowotworowych mają znaczenie
Wiele z obecnie najbardziej obiecujących leków przeciwnowotworowych to przeciwciała zaprojektowane tak, by jednocześnie wiązać dwa różne cele, pomagając komórkom odpornościowym odnaleźć guzy. Te tzw. „bispecyficzne” przeciwciała mogą być skuteczniejsze niż starsze leki ukierunkowane na pojedynczy cel, ale są też molekułami bardziej złożonymi. W tym badaniu przyjrzano się z bliska jednemu z takich eksperymentalnych leków i postawiono proste, lecz istotne pytanie: czy drobne białkowe łączniki łączące jego części pozostają nienaruszone podczas rzeczywistych warunków produkcji i przechowywania, czy też stają się słabymi punktami?
Budowanie „dwuręcznego” przeciwciała
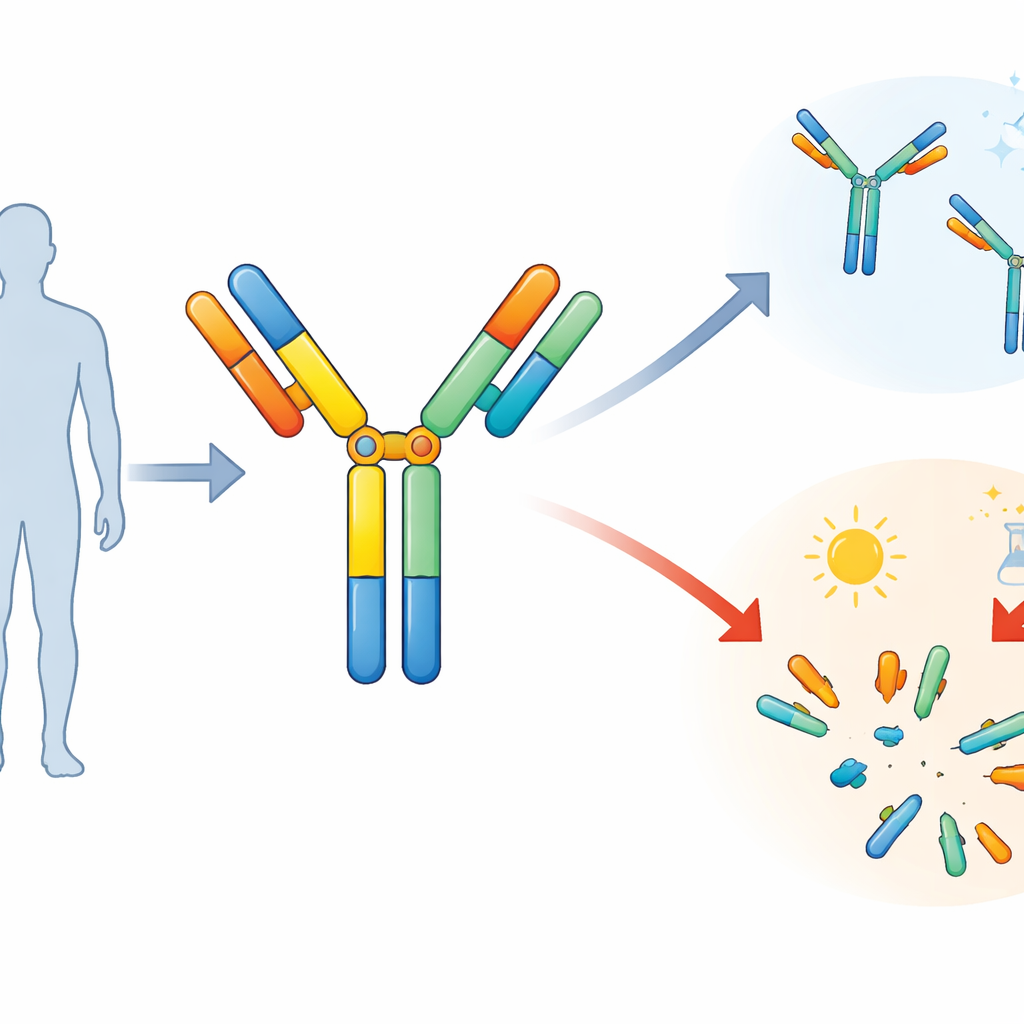
Naukowcy skupili się na symetrycznym przeciwciele bispecyficznym zaprojektowanym do wiązania markera nowotworowego zwanego HER2 oraz receptora komórek odpornościowych CD3. Symetryczne w tym kontekście oznacza, że cząsteczka jest zbudowana w zbalansowany, lustrzany sposób, z czterema „chwytnymi” końcówkami zamiast zwyczajowych dwóch. Aby to osiągnąć, zespół zszył dobrze znane elementy przeciwciała krótkimi odcinkami elastycznego białka zwanymi łącznikami. Te łączniki działają jak zawiasy lub dystanse, pozwalając regionom wiążącym przyjąć odpowiednie położenie, by lek mógł jednocześnie pochwycić komórkę nowotworową i komórkę T.
Słabe punkty pod wpływem ciepła i ciężkich warunków
Aby sprawdzić, jak solidna jest ta konstrukcja, zespół świadomie ją obciążył. Podgrzewali próbki przez tygodnie i umieszczali je w roztworach o różnym stopniu kwasowości (pH) oraz zasoleniu, naśladując warunki, jakich molekuła może doświadczać podczas oczyszczania, formułowania lub długotrwałego przechowywania. Przy użyciu techniki rozdzielającej cząsteczki wg rozmiaru obserwowali, jak udział nienaruszonego przeciwciała stopniowo maleje, a ilość mniejszych fragmentów rośnie, szczególnie przy wyższym pH. Samo sole miały jedynie umiarkowany wpływ, ale w połączeniu z wysokim pH fragmentacja wzrastała gwałtownie, co sygnalizowało, że niektóre części cząsteczki ulegają rozdzieleniu.
Zbliżenie na miejsca pęknięć
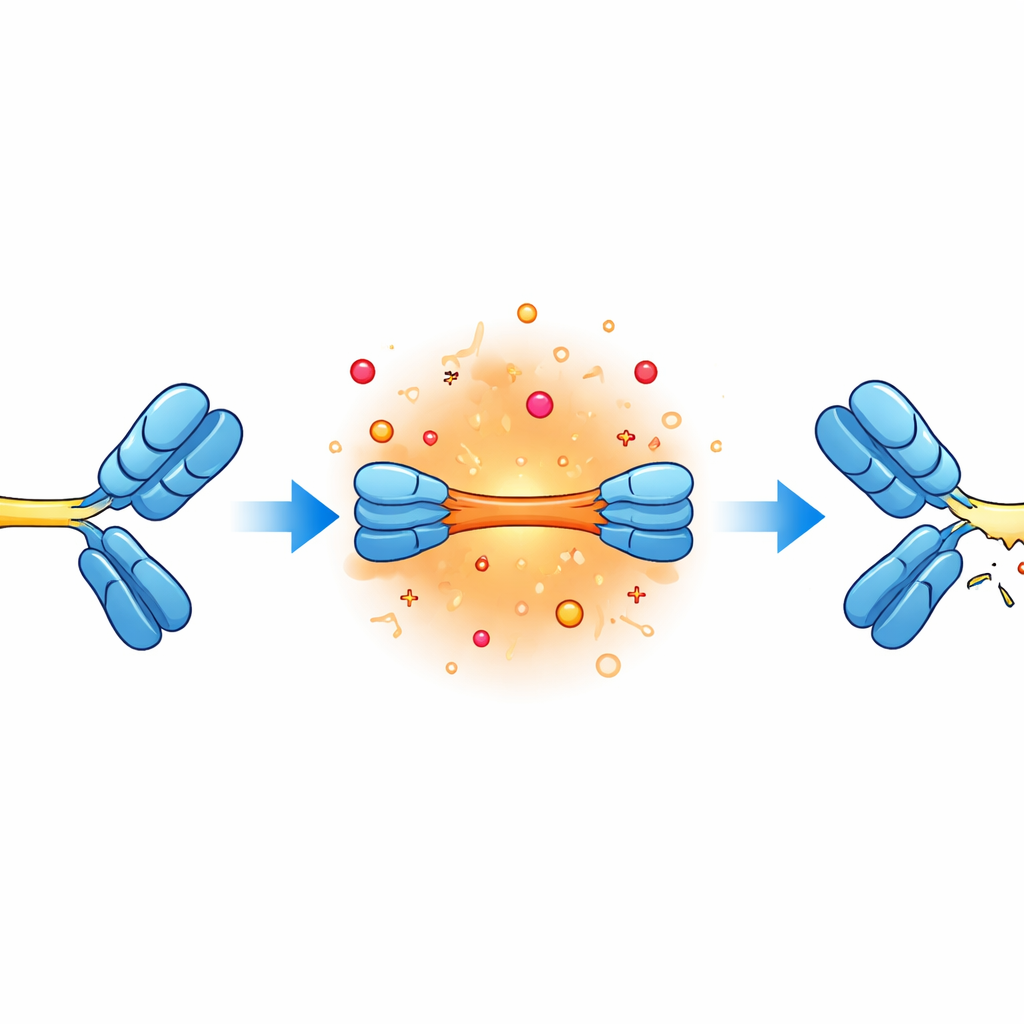
Następnym krokiem było ustalenie dokładnych miejsc pęknięć. Badacze zebrali różne fragmenty i przeanalizowali ich masy przy użyciu wysokorozdzielczej spektrometrii mas, w istocie ważąc i rekonstruując kawałki niczym molekularne puzzle. Wykazało to, że dwa konkretne łączniki — krótkie sekwencje często określane jako G4S i G4 — były szczególnie podatne na przecięcia. Te elastyczne łączniki leżą pomiędzy głównymi ramionami przeciwciała a dodanymi segmentami wiążącymi. W warunkach zasadowych, zasolonych i podwyższonej temperatury wiązania peptydowe w tych regionach były przecinane krok po kroku, tworząc serię przewidywalnych fragmentów wzdłuż łańcuchów łączników.
Nie tylko łączniki: inne wiązania zagrożone
Analiza wykazała także uszkodzenia w innych wrażliwych miejscach. Niektóre pęknięcia występowały w pobliżu określonych reszt asparaginy, które są znane z powolnych chemicznych przemian przy wysokim pH, co w końcu może prowadzić do przecięcia łańcucha. Dodatkowo zaburzone zostały wiązania obejmujące zawierające siarkę reszty cysteiny, które zwykle pomagają utrzymać razem ciężkie i lekkie łańcuchy przeciwciała. Doprowadziło to do odczepienia fragmentów łańcucha lekkiego i powstania różnych chemicznie zmodyfikowanych wariantów. Chociaż tego rodzaju zmiany są znane z badań nad standardowymi przeciwciałami monoklonalnymi, ich pojawienie się w pobliżu regionów łącznikowych sugeruje, że dodatkowa elastyczność konstrukcji bispecyficznej może narażać sąsiednie wiązania na większy stres.
Wnioski projektowe dla bezpieczniejszych i trwalszych leków
Dla osób niebędących specjalistami główny wniosek jest taki, że nadanie przeciwciałom większej wszechstronności przez dodanie dodatkowych ramion wiążących to nie tylko kwestia sprytnego inżynierowania genetycznego; wymaga też starannej uwagi wobec małych regionów łącznikowych, które wszystko spinają. W tym przypadku powszechnie stosowane elastyczne łączniki łączące funkcjonalne części przeciwciała bispecyficznego okazały się słabymi punktami strukturalnymi w realistycznych warunkach obciążenia. Konkluzja badania nie brzmi, że przeciwciała bispecyficzne są niebezpieczne, lecz że ich stabilność w dużym stopniu zależy od tego, jak łączniki są zbudowane i rozmieszczone. Przyszłe projekty będą musiały optymalizować długość łączników, ich sekwencję i lokalne otoczenie, aby następna generacja terapii przeciwciałowych mogła w pełni zrealizować swój potencjał kliniczny bez rozpadania się podczas produkcji, przechowywania czy leczenia.
Cytowanie: Ingavat, N., Kok, Y.J., Dzulkiflie, N. et al. Structural stability of symmetric bispecific antibodies: a case study showing potential compromise near linker regions. Sci Rep 16, 9715 (2026). https://doi.org/10.1038/s41598-026-40607-2
Słowa kluczowe: przeciwciała bispecyficzne, stabilność białek, projektowanie łączników, inżynieria przeciwciał, rozwój biofarmaceutyków