Clear Sky Science · pl
Analiza teoretyczna niskomocowego optogenetycznego tłumienia potencjałów czynnościowych w ludzkich kardiomiocytach komór komorowych z ekspresją kanałorodopsyn selektywnych dla potasu
Łagodniejszy sposób na uspokojenie przyspieszonego serca za pomocą światła
Szybkie, chaotyczne rytmy serca mogą prowadzić do omdleń, udaru lub nagłej śmierci. Obecne terapie — silne leki, wszczepiane defibrylatory czy wysokonapięciowe wstrząsy — mogą ratować życie, ale bywają bolesne i niedokładne. W tej pracy badane jest bardzo inne podejście: użycie słabych błysków światła i specjalnie zaprojektowanych białek, aby delikatnie nakierować komórki serca z powrotem na bezpieczny, stabilny rytm, przy zużyciu energii znacznie mniejszym niż w obecnych metodach.
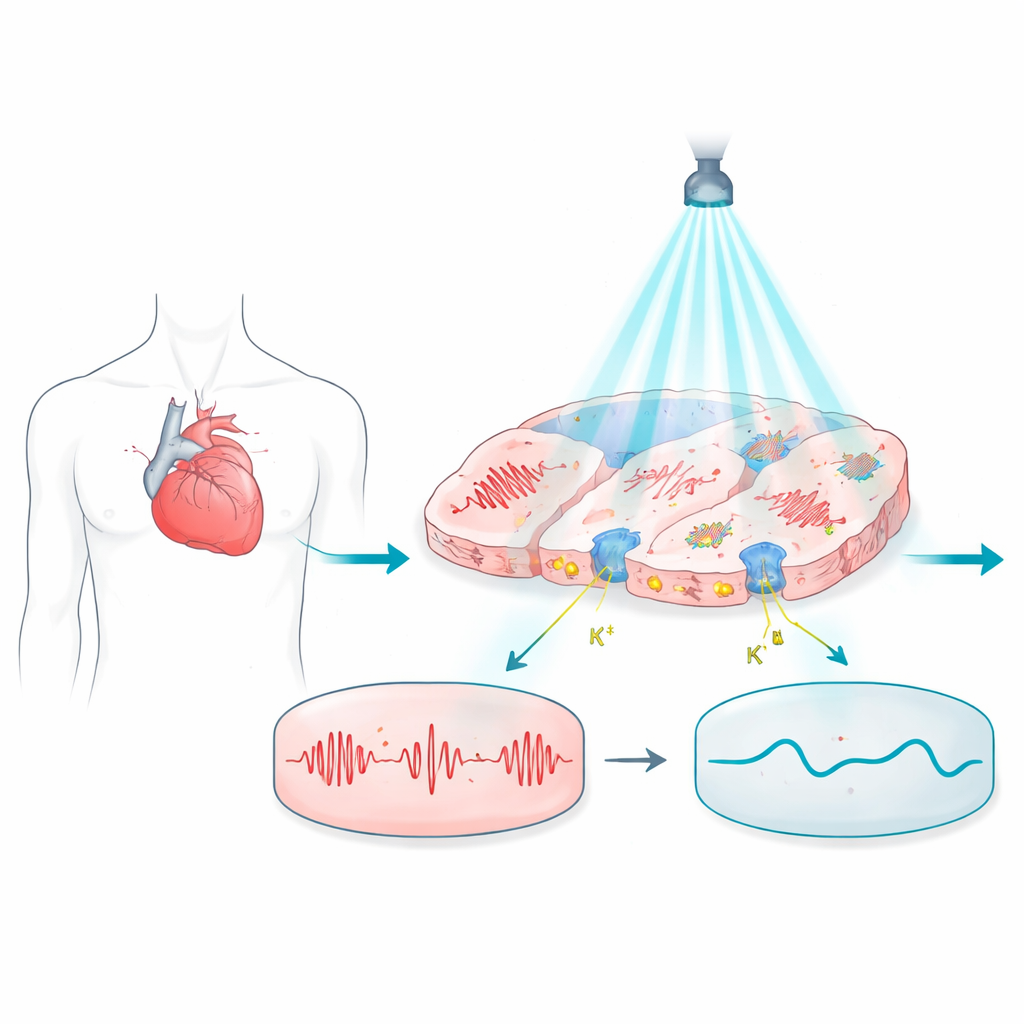
Oświetlając problematyczne uderzenia serca
Praca opiera się na optogenetyce, technice, w której komórki wyposażane są w białka wrażliwe na światło, dzięki czemu ich aktywność elektryczna może być kontrolowana za pomocą błysków światła. W sercu te białka mogą w teorii zastąpić metalowe elektrody, oferując kontrolę bez kontaktu i bez bólu. Jednak większość dotychczas używanych białek aktywowanych światłem ma tendencję do przesuwania napięcia komórkowego w kierunku depolaryzacji, ku stanowi pobudzenia, co utrudnia utrzymanie komórek w spokojnym spoczynku lub precyzyjne regulowanie długości każdego bicia serca. Ogranicza to ich użyteczność w bezpiecznym wyłączaniu niebezpiecznych rytmów lub korygowaniu zaburzeń elektrycznych zależnych od subtelnego timingu.
Nowe przełączniki świetlne dopasowane do „ustawienia spoczynkowego” serca
Niedawno odkryte białka zwane kanałorodopsynami selektywnymi dla potasu, w tym WiChR i HcKCR1, obiecują naprawić tę niezgodność. W przeciwieństwie do starszych białek, które przepuszczają mieszankę jonów, kanały te silnie preferują potas i naturalnie ściągają napięcie komórkowe w kierunku tej samej ujemnej wartości, którą przyjmuje w spoczynku. Autorzy stworzyli szczegółowe modele komputerowe ludzkich komór kardiomiocytów komorowych z ekspresją tych nowszych kanałów i porównali je z dwoma dobrze znanymi, bardziej pobudzającymi opsynami, ChR2(H134R) i ChRmine. Symulując reakcje tych komórek na różne barwy i natężenia światła, mogli bezpiecznie zbadać warunki, których testowanie w żywych sercach byłoby trudne lub czasochłonne.
Łagodne światło, silna kontrola
Symulacje pokazują, że kanały selektywne dla potasu zapewniają znacznie bardziej ekonomiczną i stabilną kontrolę. W szczególności WiChR może całkowicie zahamować potencjały czynnościowe — krótkie skoki elektryczne wyzwalające każde uderzenie serca — przy natężeniach światła setki do tysiące razy mniejszych niż te potrzebne dla wielu wcześniejszych narzędzi. Pod ciągłym światłem WiChR i HcKCR1 utrzymywały napięcie komórkowe blisko normalnego poziomu spoczynkowego, skutecznie trzymając komórkę w cichym, bezpiecznym stanie. Dla porównania, ChR2 i ChRmine miały skłonność do przesuwania napięcia w kierunku wartości bardziej dodatnich, czasem blokując aktywność, lecz dopiero po wprowadzeniu komórki w zestresowany, nadpobudliwy stan. WiChR dobrze sprawdzał się także przy krótkich impulsach światła, niezawodnie zapobiegając skokom elektrycznym z bicia na bicie, co sugeruje, że mógłby nadążać za szybkimi rytmami serca bez przegrzewania tkanki czy marnowania energii.
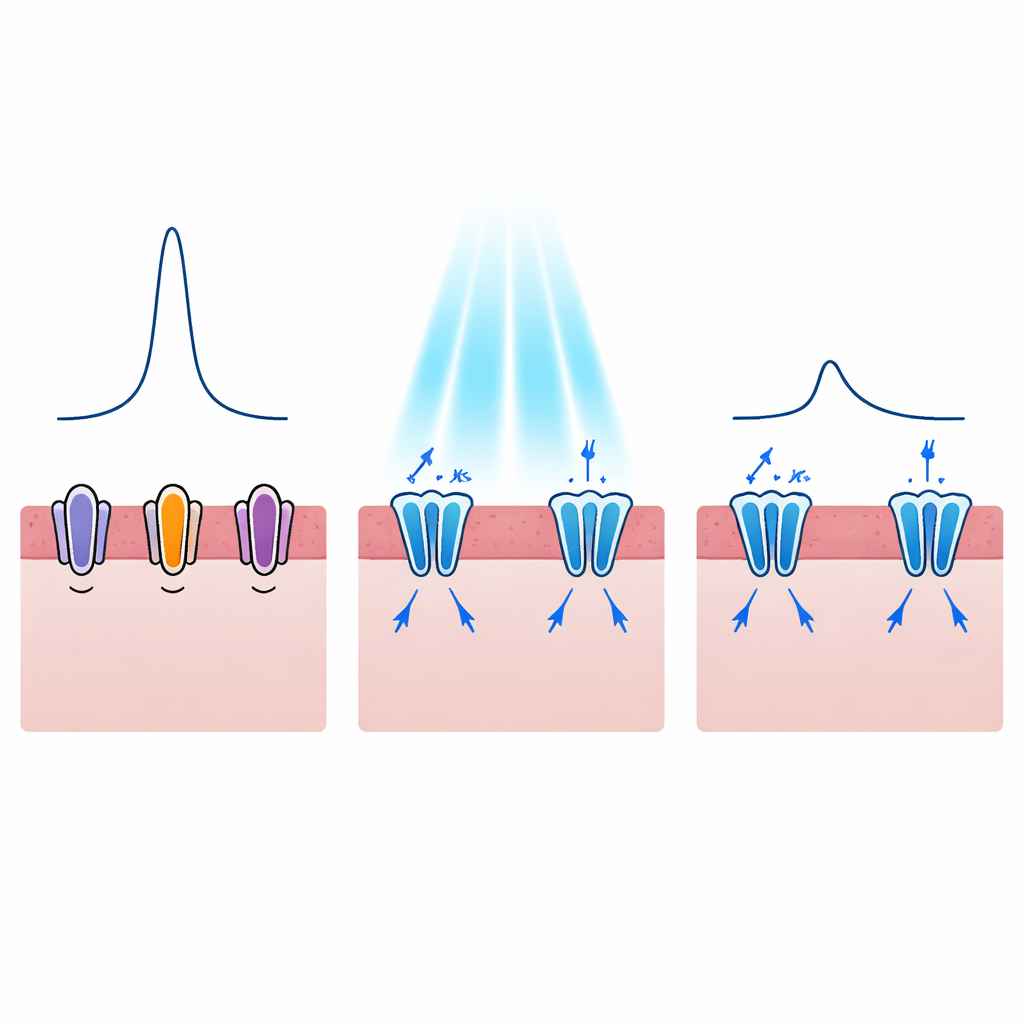
Przekształcanie każdego uderzenia serca, a nie tylko jego zatrzymywanie
Niebiezpieczne arytmie często wiążą się nie tylko z tym, czy komórka serca się wyzwala, lecz także z tym, jak długo pozostaje pobudzona. W zaburzeniach takich jak zespół długiego QT impuls elektryczny każdego bicia jest wydłużony, co zwiększa ryzyko przejścia w śmiertelne rytmy. Autorzy zatem zastanawiali się, czy aktywowane światłem kanały potasowe mogłyby skrócić ten impuls w kontrolowany sposób. Ich modele wykazały, że włączenie WiChR lub HcKCR1 podczas fazy plateau potencjału czynnościowego generowało silne prądy potasowe wypływowe, które szybciej przyciągały napięcie z powrotem w dół. W miarę wzrostu poziomów światła czas trwania impulsu elektrycznego skracał się z około 300 milisekund do w przybliżeniu połowy tej wartości, a efekt ten dało się uzyskać nawet przy bardzo krótkich błyskach światła. WiChR miał tendencję do wywoływania dłużej trwających okresów ciszy, podczas gdy HcKCR1 oferował szybszy powrót do normalnego stanu po wyłączeniu światła, co sugeruje różne potencjalne zastosowania kliniczne.
Od modeli komputerowych do przyszłych terapii
Podsumowując, badanie stwierdza, że selektywne dla potasu kanały aktywowane światłem, zwłaszcza WiChR, są obiecującymi narzędziami do łagodnej, niskomocowej kontroli serca. Mogą zarówno uciszyć wymykającą się spod kontroli aktywność elektryczną, jak i skracać nadmiernie długie uderzenia serca, jednocześnie utrzymując napięcie komórkowe blisko jego naturalnego poziomu spoczynkowego. Chociaż wyniki pochodzą ze szczegółowych symulacji pojedynczych komórek, a nie z eksperymentów na całym sercu, dostarczają ilościowych wskazówek dotyczących tego, ile światła może być potrzebne, kiedy powinno być stosowane i które warianty białek najlepiej nadają się do różnych celów. W dłuższej perspektywie linia tych badań wskazuje na przyszłość, w której kardiolodzy mogliby używać precyzyjnie dostrojonych wiązek światła, zamiast bolesnych wstrząsów, do zapobiegania lub zatrzymywania zagrażających życiu arytmii.
Cytowanie: Dixit, N., Pyari, G. & Roy, S. Theoretical analysis of low-power optogenetic suppression of action potentials in human ventricular cardiomyocytes expressed with potassium-selective channelrhodopsins. Sci Rep 16, 9765 (2026). https://doi.org/10.1038/s41598-026-40578-4
Słowa kluczowe: optogenetyka serca, tłumienie arytmii, kanałorodopsyny selektywne dla potasu, czas trwania potencjału czynnościowego, zespół długiego QT