Clear Sky Science · pl
Odkrycie hydroksytriazolu jako potencjalnego inhibitora glyoksalazy I z wykorzystaniem technik wspomaganego komputerowo projektowania leków
Dlaczego powstrzymanie małego „sprzątacza” komórkowego może zwalczać raka
Komórki nowotworowe często rosną tak szybko, że toną we własnych odpadach. Jednym z ich mechanizmów przeżycia jest wbudowana ekipa sprzątająca, która detoksykuje szkodliwe produkty uboczne spalania cukrów. W tej pracy badano, jak wyłączyć jednego kluczowego członka tej ekipy — enzym o nazwie glyoksalaza I — używając komputerów do przesiawania dziesiątek tysięcy cząsteczek oraz eksperymentów do przetestowania najlepszych kandydatów. Celem jest odkrycie nowych „punktów wyjściowych” dla leków, które mogłyby kiedyś pomóc lekarzom selektywnie zatruwać komórki nowotworowe od środka.
Ukryty system usuwania odpadów wewnątrz naszych komórek
Każda komórka nieustannie rozkłada cukier, aby wytwarzać energię, a ten proces generuje reaktywny związek odpadowy zwany metylglioksem. W normalnych ilościach organizm przekształca metylglioksal w nieszkodliwy kwas mlekowy za pośrednictwem systemu glyoksalazowego — dwustopniowej ścieżki zależnej od pomocniczej cząsteczki glutationu. Glyoksalaza I jest pierwszym i najważniejszym etapem tego łańcucha. Komórki nowotworowe, które spalają cukier w zawrotnym tempie, silnie polegają na glyoksalazie I, aby zapobiec osiągnięciu toksycznych poziomów metylglioksalu. Jeśli ten enzym zostanie zablokowany, metylglioksal kumuluje się i może skierować uszkodzone komórki ku programowanej śmierci. To sprawia, że glyoksalaza I jest atrakcyjnym celem dla leków przeciwnowotworowych uderzających w podstawową słabość metabolizmu guza.
Przeszukiwanie przestrzeni chemicznej przy pomocy krzemowych mózgów i statystyki
Zamiast testować losowe substancje w laboratorium, badacze użyli wspomaganego komputerowo projektowania leków do przeszukania dużej komercyjnej kolekcji ponad 50 000 małych cząsteczek. Specjalistyczne oprogramowanie najpierw oczyszczało i standaryzowało każdą cząsteczkę, następnie przewidywało jej trójwymiarowy kształt i zachowanie w warunkach zbliżonych do pH organizmu. Szybki etap wirtualnego przesiewu oceniał, jak dobrze każdy kandydat mógłby dopasować się do miejsca aktywnego glyoksalazy I. Zespół następnie zastosował proste reguły dotyczące rozmiaru, rozpuszczalności i innych właściwości podobnych do leków, aby odrzucić cząsteczki mało obiecujące w warunkach biologicznych. Szczegółowszy program dokujący zbadał, jak najbardziej obiecujące molekuły mogą ustawić się wewnątrz enzymu, ze szczególnym uwzględnieniem tego, jak mogłyby sięgnąć i chwycić atom cynku, który leży w sercu chemii glyoksalazy I.
Nowy sposób chwycenia metalowego jądra enzymu
Wcześniejsze próby zablokowania glyoksalazy I koncentrowały się na dobrze znanych grupach chemicznych, takich jak kwasy karboksylowe i kwasy hydroksamamowe, które dobrze wiążą metale, ale często cierpią na słabą stabilność lub niepożądane skutki uboczne. Niniejsze badanie odkryło zamiast tego inny typ jednostki „chwytającej metal”: pierścień hydroksytriazolowy. Spośród szesnastu wysoko ocenionych cząsteczek wybranych do zakupu i testów laboratoryjnych, jedna nosząca ten pierścień — oznaczona jako SPB07393SC — wyróżniła się spośród pozostałych. W wirtualnym dokowaniu jej grupa hydroksytriazolowa sięgała do atomu cynku, podczas gdy jej dwa pierścienie aromatyczne wkładały się w pobliskie oleiste kieszenie enzymu. Symulacje komputerowe kompleksu trwające dziesiątki nanosekund sugerowały, że cząsteczka pozostawała ściśle związana, z stabilnymi odległościami, zwartą konformacją białka i trwałą siecią wiązań wodorowych.
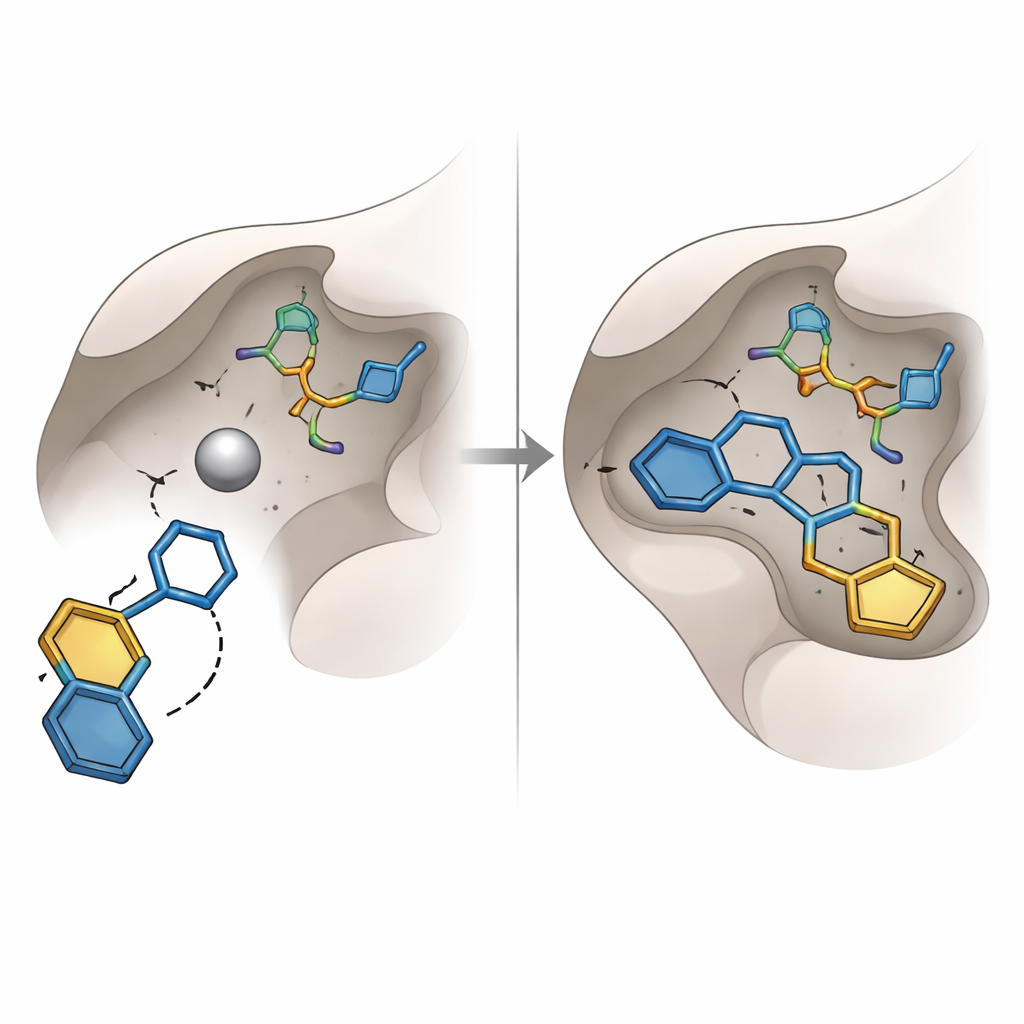
Sprawdzenie przewidywań w praktyce
Aby sprawdzić, czy modele komputerowe przekładają się na efekty w rzeczywistości, zespół zmierzył, jak dobrze wybrane cząsteczki spowalniają aktywność oczyszczonej ludzkiej glyoksalazy I w teście płytkowym. Piętnaście z szesnastu kandydatów wykazało jedynie słabą lub znikomą inhibicję w badanych warunkach, co podkreśla pułapki polegania wyłącznie na statycznych wynikach dokowania. W przeciwieństwie do nich SPB07393SC silnie hamowała enzym, z aktywnością w średnim zakresie mikromolowym, co czyni ją solidnym wczesnym „trafieniem”, a nie gotowym lekiem. Dodatkowe narzędzia programowe przewidziały, że ta cząsteczka powinna mieć akceptowalną rozpuszczalność, dobrą wchłanialność, zdolność dotarcia do mózgu w razie potrzeby oraz niskie prawdopodobieństwo wywołania pewnych toksyczności genetycznych lub wątrobowych, choć te prognozy bezpieczeństwa wciąż wymagają potwierdzenia eksperymentalnego.
Co to oznacza dla przyszłych leków przeciwnowotworowych
Praca wprowadza hydroksytriazol jako nowy sposób zakotwiczenia kandydatów na leki do atomu cynku w centrum glyoksalazy I, rozszerzając paletę chemicznych sztuczek dostępnych dla projektantów leków. Choć sama SPB07393SC jest jedynie punktem wyjścia, jej połączenie zdolności blokowania enzymu, przewidywanych właściwości podobnych do leku i stabilnego wiązania w symulacjach dynamicznych czyni ją obiecującym szkieletem do dalszego dopracowywania. Szerzej, badanie pokazuje zarówno moc, jak i ograniczenia przesiewania wspomaganego komputerowo: może szybko zawęzić ogromne biblioteki chemiczne do kilku realistycznych kandydatów, ale uważne eksperymenty laboratoryjne wciąż są niezbędne, by ujawnić, które cząsteczki rzeczywiście wyłączają enzym, od którego komórki nowotworowe zależą w zarządzaniu swoimi toksycznymi odpadami.
Cytowanie: Al-Qazzan, M., Al-Balas, Q., Alnajjar, B. et al. Discovery of hydroxytriazole as a potential glyoxalase-I inhibitor utilizing computer-aided drug design techniques. Sci Rep 16, 9945 (2026). https://doi.org/10.1038/s41598-026-40497-4
Słowa kluczowe: glyoksalaza I, metabolizm nowotworów, wspomagane komputerowo projektowanie leków, inhibitory wiążące cynk, dokowanie molekularne