Clear Sky Science · pl
Reagujące na bodźce nanonośniki z powłoką chitozanową na ferrytach do celowanego dostarczania kapsaicyny i bioaktywności selektywnej wobec HepG2 zależnej od rdzenia
Przyprawa o ukrytej mocy
Papryczki chili dodają naszym potrawom nie tylko ostrości: pieczenie pochodzi od kapsaicyny, naturalnego związku, który może też zabijać komórki nowotworowe. Jednak zastosowanie kapsaicyny jako leku jest trudne, ponieważ słabo rozpuszcza się w wodzie, szybko znika z organizmu i przy wysokich dawkach podrażnia zdrowe tkanki. W tym badaniu sprawdzono sposób ujarzmienia tej gorącej cząsteczki przez umieszczenie jej w malutkich, inteligentnych cząstkach, które mogą bezpiecznie przenosić kapsaicynę przez krew i uwalniać ją głównie wewnątrz guzów wątroby.
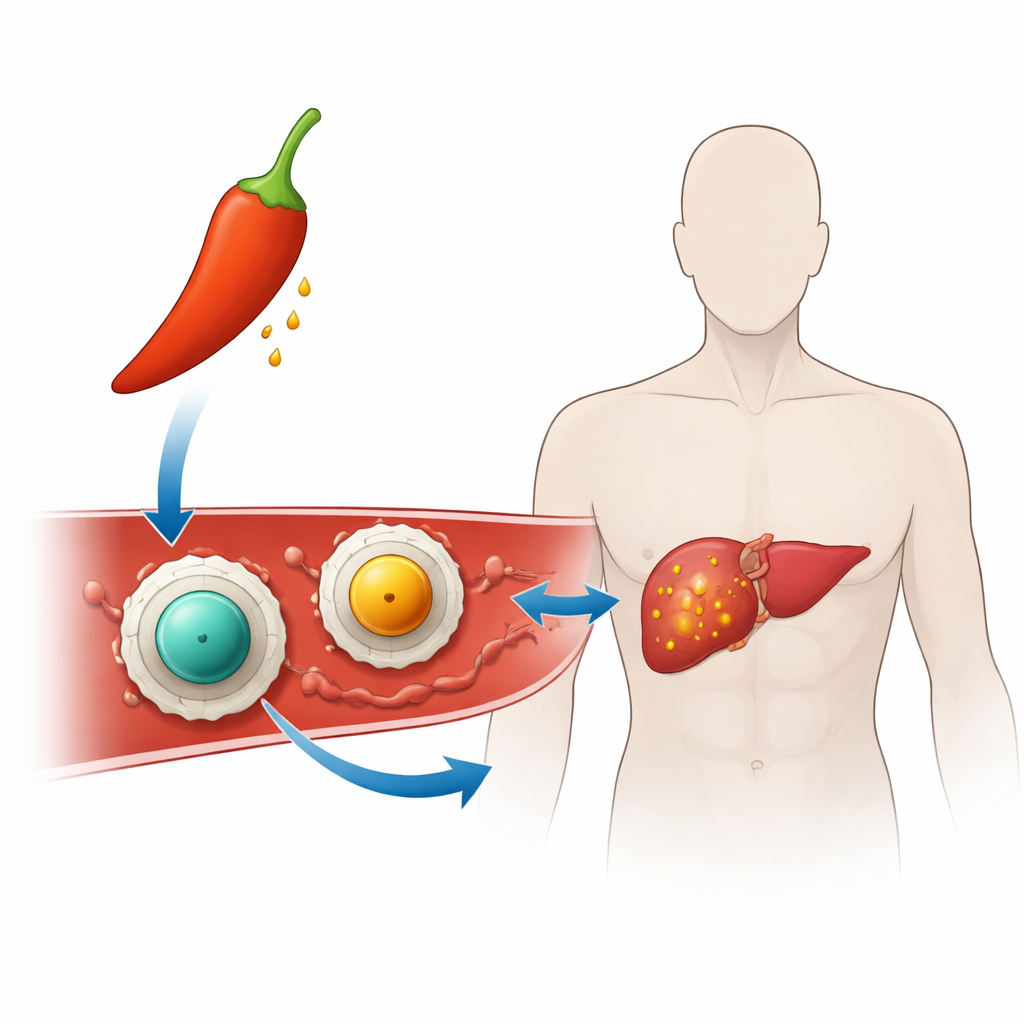
Przekształcenie ostrej papryki w terapię celowaną
Naukowcy zbudowali „nanonośniki” – cząstki tysiące razy mniejsze od ziarenka piasku – aby przetransportować kapsaicynę do komórek nowotworowych. Każdy nanonośnik ma stały rdzeń wykonany z magnetycznego minerału zwanego ferrytem (albo ferrytem cynkowym, albo ferrytem manganowym) owinięty cienką powłoką z chitozanu, substancji cukropodobnej pozyskiwanej z owoców morza, już stosowanej w produktach medycznych i spożywczych. Ta powłoka ułatwia zawieszenie cząstek w wodzie i pomaga im przylegać do powierzchni komórek oraz DNA, co jest istotne dla działania przeciwnowotworowego. Ładując kapsaicynę do tej chitozanowej powłoki, zespół miał nadzieję utrzymać lek stabilny i ukryty aż do dotarcia do surowego środowiska wewnątrz guza.
Inteligentne uwalnianie w warunkach guzowych
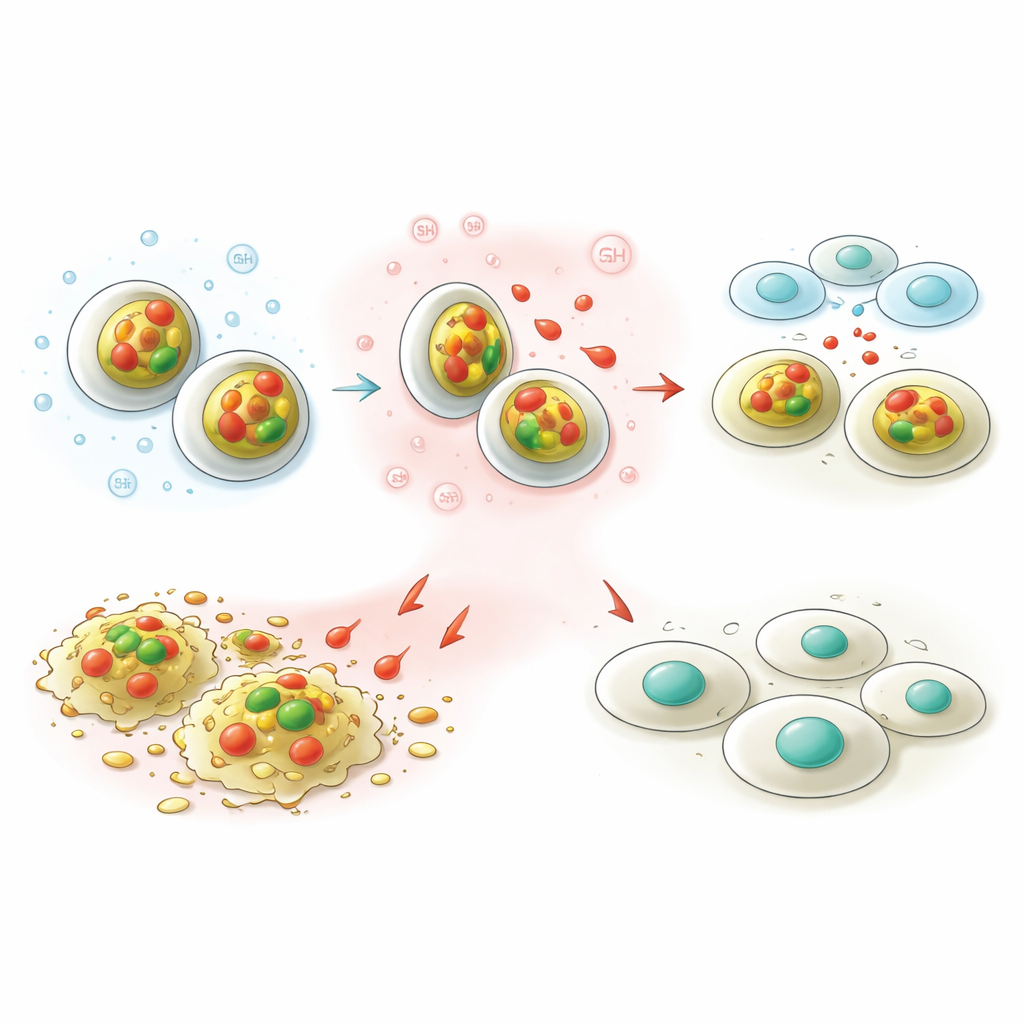
Jedną z kluczowych cech guzów jest to, że mają one tendencję do bycia bardziej kwaśnymi i bogatszymi w niektóre przeciwutleniacze, takie jak glutathion, niż tkanki zdrowe. Zespół zaprojektował swoje nanonośniki tak, aby wyczuwały te warunki. W testach laboratoryjnych przy normalnym pH krwi mniej niż 10 procent zgromadzonej kapsaicyny wyciekło przez dwa dni, co sugeruje, że cząstki niosłyby ładunek bezpiecznie podczas krążenia. W warunkach przypominających guza – bardziej kwaśnych i z obfitym glutathionem – cząstki uwalniały około jednej trzeciej kapsaicyny. To „włącz-wyłącz” zachowanie oznacza, że lek jest częściej uwalniany wewnątrz komórek nowotworowych niż po drodze, co potencjalnie zwiększa korzyści przy jednoczesnym zmniejszeniu działań niepożądanych.
Jak składniki cząstek wpływają na bezpieczeństwo i siłę działania
Chociaż dwa rodzaje nanonośników wyglądały podobnie z daleka, ich wewnętrzne rdzenie robiły dużą różnicę. Cząstki na bazie cynku miały tendencję do bycia mniejszymi i silniej wiązały kapsaicynę, podczas gdy cząstki na bazie manganu były bardziej porowate i uwalniały lek łatwiej. Oba typy miały silny dodatni ładunek powierzchniowy, co pomaga im w interakcji z ujemnie naładowanymi powierzchniami komórek i DNA. Testy na ludzkiej krwi wykazały bardzo niewielkie uszkodzenia czerwonych krwinek, a puste cząstki były łagodne dla normalnych komórek płuc, co potwierdza ich podstawowe bezpieczeństwo. Po załadowaniu kapsaicyną oba systemy stały się bardziej skuteczne przeciw komórkom raka wątroby, ale wersja manganowa osiągnęła najlepszą równowagę: silniej niszczyła komórki nowotworowe, pozostając relatywnie łagodna dla komórek normalnych.
Poza rakiem: dodatkowe efekty ochronne
Nanonośniki robiły więcej niż tylko dostarczały kapsaicynę. Spowalniały także wzrost kilku chorobotwórczych bakterii tak samo skutecznie jak standardowy antybiotyk w niektórych testach oraz pomagały neutralizować szkodliwe rodniki wolne, związane z zapaleniem i uszkodzeniem tkanek. Dokładne pomiary oparte na świetle wykazały, że po zapakowaniu kapsaicyny w cząstki ferryto–chitozanowe, przyłączała się ona silniej i stabilniej do DNA. Szybkie eksperymenty kinetyczne ujawniły dwustopniowy taniec: DNA najpierw przyczepia się do dodatnio naładowanej powierzchni cząstki, potem kompleks przeorganizowuje się w ciaśniejsze, trwalsze zespolenie. Te wzmocnione interakcje prawdopodobnie pomagają wyjaśnić, dlaczego naładowane cząstki wykazują silniejsze działanie przeciwnowotworowe, przeciwdrobnoustrojowe i przeciwutleniające niż sama kapsaicyna lub same cząstki ferryto.
Co to może znaczyć dla pacjentów
Na razie wyniki pochodzą z hodowli komórek, nie od pacjentów. Mimo to sugerują, że starannie zaprojektowane nanonośniki mogą przekształcić składnik ostrej przyprawy w bardziej precyzyjną broń przeciw nowotworom. Poprzez wybór odpowiedniego materiału rdzenia i powłoki badacze stworzyli maleńkie opakowania, które utrzymują kapsaicynę stabilną, przenoszą ją bezpiecznie we krwi i rozładowują ją preferencyjnie w warunkach przypominających guz, szczególnie w komórkach raka wątroby. Spośród testowanych projektów cząstki na bazie manganu oferowały najbardziej obiecujące połączenie celowanego niszczenia nowotworu, niskiego uszkodzenia komórek normalnych oraz dodatkowych korzyści przeciwbakteryjnych i przeciwutleniających. Po dalszych badaniach na zwierzętach i badaniach bezpieczeństwa takie „inteligentne” cząstki inspirowane papryką mogłyby pewnego dnia przyczynić się do łagodniejszych, bardziej ukierunkowanych terapii raka wątroby i potencjalnie innych chorób.
Cytowanie: Bakr, E., Elshami, F.I., Okba, E.A. et al. Stimuli-responsive chitosan-coated ferrite nanocarriers for targeted capsaicin delivery and core-dependent HepG2-selective bioactivity. Sci Rep 16, 8957 (2026). https://doi.org/10.1038/s41598-026-40433-6
Słowa kluczowe: kapsaicyna, rak wątroby, nanocząsteczki, celowane dostarczanie leków, nośniki reagujące na bodźce