Clear Sky Science · pl
MOV10, nowa immunoterapia i prognostyczny biomarker, przyczynia się do rozwoju glejaka przez regulację autofagii
Dlaczego to badanie nad rakiem mózgu ma znaczenie
Glejaki wielopostaciowe (glioblastoma), agresywna postać nowotworu mózgu, są niezwykle trudne do leczenia. Większość pacjentów przeżywa tylko kilka miesięcy od rozpoznania, mimo zabiegu chirurgicznego, radioterapii i chemioterapii. W tym badaniu przyjrzano się pojedynczemu molekułowi o nazwie MOV10, który wykazuje nadmierną aktywność w tych guzach. Pokazując, w jaki sposób MOV10 wspiera wzrost komórek nowotworowych, pozwala im unikać układu odpornościowego i opierać się śmierci, badacze wskazują nowy potencjalny cel dla skuteczniejszych terapii — oraz możliwy marker prognostyczny do przewidywania losów pacjentów.
Ukryty pomocnik śmiertelnych guzów mózgu
Zespół rozpoczął od eksploracji dużych publicznych baz danych onkologicznych zawierających informacje genetyczne i kliniczne od setek osób z glejakiem — szeroką grupą nowotworów mózgu, w tym glejakiem wielopostaciowym. Stwierdzili, że MOV10, białko zaangażowane w przetwarzanie RNA wewnątrz komórek, jest aktywowane na wyższych poziomach w tkankach glejaka niż w normalnym mózgu. Pacjenci, których guzy wytwarzały więcej MOV10, mieli tendencję do krótszego przeżycia, a związek ten utrzymywał się po uwzględnieniu wieku, stopnia zaawansowania guza i kluczowych cech genetycznych. Na podstawie tych czynników badacze zbudowali model matematyczny pokazujący, że poziomy MOV10 mogą pomóc przewidzieć szanse przeżycia pacjenta, sugerując, że MOV10 może pełnić rolę biomarkera prognostycznego.
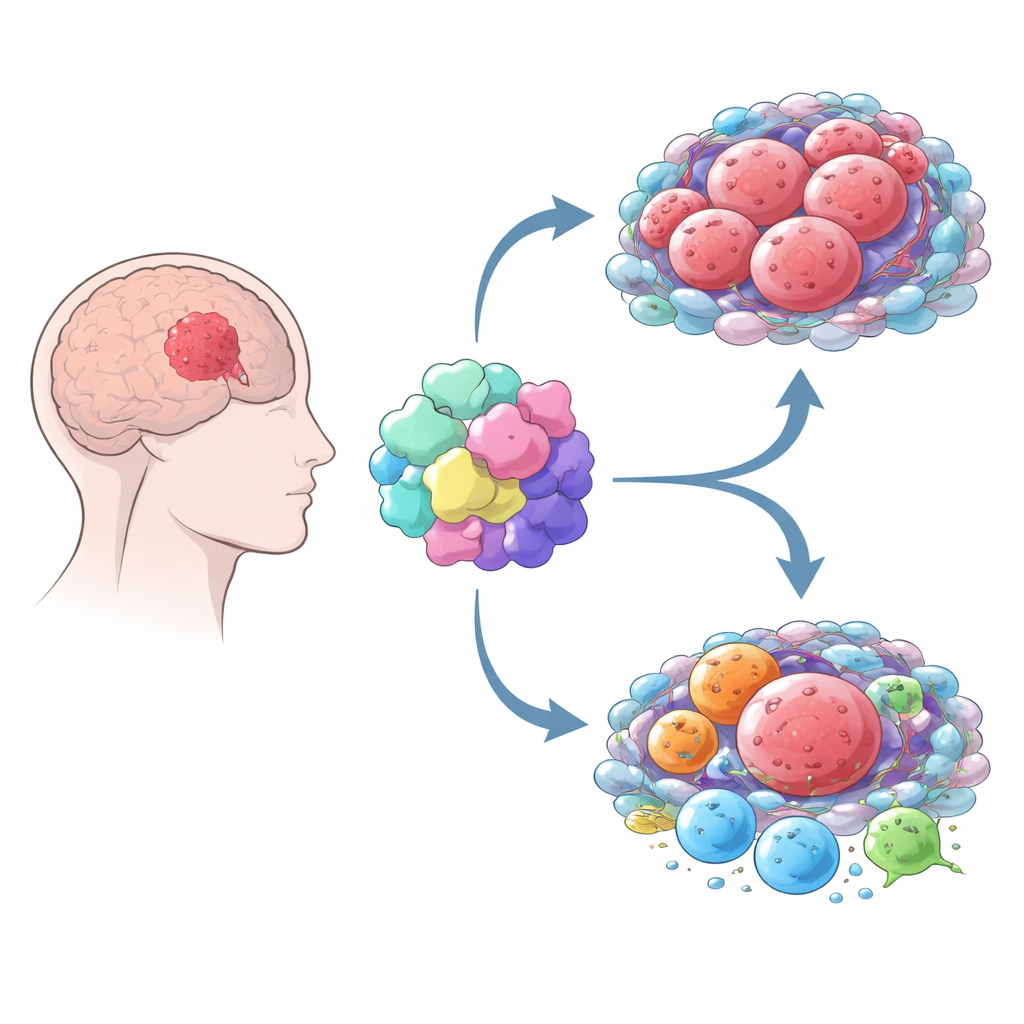
Jak MOV10 przebudowuje sąsiedztwo guza
Nowotwór nie rozwija się w izolacji — wykorzystuje otaczające „sąsiedztwo” komórek odpornościowych i podporowych. Łącząc kilka narzędzi obliczeniowych, autorzy pokazali, że glejaki o wysokim poziomie MOV10 są otoczone bogatszym miksem komórek odpornościowych i zrębowych niż guzy o niskim MOV10. To jednak nie oznacza skutecznej odpowiedzi immunologicznej. Zamiast tego guzy z wysokim poziomem MOV10 zawierają więcej makrofagów, zwłaszcza podtypu często nazywanego M2, który zwykle wspiera wzrost guza i tłumi odpowiedzi immunologiczne. Te guzy wykazywały także silniejsze sygnatury wyczerpanych limfocytów T oraz wyższą aktywność „hamulców” immunologicznych, będących celami popularnych leków immunoonkologicznych, takich jak PD-1 i CTLA-4. W całości układ wskazuje, że MOV10 wiąże się z immunosupresyjnym mikrośrodowiskiem, w którym obrony organizmu są osłabione.
Od big data do komórek w laboratorium
Aby wyjść poza korelacje, badacze zbadali MOV10 bezpośrednio w próbkach pacjentów i hodowlach komórkowych. Potwierdzili, że MOV10 występuje w większej ilości w tkankach glejaka niż w normalnym mózgu, a kilka powszechnie używanych linii komórkowych glejaka także wykazuje wysokie poziomy. Gdy zastosowali małe interferujące RNA (siRNA), aby zmniejszyć ekspresję MOV10 w komórkach glejaka hodowanych na płytkach, komórki dzieliły się wolniej, tworzyły mniej kolonii i traciły część zdolności do poruszania się oraz inwazji przez sztuczne membrany. Białka napędzające progresję cyklu komórkowego i inwazję spadły w obfitości, co wspiera ideę, że MOV10 aktywnie promuje agresywne zachowanie, zamiast być biernym towarzyszem.
Powiązanie MOV10 z komórkami odpornościowymi i szlakami samoczyszczenia
Badanie przyjrzało się także, jak MOV10 oddziałuje z dwoma kluczowymi procesami: zachowaniem makrofagów związanych z guzem oraz komórkowym systemem „samoczyszczenia” znanym jako autofagia. W próbkach ludzkich guzów MOV10 występował w tych samych rejonach co makrofagi o fenotypie podobnym do M2. W systemie współhodowli, gdy komórki glejaka były zmodyfikowane, by produkować mniej MOV10, mniej makrofagów typu M2 migrowało przez barierę w ich kierunku, sugerując, że MOV10 w komórkach guza pomaga przyciągać lub wspierać te pro‑guzowe komórki odpornościowe. Równocześnie analizy genetyczne powiązały MOV10 z kilkoma genami biorącymi udział w autofagii. Przy użyciu fluorescencyjnych znaczników, które uwidaczniają struktury recyklingu komórkowego, zespół wykazał, że obniżenie MOV10 zwiększa aktywność autofagii w komórkach glejaka i wyzwala więcej zaprogramowanej śmierci komórkowej. Zmiany w charakterystycznych białkach autofagii i apoptozy potwierdziły te obserwacje.
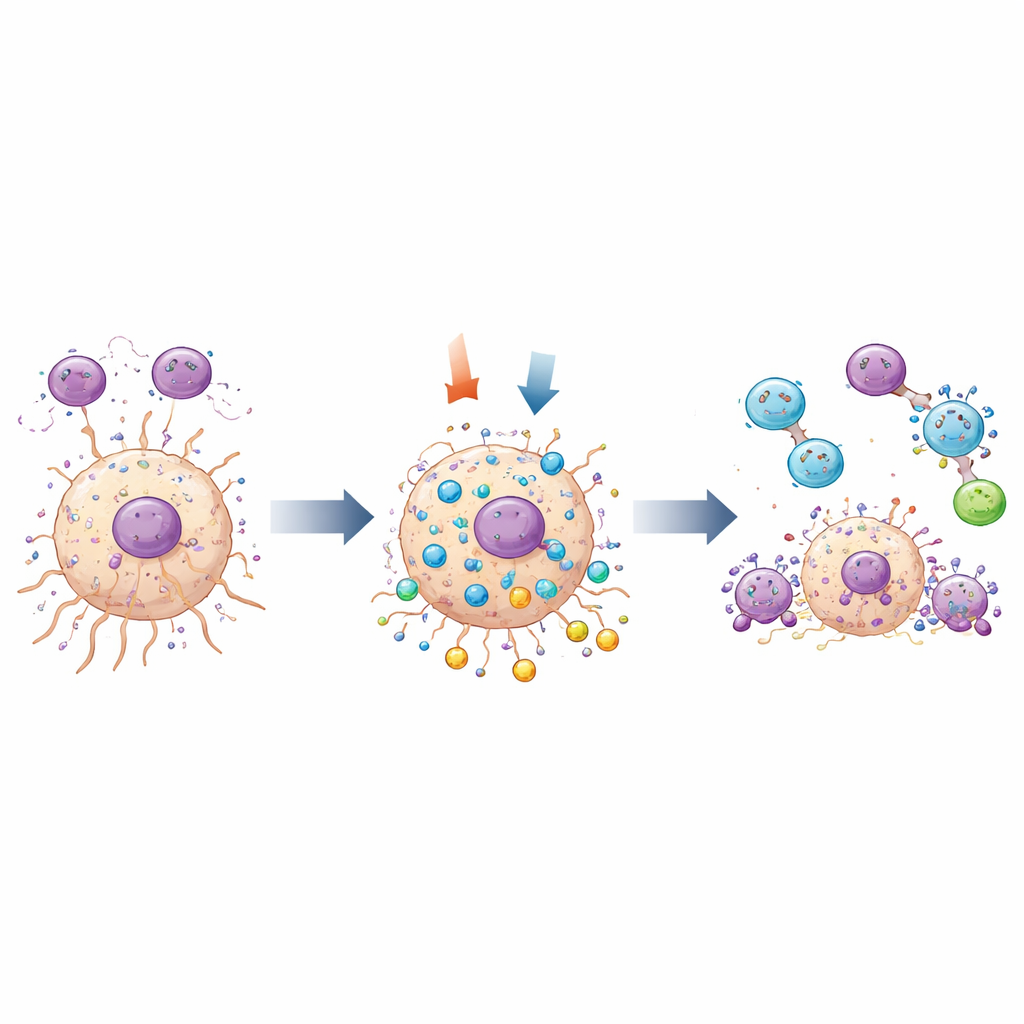
Co to oznacza dla przyszłych terapii
W sumie wyniki przedstawiają MOV10 jako wszechstronnego sojusznika glejaka: zwiększa wzrost i inwazję komórek nowotworowych, pomaga zbudować immunosupresyjne mikrośrodowisko bogate w makrofagi wspierające guz oraz utrzymuje w ryzach komórkowe systemy autodestrukcji i recyklingu. Kiedy MOV10 jest wyciszony, komórki glejaka rosną wolniej, łatwiej umierają i wydają się mniej zdolne do rekrutowania szkodliwych typów komórek odpornościowych. Dla osób nietechnicznych kluczowy przekaz jest taki, że MOV10 pełni rolę zarówno „termometru”, jak i „wyłącznika”: jego poziom w guzie może pomóc przewidzieć przebieg choroby, a jego obniżenie mogłoby, w teorii, uczynić guzy mózgu bardziej podatnymi na leczenie. Choć potrzebne są dalsze badania na modelach zwierzęcych i ostatecznie próby kliniczne, MOV10 wyróżnia się teraz jako obiecujący cel w dążeniu do lepszych terapii przeciw jednemu z najbardziej śmiertelnych nowotworów mózgu.
Cytowanie: Wang, F., Ruan, L., Yang, W. et al. MOV10, a novel immunotherapy and prognostic biomarker, contributes to glioma development by regulating autophagy. Sci Rep 16, 9501 (2026). https://doi.org/10.1038/s41598-026-40396-8
Słowa kluczowe: glejak wielopostaciowy, immunoterapia nowotworów mózgu, białko MOV10, mikrośrodowisko guza, autofagia i apoptoza