Clear Sky Science · pl
Trabectedyna plus tkankowo-celowany czynnik krzepnięcia CD13 tTF-NGR w zaawansowanym nawrotowym lub opornym mięsakach tkanek miękkich: dane translacyjne, bezpieczeństwo kliniczne i skuteczność
Dlaczego to badanie ma znaczenie
Osoby z zaawansowanymi mięsakami tkanek miękkich – rzadkimi nowotworami rozwijającymi się w mięśniach, tkance tłuszczowej lub innych tkankach podtrzymujących – często zostają bez skutecznych opcji terapeutycznych. To badanie bada nową dwuetapową strategię lekową zaprojektowaną tak, by uwięzić istniejący lek chemioterapeutyczny wewnątrz guza i odciąć jego dopływ krwi, z nadzieją na lepszą kontrolę choroby przy jednoczesnym utrzymaniu działań niepożądanych na akceptowalnym poziomie.
Rzadki nowotwór, który potrzebuje lepszych opcji
Mięsaki tkanek miękkich stanowią zaledwie około 1% nowotworów dorosłych, ale często są agresywne, gdy się rozsiewają lub nie można ich usunąć chirurgicznie. Standardowa chemioterapia może je spowolnić, jednak przeżycie osób z chorobą zaawansowaną pozostaje niskie. Trabectedyna jest jednym z głównych leków stosowanych po niepowodzeniu terapii pierwszego rzutu. Działa przez uszkadzanie DNA komórek nowotworowych oraz wpływ na komórki mikrośrodowiska guza. Mimo to wiele guzów ostatecznie nawraca, co motywuje badaczy do poszukiwania sposobów na zwiększenie jej skuteczności bez istotnego zwiększania szkód dla pacjentów.
Dwuetapowa „pułapka” na guz
Zespół przetestował koncepcję nazwaną „pułapką trabectedyny” (TRABTRAP). Najpierw pacjenci otrzymują trabectedynę w infuzji trwającej 24 godziny. W kolejnych dwóch lub trzech dniach podawany jest drugi lek, tTF-NGR. Ten zmodyfikowany białkowy fragment trafia do markera zwanego CD13, występującego głównie na naczyniach zaopatrujących guzy. Gdy tTF-NGR przyłącza się do tych naczyń, wywołuje miejscowe krzepnięcie krwi i blokuje przepływ, powodując obumieranie części guza. Założenie jest takie, że wcześniejsze podanie trabectedyny pozwala jej wniknąć do guza, a następnie tTF-NGR zamyka „wyjścia”, zamykając drobne naczynia guza, uwięziając lek tam, gdzie jest najbardziej potrzebny, i wzmacniając efekt obu terapii.
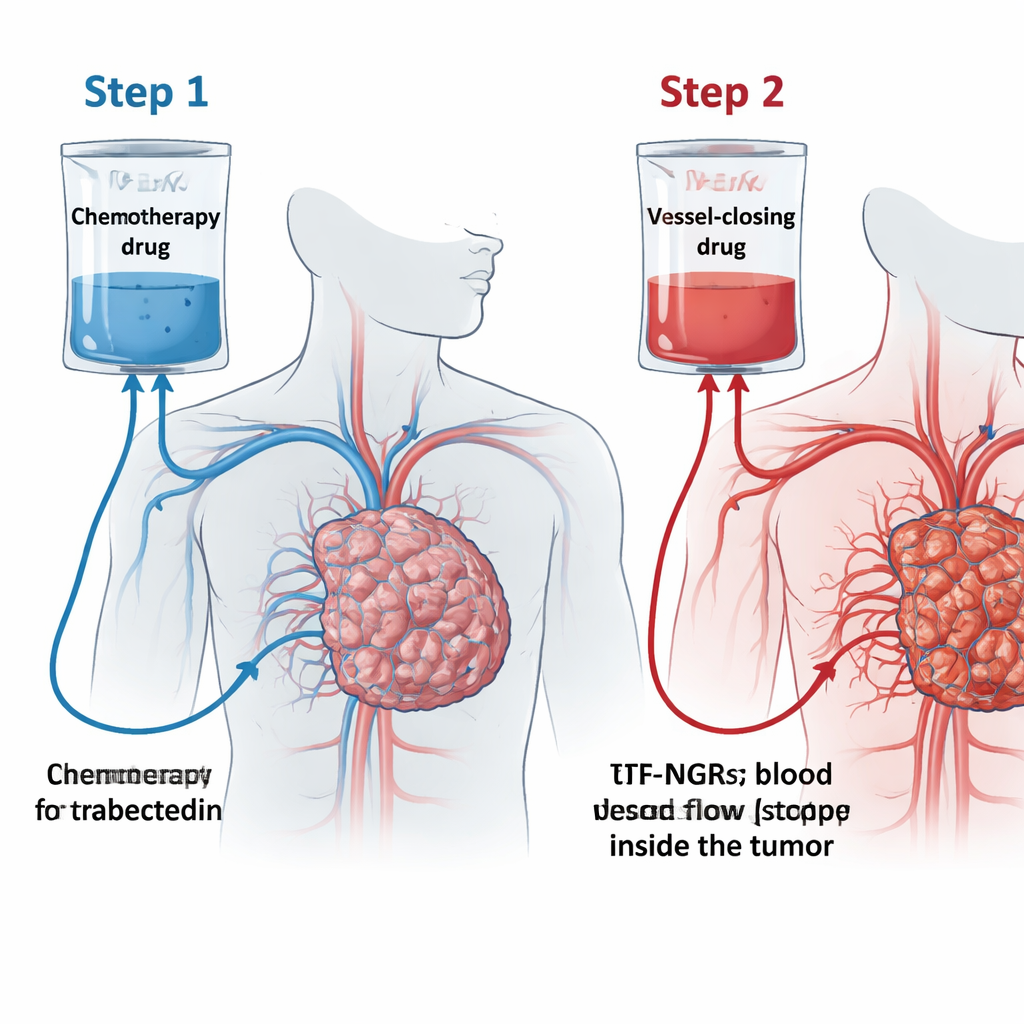
Od laboratorium do wczesnych badań u pacjentów
W badaniach laboratoryjnych badacze pokazali, że trabectedyna powoduje, iż komórki śródbłonka naczyń i komórki mięsaka eksponują na powierzchni więcej określonej cząsteczki tłuszczowej sprzyjającej krzepnięciu. Zmiana ta sprawiała, że tTF-NGR był bardziej skuteczny w wywoływaniu miejscowego tworzenia skrzepu na tych komórkach, co jest dokładnie tym, co potrzeba, aby zamknąć naczynia guza. U myszy z ludzkimi guzami mięsakowymi sekwencja trabectedyna, a następnie tTF-NGR prowadziła do większego zmniejszenia guzów niż każdy z leków osobno. Ponieważ guzy u zwierząt ulegały tak intensywnej destrukcji w wyniku połączenia, zespół nie był w stanie wiarygodnie zmierzyć, ile dodatkowej trabectedyny zostało uwięzione, ale silniejsza kontrola guza potwierdziła zasadniczą ideę „pułapki”.
Poszukiwanie bezpiecznej dawki u rzeczywistych pacjentów
Istotą pracy jest faza „run-in” bezpieczeństwa w badaniu TRABTRAP przeprowadzona u 19 osób z zaawansowanymi, wielokrotnie wcześniej leczonymi mięsakami tkanek miękkich. Wszyscy pacjenci otrzymali standardową dawkę trabectedyny. Drugi lek, tTF-NGR, rozpoczęto od najwyższej dawki wcześniej tolerowanej przy monoterapii, a następnie ostrożnie obniżano ją w przypadku wystąpienia poważnych działań niepożądanych. Przy wyższych dawkach u niektórych pacjentów pojawiły się istotne problemy kardiologiczne lub związane z zakrzepicą, takie jak utajone uszkodzenie mięśnia sercowego wykrywane w badaniach krwi, drobne zatory płucne czy zakrzepica żył głębokich. Zdarzenia te ustępowały po leczeniu i zaprzestaniu albo zmniejszeniu dawki tTF-NGR, ale sygnalizowały konieczność obniżenia dawki. Przy dawce 0,5 mg/m² tTF-NGR podawanej przez dwa dni po trabectedynie sześciu pacjentów ukończyło co najmniej dwa cykle bez toksyczności ograniczającej dawkę, a niektórzy kontynuowali leczenie nawet do 14 cykli.
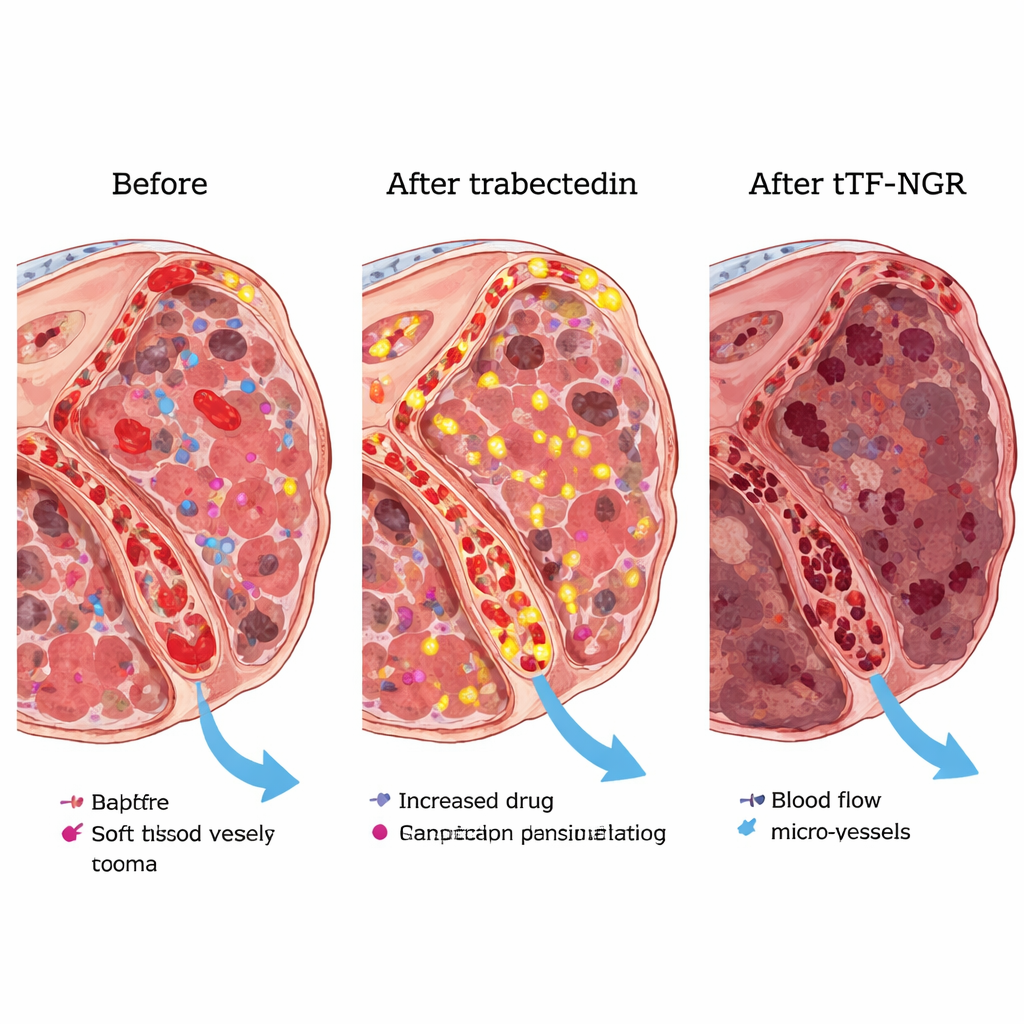
Wczesne sygnały korzyści i interakcje leków
Chociaż ta część badania była zbyt mała, by udowodnić skuteczność, wyniki były obiecujące. Spośród 19 pacjentów większość uzyskała przynajmniej przejściową kontrolę choroby, a u dwóch stwierdzono wyraźne częściowe zmniejszenie guzów. U osób z liposarcomą lub leiomyosarcomą – dwoma podtypami mięsaków często reagującymi na trabectedynę – niemal dwie trzecie miało stabilizację choroby lub częściowe odpowiedzi przy pierwszym istotnym badaniu kontrolnym. Szczegółowe badania MRI u jednego pacjenta potwierdziły, że tTF-NGR w wybranej dawce może selektywnie zmniejszać przepływ krwi wewnątrz ognisk guza. Badania krwi wykazały, że podany po trabectedynie tTF-NGR utrzymywał się dłużej w krążeniu i wydawał się bardziej czynny niż przy stosowaniu samodzielnym, co pomaga wyjaśnić, dlaczego bezpieczna dawka w połączeniu jest niższa niż dla leku stosowanego w monoterapii.
Co to oznacza dla pacjentów
Dla osób z zaawansowanym mięsakami tkanek miękkich TRABTRAP stanowi starannie opracowaną próbę zwiększenia efektu istniejącej chemioterapii poprzez skojarzenie jej z czynnikiem zamykającym naczynia, który celuje w własne zaopatrzenie guza w krew. Faza run-in bezpieczeństwa pokazuje, że przy dostosowanych dawkach to połączenie można podawać wielokrotnie, a działania niepożądane są znaczące, lecz na ogół możliwe do opanowania i odwracalne przy ścisłym nadzorze. Choć jest za wcześnie, by stwierdzić, czy podejście to wydłuży życie lub konsekwentnie zmniejszy guzy, obiecująca wczesna kontrola choroby i wyraźne efekty na przepływ krwi w guzie uzasadniają kontynuację badań w większym, randomizowanym badaniu. Jeśli przyszłe wyniki będą pozytywne, ten dwuetapowy sposób leczenia mógłby otworzyć nową drogę terapii mięsaków i zainspirować podobne strategie wobec innych trudnych do leczenia nowotworów.
Cytowanie: Hessling, K., Brand, C., Schwöppe, C. et al. Trabectedin plus CD13-targeted tissue factor tTF-NGR against advanced relapsed or refractory soft tissue sarcoma: translational data, clinical safety and efficacy. Sci Rep 16, 7389 (2026). https://doi.org/10.1038/s41598-026-40362-4
Słowa kluczowe: mięsak tkanek miękkich, trabectedyna, naczynia nowotworowe, celowana terapia koagulacyjna, chemioterapia skojarzona