Clear Sky Science · pl
Adaptacyjny wybór przykładów dla prototypowego, wyjaśnialnego wykrywania mitoz w patologii cyfrowej
Dlaczego to ma znaczenie dla opieki nad pacjentem onkologicznym
Gdy patolodzy oglądają próbki nowotworowe pod mikroskopem, zliczanie komórek nowotworowych aktywnie się dzielących pomaga ocenić agresywność guza i dobrać leczenie. Sztuczna inteligencja potrafi obecnie szybko wykrywać te dzielące się komórki na cyfrowych skanach, ale jej decyzje często pozostają tajemnicą nawet dla ekspertów. W artykule wprowadzono metodę nazwaną Adaptacyjnym Wyborem Przykładów (AES), która pozwala systemowi AI „pokazać swoje rozumowanie” poprzez wskazanie rzeczywistych, wcześniejszych przypadków wspierających lub podważających każdą decyzję, co sprawia, że automatyczne wykrywanie mitoz staje się bardziej przejrzyste i klinicznie wiarygodne.
Wyzwanie wykrywania komórek dzielących się
Komórki nowotworowe w trakcie podziału, zwane figurami mitotycznymi, są małe, rzadkie i wizualnie zróżnicowane. Pod rutynowym, różowo-fioletowym barwieniem mogą bardzo przypominać nieszkodliwe struktury, takie jak komórki w fazie obumierania czy pewne komórki układu odpornościowego. Eksperci muszą przeszukiwać ogromne cyfrowe skany, co jest pracochłonne, męczące i podatne na rozbieżności oceny. Nowoczesne systemy głębokiego uczenia mogą dorównywać lub przewyższać ekspertów w tym zadaniu, ale zachowują się jak czarne skrzynki: generują dla każdego podejrzanego obiektu wynik bez jasnego uzasadnienia. W medycynie, gdzie decyzje terapeutyczne mogą zmieniać życie, brak przejrzystości jest poważną przeszkodą we wdrożeniu AI do rutynowej praktyki.
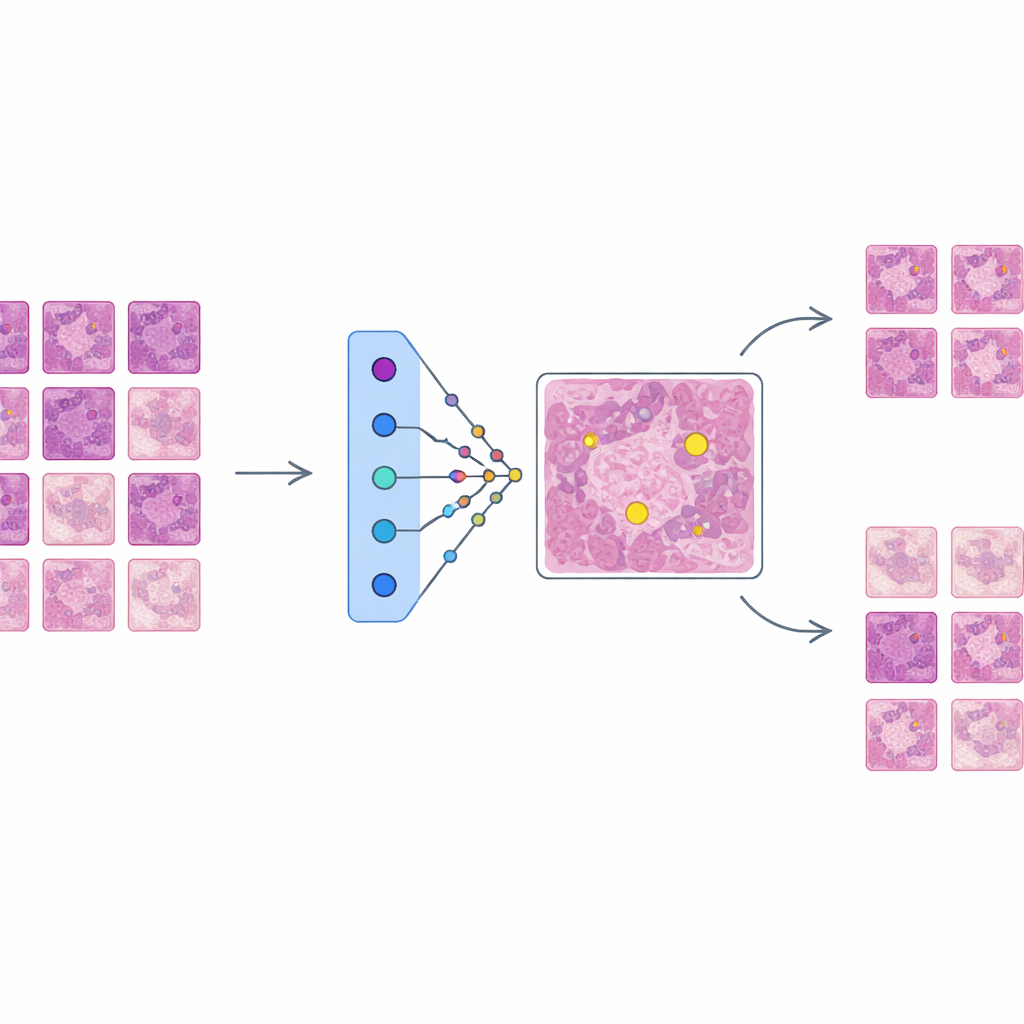
Budowanie silnego, lecz nieprzejrzystego detektora
Autorzy najpierw trenują zaawansowaną sieć do detekcji obiektów opartą na architekturze Faster R-CNN, aby odnajdywała figury mitotyczne w dużym, zróżnicowanym zbiorze danych o nazwie MIDOG++. Obrazy pochodzą zarówno z guzów ludzkich, jak i psich, obejmują kilka typów nowotworów i laboratoriów oraz zawierają ponad jedenaście tysięcy starannie oznakowanych komórek dzielących się. Aby zachować drobne detale, skany są dzielone na małe płaty i mocno augmentowane, by imitować rzeczywiste wariacje barwienia i obrazowania. Otrzymany detektor osiąga solidne wyniki w różnych typach nowotworów, z wartościami F1 sięgającymi 0,84, co potwierdza jego dokładność, ale także złożoność — typ systemu, który wymaga lepszych wyjaśnień, zanim klinicyści zaufają mu w praktyce.
Nauczanie AI, by wyjaśniała się przykładami
AES działa jako warstwa interpretowalności na wierzchu wytrenowanego detektora, nie zmieniając jego sposobu działania. Dla każdego obszaru, który detektor oznaczył jako potencjalnie mitotyczny, AES przeszukuje bibliotekę rzeczywistych fragmentów tkanki pochodzących z danych treningowych. Z tej biblioteki wybiera niewielki zestaw przykładów „wspierających”, które przypominają prawdziwe mitozy, oraz zestaw przykładów „podważających”, które bardziej przypominają komórki niemitozyjne. W tle AES traktuje współczynniki ufności detektora jako gładki pejzaż i używa narzędzia matematycznego zwanego funkcjami podstawy radialnej do przybliżenia, jak ta ufność zmienia się wokół każdego przypadku. Zachowywane są tylko prototypy, które istotnie wpływają na lokalny poziom ufności, więc wyjaśnienie pojedynczej decyzji zwykle obejmuje około dziesięciu starannie dobranych przykładów zamiast setek ledwie istotnych.
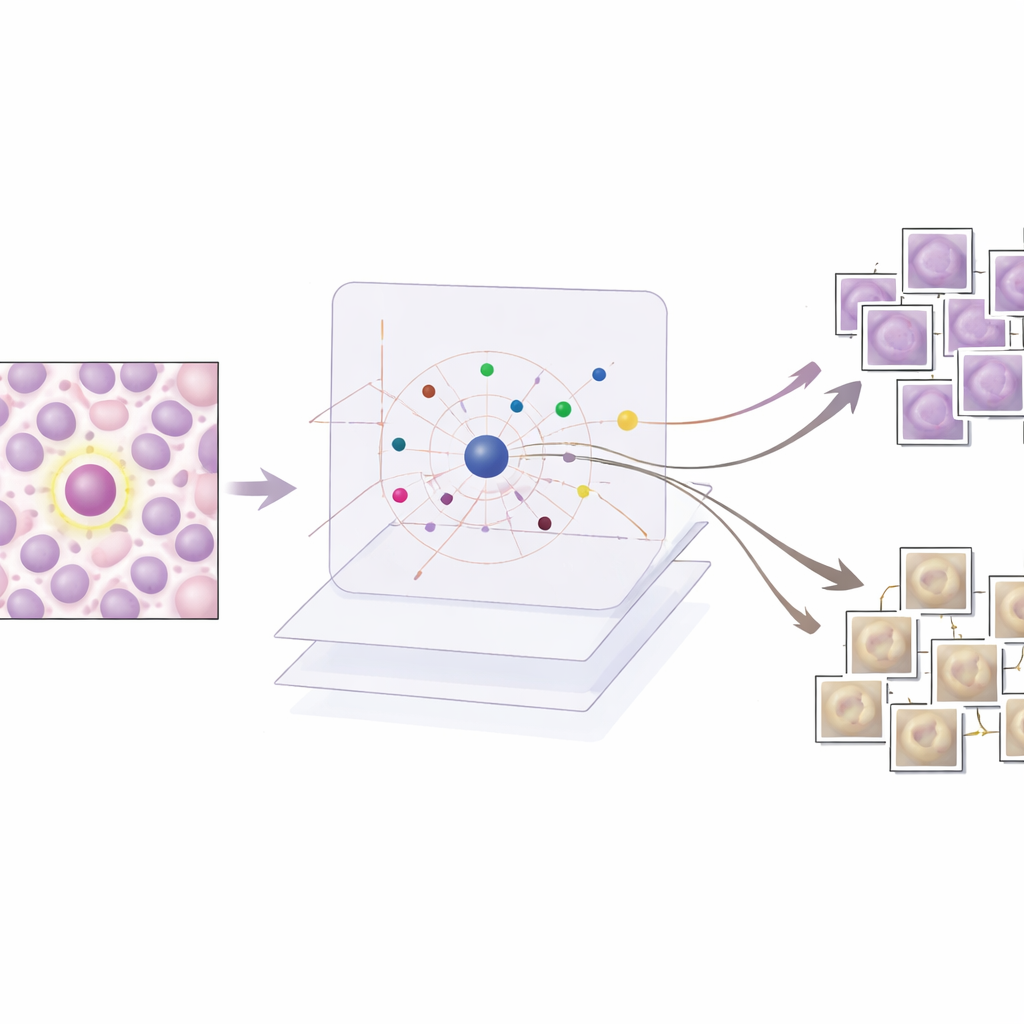
Co przykłady ujawniają o decyzjach AI
Naukowcy oceniają AES zarówno ilościowo, jak i jakościowo. Ilościowo pokazują, że kompaktowy słownik liczący około 190 obrazów prototypowych potrafi z dużą dokładnością naśladować współczynniki ufności detektora, przy jednoczesnym utrzymaniu liczby przykładów pokazywanych dla pojedynczego przypadku na poziomie umożliwiającym przegląd przez człowieka. Jakościowo analizują trzy typowe scenariusze. Gdy detektor jest wyraźnie poprawny, AES zwraca tylko prototypy mitotyczne silnie wspierające decyzję, co daje klinicystom pewność. W przypadku fałszywych alarmów metoda ukaże podobne do mitoz przykłady, które wyjaśniają, dlaczego detektor został zmyślony przez podobną teksturę czy wzory chromatyny, często obok słabszych prototypów niemitozyjnych sugerujących niepewność. W przypadku pominiętych mitoz AES zwykle zwraca głównie prototypy niemitozyjne lub niejednoznaczne przykłady, wskazując na luki w danych treningowych i sugerując, gdzie potrzebne są nowe lub lepiej oznakowane przykłady.
Od czarnej skrzynki do narzędzia współpracy
Ugruntowując każdą prognozę w kilku rzeczywistych, oznakowanych fragmentach tkanki, AES sprawia, że złożony detektor AI zachowuje się bardziej jak ludzki współpracownik, który uzasadnia decyzje, przypominając sobie wcześniejsze przypadki. System nie tylko informuje, czy komórka prawdopodobnie się dzieli, ale także pokazuje dlaczego i z jaką pewnością, poprzez mieszankę i wpływ prototypów wspierających i podważających. Takie rozwiązanie pozwala patologom szybko potwierdzać mocne predykcje, skupić uwagę na granicznych lub mylących obszarach oraz identyfikować systematyczne wzorce błędów, które mogą kierować dalszym treningiem. Choć metoda opracowana została do wykrywania mitoz, ten sam sposób można rozszerzyć na inne zadania w patologii cyfrowej, pomagając przesunąć AI z nieprzejrzystej automatyzacji ku interpretowalnemu, opartemu na przypadkach asystentowi, którego klinicyści mogą pytać, któremu mogą ufać i który może być udoskonalany.
Cytowanie: Banik, M., Kreutz-Delgado, K., Mohanty, I. et al. Adaptive example selection for prototype based explainable mitosis detection in digital pathology. Sci Rep 16, 9481 (2026). https://doi.org/10.1038/s41598-026-40283-2
Słowa kluczowe: wyjaśnialna sztuczna inteligencja, patologia cyfrowa, wykrywanie mitoz, modele oparte na prototypach, diagnostyka nowotworowa