Clear Sky Science · pl
Ultranasilne pulsacyjne źródło promieniowania jonizującego oparte na bezpośrednim przyspieszaniu elektronów laserem do badania efektu FLASH
Dlaczego ultrakrótki impuls promieniowania ma znaczenie
Radioterapia nowotworów balansuje na cienkiej linii: dostarczyć wystarczającą dawkę, by zniszczyć guz, nie szkodząc trwałe tkankom zdrowym. Niedawno powstała i budząca duże zainteresowanie koncepcja, zwana efektem FLASH, sugeruje, że podanie dawki w ultrakrótkim, ultramocnym wybuchu może oszczędzać tkanki normalne przy jednoczesnym działaniu na nowotwór. W tym badaniu przedstawiono nowy rodzaj eksperymentalnego źródła promieniowania opartego na potężnym laserze, który generuje wyjątkowo krótkie serie wysokoenergetycznych elektronów, i użyto go do obserwacji, jak tlen w wodzie i płynach biologicznych jest nagle zużywany podczas naświetlania — procesu uważanego za centralny w efekcie FLASH. 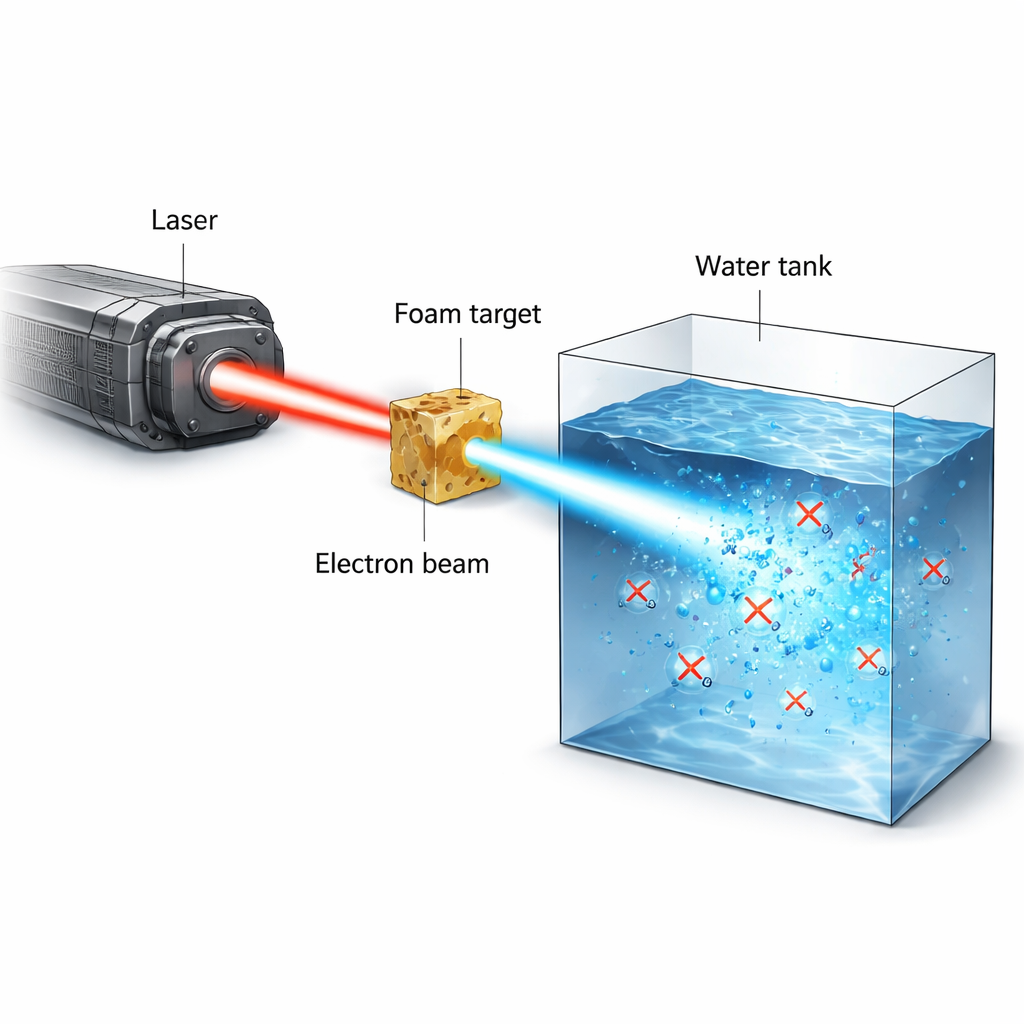
Od maszyn szpitalnych do wiązek napędzanych laserem
Konwencjonalna radioterapia wykorzystuje promieniowanie X, elektrony lub protony z dużych akceleratorów. Urządzenia te zwykle dostarczają dawkę w czasie od milisekund do sekund i choć są bardzo precyzyjne, nadal uszkadzają tkanki zdrowe, ponieważ promieniowanie pośrednio łamie DNA przez rozpady cząsteczek wody i wytwarzanie reaktywnych form tlenu. Obecność tlenu w dobrze unaczynionej tkance zdrowej faktycznie nasila to uszkodzenie — tzw. efekt tlenu. Radioterapia FLASH zmierza do odwrócenia tej sytuacji, podając pełną dawkę terapeutyczną w ułamku sekundy przy ultrawysokich szybkościach dawki, co w badaniach na zwierzętach wydaje się tymczasowo chronić tkanki normalne bez osłaniania guzów. Jednak standardowe akceleratory medyczne mają trudności z osiągnięciem takich ekstremalnych szybkości dawki, co skłania do poszukiwania alternatywnych źródeł, takich jak lasery wysokiej mocy.
Przekształcanie pianki i światła w potężny wybuch elektronów
Naukowcy użyli lasera wysokiej mocy PHELIX do wygenerowania wąskich, wysokoprądowych wiązek elektronów o energiach dochodzących do kilku milionów elektronowoltów (MeV). Laser najpierw zjonizował niskogęstą piankę polimerową do stanu plazmy bliskiej krytycznej. W drugim, ultrakrótki impulsie trwającym poniżej trylionowej części sekundy laser popychał i pułapkował elektrony wewnątrz kanału plazmowego, bezpośrednio je przyspieszając do wysokich energii. Ten proces, zwany bezpośrednim przyspieszaniem laserowym, wytwarza silnie skolimowaną wiązkę mogącą przenosić dziesiątki nanokulombów ładunku w impulsie o skali pikosekundy. Gdy ta wiązka uderza w wodę lub materiał o charakterze wodnym, może zdeponować 20–50 grayów dawki w pojedynczym strzale, przy chwilowych szybkościach dawki powyżej 10¹³ gray na sekundę — daleko poza możliwościami standardowych urządzeń.
Obserwacja znikania tlenu w mgnieniu oka
Aby zbadać, jak tak intensywne impulsy wpływają na chemię w warunkach przypominających tkanki, zespół skonstruował hermetyczne zbiorniki z wodą działające w próżni i napełniane albo czystą wodą, medium hodowlanym komórek, albo lizowanymi komórkami, wszystkie uprzednio w pełni natlenowane. Wiązka elektronów była kształtowana i filtrowana tak, by to wysokoekranowe elektrony dominowały w dawce wewnątrz zbiornika, podczas gdy protony i promieniowanie rentgenowskie były w dużym stopniu tłumione lub dokładnie uwzględniane przy pomocy warstw osłon i filmów radiochromicznych. Czujnik optyczny umieszczony na wewnętrznej ścianie zbiornika monitorował rozpuszczony tlen, mierząc, jak cząsteczki tlenu gasiły luminescencję kropki barwnika. Po każdym pojedynczym impulsie sensor zarejestrował nagły spadek stężenia tlenu, który następnie powoli wracał do poziomu w miarę dyfuzji tlenu w obszarze sensora. Łącząc dane z filmów, symulacje i znane moce hamowania elektronów, autorzy zrekonstruowali dawkę dostarczoną do naświetlanego wolumenu i powiązali ją bezpośrednio z mierzoną utratą tlenu. 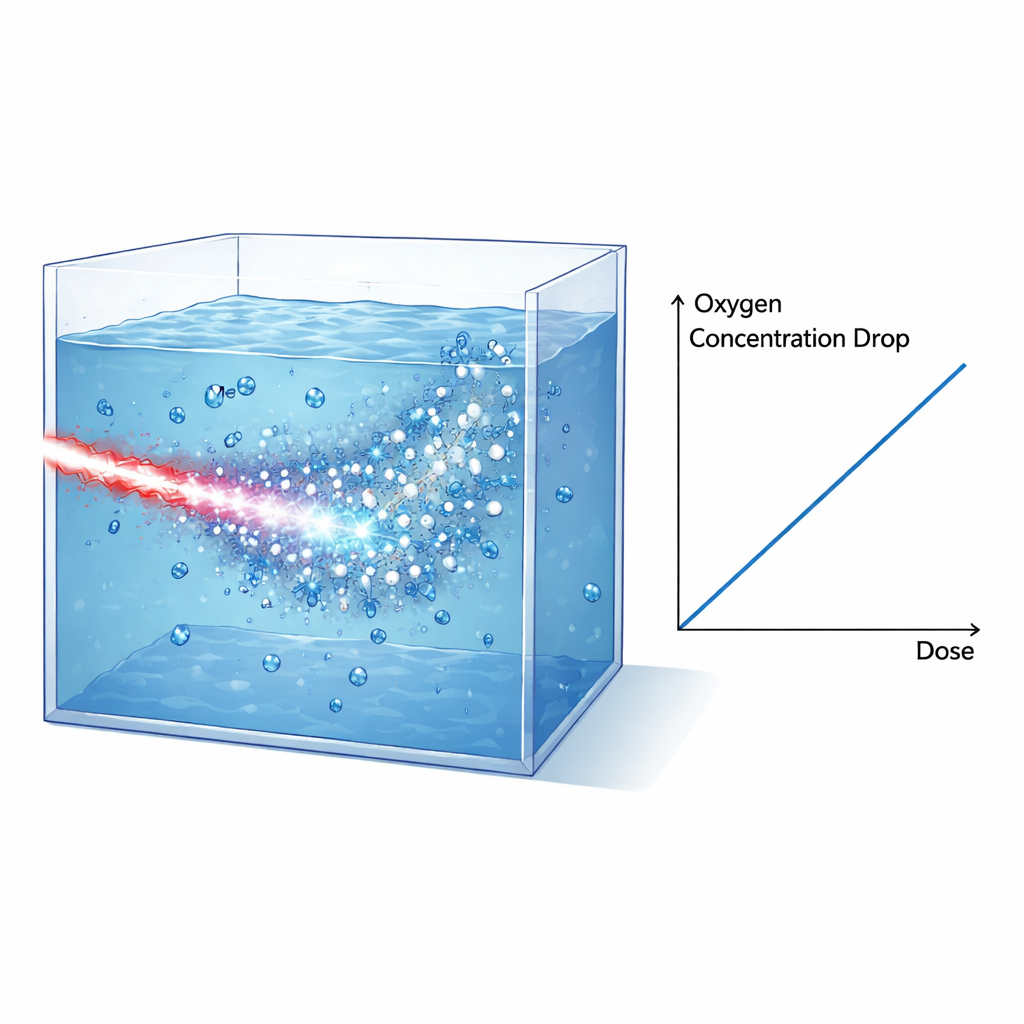
Łączenie eksperymentu z teorią
Kluczowe odkrycie polega na tym, że spadek rozpuszczonego tlenu jest wprost proporcjonalny do dostarczonej dawki zarówno w wodzie, jak i w medium hodowlanym, z bardzo podobnymi nachyleniami zależności. Po skorygowaniu o niewielką dodatkową dawkę od promieniowania rentgenowskiego, zmierzone zużycie tlenu w wodzie wynosi około 0,32 mikromola na litr na gray. Ta wartość zgadza się zadziwiająco dobrze z przewidywaniami złożonych symulacji typu Monte Carlo śledzących strukturę torów (TRAX-CHEM), które śledzą trajektorie elektronów w wodzie i modelują szybką chemię zachodzącą w mikrosekundach po napromienieniu. Co istotne, w tym układzie napędzanym laserowo niemal cała dawka jest dostarczona w czasie rzędu jednej pikosekundy — znacznie krócej niż charakterystyczne czasy reakcji chemicznych, które następują później. Oznacza to, że eksperyment wiernie odtwarza idealne warunki przyjęte w tych symulacjach, dostarczając rygorystycznego testu dla stosowanych modeli.
Budowanie lepszego poligonu do badań nad FLASH
Poza walidacją teorii, autorzy wykorzystują wyniki do zaprojektowania ulepszonej konfiguracji eksperymentalnej. Upraszczając geometrię, eliminując magnesy i symetrycznie umieszczając wodę oraz filmy pomiarowe wokół wiązki, przyszłe układy mogłyby bezpośrednio mierzyć dawkę wewnątrz zbiornika bez skomplikowanej rekonstrukcji, jednocześnie jeszcze bardziej tłumiąc niepożądane wkłady protonów i promieniowania rentgenowskiego. Symulacje pokazują, że modyfikacja celu — na przykład dodanie cienkich warstw plastiku lub złota — umożliwia regulację dawki na strzał w przybliżeniu między 40 a 80 gray, oferując elastyczną platformę do badania szerokiego zakresu warunków istotnych dla FLASH.
Co to oznacza dla przyszłych terapii nowotworowych
Dla czytelników niebędących specjalistami kluczowy przekaz jest taki, że to źródło oparte na laserze generuje niezwykle intensywne, ultrakrótki impulsy elektronów, które imitują — a w pewnych aspektach przewyższają — warunki przewidywane dla radioterapii FLASH. Badanie pokazuje, że te impulsy szybko zużywają rozpuszczony tlen w wodzie i mediach biologicznych w sposób zgodny z zaawansowanymi przewidywaniami teoretycznymi. Ponieważ wyczerpywanie tlenu i związana z nim chemia rodnikowa są wiodącymi kandydatami na wyjaśnienie, dlaczego FLASH może chronić tkanki zdrowe, posiadanie kontrolowalnego, dobrze zrozumiałego źródła takiego jak to stanowi istotny krok naprzód. Zapewnia potężny poligon do dopracowywania modeli i ostatecznie do prowadzenia prac nad projektowaniem przyszłych urządzeń klinicznych, które mogłyby skuteczniej leczyć nowotwory przy mniejszych skutkach ubocznych.
Cytowanie: Gyrdymov, M., Bukharskii, N., Fabian, V. et al. Ultra-intense pulsed source of ionizing radiation based on direct laser acceleration of electrons for studying the FLASH effect. Sci Rep 16, 7164 (2026). https://doi.org/10.1038/s41598-026-40281-4
Słowa kluczowe: radioterapia FLASH, elektrony napędzane laserem, ultranagła dawka, utlenowanie, radioliza wody