Clear Sky Science · pl
Selektywne usuwanie przeciwciał monoklonalnych przez receptor mannozowy zależy od parowania glikanów
Dlaczego wzory cukrowe w lekach mają znaczenie
Wiele z dzisiejszych najlepiej sprzedających się leków to przeciwciała monoklonalne — białka zaprojektowane tak, by przez tygodnie krążyć we krwi i precyzyjnie celować w choroby, takie jak nowotwory czy schorzenia autoimmunologiczne. Jednak nie wszystkie przeciwciała zachowują się tak samo po wstrzyknięciu. Badanie stawia pozornie proste, ale dalekosiężne pytanie: w jaki sposób drobny „wzór cukrowy” przyłączony do przeciwciała decyduje o tym, jak szybko organizm je usuwa, i czy może to także kształtować skutki uboczne, takie jak reakcje immunologiczne?
Maleńkie cukry jako sygnały drogowe
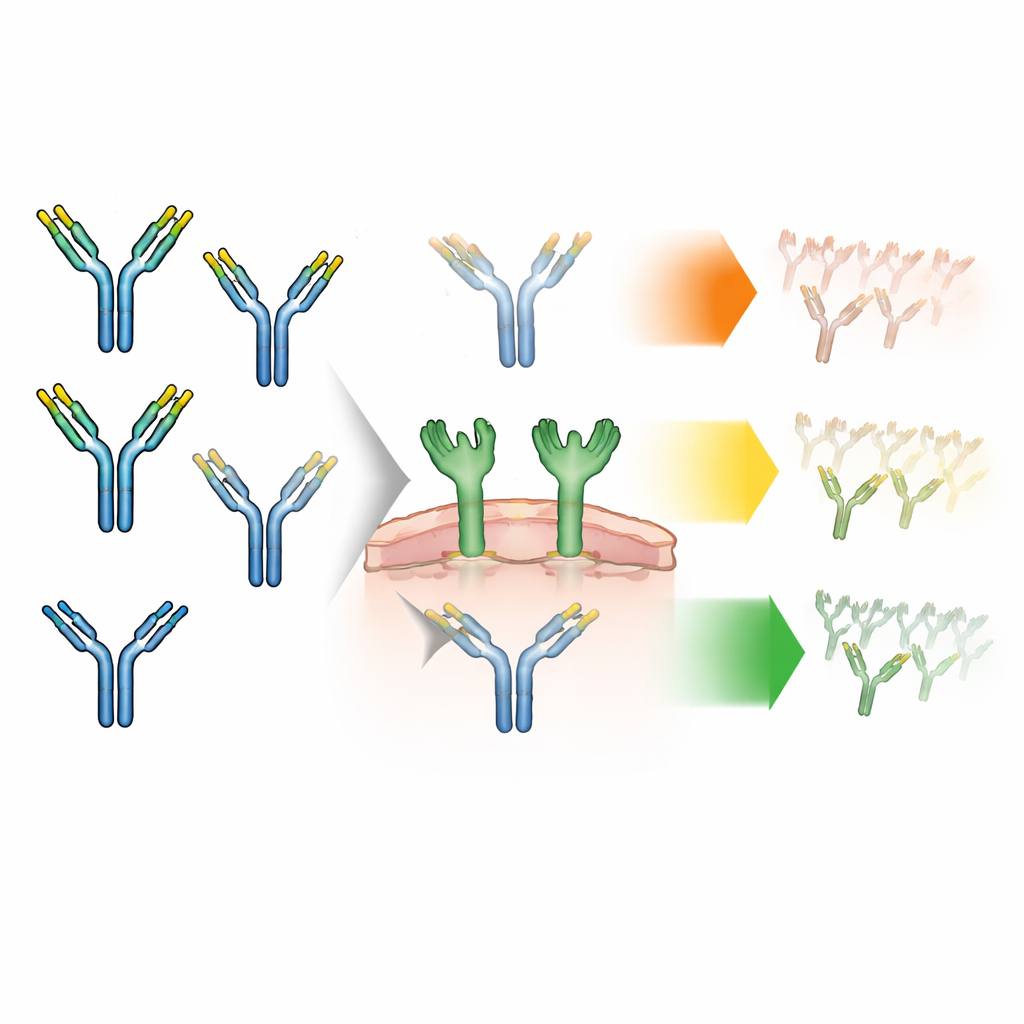
Przeciwciała naturalnie noszą krótkie łańcuchy cukrów — zwane glikanami — na swoim szkielecie. Glikany występują w różnych „odmianach”. Większość ma złożoną budowę, ale mniejszość to tzw. wysokomannozydowe formy, prostsze, które wcześniejsze badania powiązały z szybszym usuwaniem z krwi. Każde przeciwciało ma dwa miejsca glikozylacji działające w parze; mogą być one zgodne (pary symetryczne) lub różne (pary asymetryczne). Do tej pory producenci leków zazwyczaj zliczali, ile każdego typu cukru występuje łącznie, nie pytając, jak te dwa cukry na tym samym przeciwciałe się parują. Autorzy przypuszczali, że pattern parowania może zmieniać siłę interakcji przeciwciał z białkiem-czujnikiem cukrów na komórkach odpornościowych — receptorem mannozowym — a przez to wpływać na tempo usuwania leku.
Sortowanie przeciwciał według par cukrowych
Aby to zbadać, zespół przygotował przeciwciała wzbogacone w glikany wysokomannozydowe, a następnie fizycznie rozdzielił je na trzy główne grupy: przeciwciała z dwoma glikanami złożonymi, z jednym glikanem złożonym i jednym wysokomannozydowym (asymetryczne) oraz z dwoma glikanami wysokomannozydowymi (symetryczne). Dokładnie potwierdzili, że te grupy były niemal identyczne pod każdym innym względem: rozmiarem, kształtem, ładunkiem i stabilnością oraz podobnym wiązaniem do receptora recyklingującego, który zwykle chroni przeciwciała przed degradacją. To oznaczało, że wszelkie późniejsze różnice obserwowane w eksperymentach komórkowych czy u zwierząt można przypisać wyłącznie parowaniu glikanów, a nie ukrytym uszkodzeniom czy zanieczyszczeniom.
Obserwowanie, jak komórki pochłaniają przeciwciała
Następnie badacze sprawdzili, jak szybko każdy wzór cukrowy pozwala przeciwciałom być „połkniętym” przez komórki noszące receptor mannozowy. Oznaczyli różne frakcje przeciwciał znacznikiem fluorescencyjnym i inkubowali je z komórkami ludzkimi zaprojektowanymi do ekspresji tego receptora. Przez prawie trzy dni śledzili wewnątrzkomórkowy blask jako miarę pobierania. Wszystkie przeciwciała były w pewnym stopniu pobierane, ale tempo się różniło: te z dwoma glikanami wysokomannozydowymi były internalizowane najszybciej, z jedną jednostką wysokomannozydową miały tempo pośrednie, a te z samymi glikanami złożonymi były najwolniejsze. Gdy zespół dodał mannan — naturalny cukier konkurujący o receptor mannozowy — pobieranie przeciwciał wysokomannozydowych spadło gwałtownie, co potwierdziło, że to właśnie ten receptor odpowiada za dużą część szybkiej internalizacji.
Śledzenie przeciwciał oznaczonych cukrami u żywych zwierząt
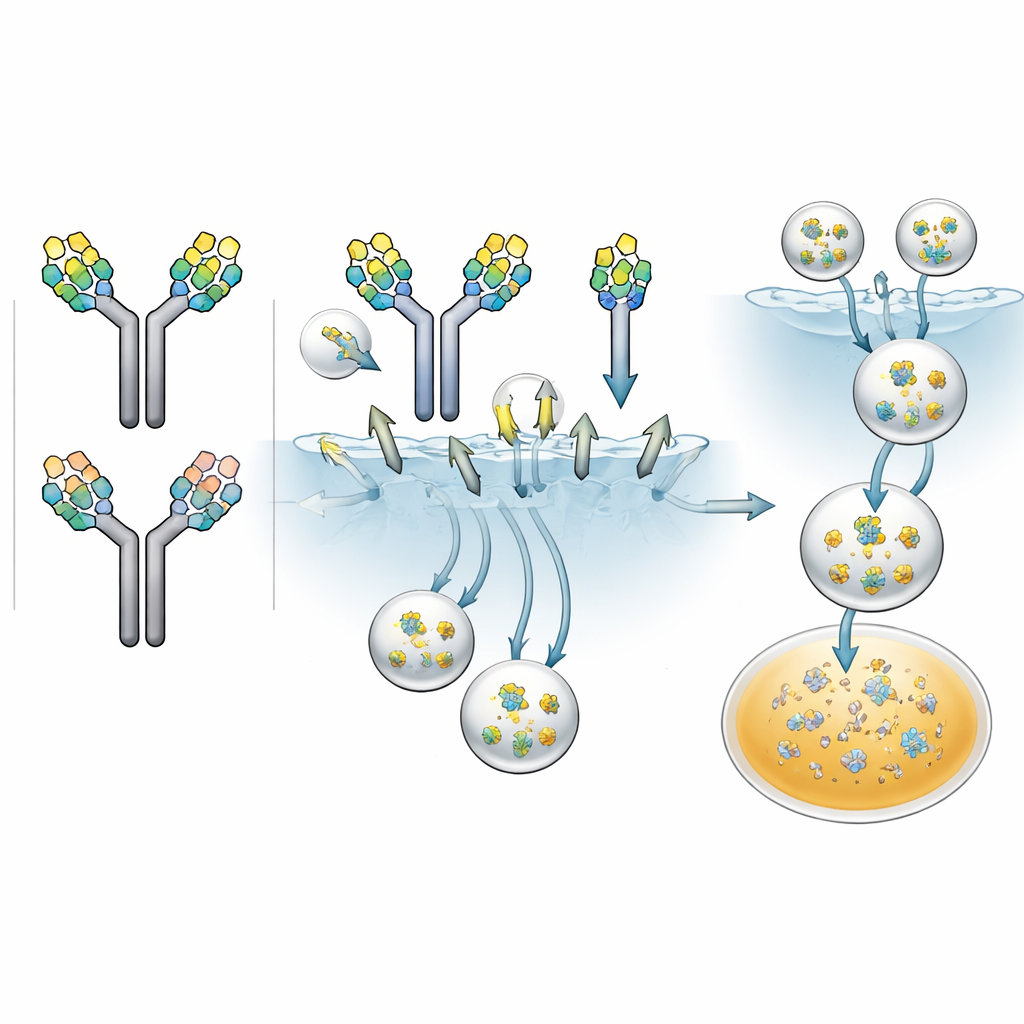
Kluczowym testem było sprawdzenie, czy te różnice komórkowe przełożą się na rzeczywiste zachowanie leku in vivo. Naukowcy przygotowali produkt leczniczy zawierający zarówno symetryczne, jak i asymetryczne pary wysokomannozydowe oraz pary złożone i wstrzyknięli go szczurzym modelom. Dzięki czułym metodom spektrometrii mas mogli śledzić nie tylko całkowite stężenie przeciwciał przez dwa tygodnie, lecz także spadek każdej pary glikanów w czasie. Wzór był wymowny: przeciwciała z dwoma glikanami wysokomannozydowymi znikały najszybciej, z okresem półtrwania około 2,4 dnia; te z jedną wysokomannozydową jednostką utrzymywały się dłużej, około 7,2 dnia; a przeciwciała z samymi glikanami złożonymi przetrwały około 17,4 dnia. Ekspozycja w czasie — pole pod krzywą stężenia — spadła do 38% dla podwójnej pary wysokomannozydowej i do 73% dla pary mieszanej w porównaniu z parą złożoną. W istocie każdy dodatkowy glikan wysokomannozydowy działał jak kolejna flaga „usuń mnie” dla receptora mannozowego.
Co to oznacza dla bezpieczniejszych, dłużej działających leków
Dla pacjentów wyniki te wyjaśniają, dlaczego dwa leki przeciwciałowe, które na papierze wyglądają podobnie, mogą inaczej zachowywać się w organizmie. Badanie pokazuje, że nie tylko obecność, ale i parowanie glikanów wysokomannozydowych silnie kieruje tempem usuwania przeciwciał, najpewniej poprzez pobieranie i rozkład zależny od receptora mannozowego wewnątrz komórek odpornościowych. Ponieważ ta sama ścieżka może także kierować antygeny do aparatów aktywujących odpowiedź immunologiczną, wzory glikanów mogą wpływać na ryzyko wytwarzania przeciwciał anty-lekowych i reakcji alergicznych. Autorzy argumentują, że producenci powinni monitorować i kontrolować parowanie glikanów — a nie tylko ich ogólny skład — podczas projektowania i testowania terapii przeciwciałowych. Taka praktyka może pomóc zapewnić bardziej przewidywalne dawkowanie, dłuższe działanie i niższe ryzyko niepożądanych reakcji immunologicznych.
Cytowanie: Baumeister, J., Meudt, M., Wei, W. et al. Selective clearance of monoclonal antibodies via the mannose receptor is dependent on glycan pairing. Sci Rep 16, 8489 (2026). https://doi.org/10.1038/s41598-026-40268-1
Słowa kluczowe: przeciwciała monoklonalne, glikozylacja, receptor mannozowy, farmakokinetyka, immunogenność