Clear Sky Science · pl
Ewolucja molekularna i różnorodność polimerazy RNA zależnej od RNA norowirusa
Dlaczego wirusy żołądkowe ciągle nas zaskakują
Norowirus to słynny wirus „grypy żołądkowej”, który potrafi w ciągu kilku dni sparaliżować rejsy wycieczkowe, szkoły i szpitale. Łatwo się rozprzestrzenia, co roku zakaża setki milionów osób i nieustannie rodzi nowe warianty. W tym badaniu prześwietlono mechanizmy tej ewolucji, skupiając się na pojedynczym enzymie wirusa — wewnętrznej „maszynie kopiującej” zwanej polimerazą RNA — aby sprawdzić, jak zmienia się w czasie i jak stabilna jest w rzeczywistości. Zrozumienie tego ukrytego silnika zmian może wyjaśnić, dlaczego niektóre szczepy norowirusa dominują na świecie, i pomóc w projektowaniu przyszłych leków przeciwwirusowych.
Wewnętrzna maszyna kopiująca wirusa
Norowirus przechowuje materiał genetyczny w postaci RNA i polega na enzymie zwanym polimerazą RNA zależną od RNA, który kopiuje to RNA w zakażonych komórkach. Enzym ten, liczący około 510 jednostek budulcowych, przypomina zgiętą dłoń z palcami, dłonią i kciukiem, tworząc kanał, przez który przechodzą RNA i nowe nukleotydy. W tej strukturze znajdują się siedem małych „ognisk” będących niemal identycznymi we wszystkich szczepach; obszary te wykonują podstawową chemię kopiowania genomu. Ponieważ polimeraza jest niezbędna do rozmnażania wirusa, nawet niewielkie zaburzenia w tych ogniskach mogą być katastrofalne dla wirusa, więc ewolucja bardzo starannie je zachowuje.
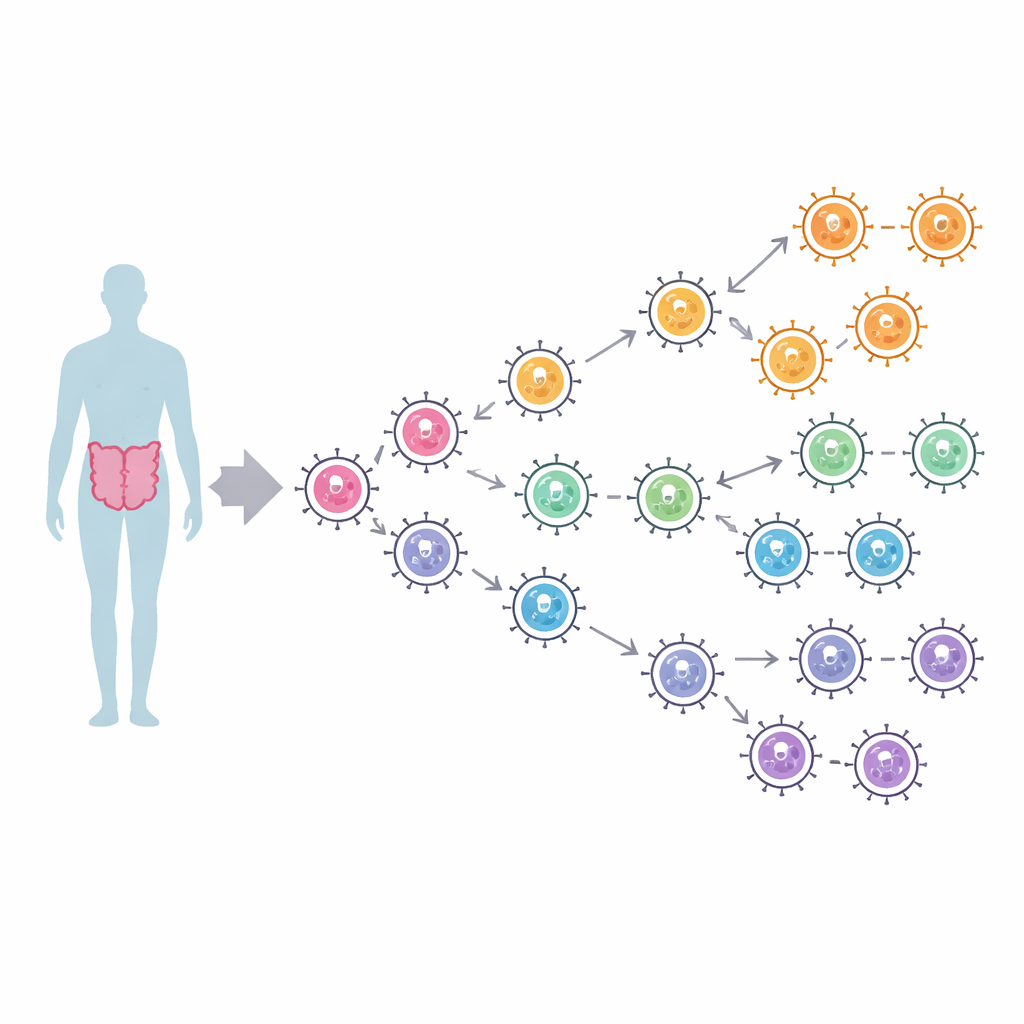
Setki szczepów, kilka kluczowych rodzin
Naukowcy zgromadzili 1 094 kompletne sekwencje polimerazy z dwóch głównych grup ludzkiego norowirusa, oznaczonych GI i GII, pobranych na całym świecie w latach 1972–2024. Korzystając z obliczeniowych drzew filogenetycznych uwzględniających daty i miejsca pobrania próbek, śledzili, jak te enzymy rozgałęziały się na przestrzeni niemal czterech wieków. Polimerazy GI podzieliły się na trzy główne linie, które prawdopodobnie zaczęły się rozdzielać już około XVII wieku, podczas gdy polimerazy GII utworzyły cztery linie, w tym odrębną gałąź dla typu znanego jako P16. Współczesne zakażenia zdominowane są przez dwa typy polimerazy GII, P16 i P31, oba historycznie powiązane z długo utrzymującym się pandemicznym genotypem kapsydu GII. Mimo globalnego rozprzestrzenienia drzewa filogenetyczne wykazały niewielkie skupienia geograficzne — szczepy z różnych kontynentów mieszają się ze sobą — co sugeruje, że norowirus szybko krąży po świecie, nie utrzymując się długo w konkretnych regionach.
Powolne, stałe zmiany i silnie chronione rdzenie
Porównując aminokwasowe jednostki budulcowe na każdej pozycji w polimerazie, zespół skatalogował tysiące zmian między typami. Stwierdzono znacznie mniej zmian w GI niż w GII, częściowo odzwierciedlając mniejszą liczbę dostępnych sekwencji, ale wyłonił się wyraźny wzór: siedem zachowanych ognisk i pobliskie miejsce wiążące RNA pozostały niemal nietknięte. Gdy zachodziły podstawienia w tych regionach, zazwyczaj były to łagodne zamiany na chemicznie podobne aminokwasy, co sugeruje, że enzym toleruje tylko bardzo subtelne modyfikacje w tych kluczowych strefach. Większość częstych zmian skupiała się w „palcach” i innych zewnętrznych rejonach enzymu, z dala od centralnej chemii. Niektóre pozycje wykazywały nawet odwracalne zmiany tam i z powrotem między różnymi typami polimerazy — znak ewolucji konwergentnej, gdy niespokrewnione szczepy dochodzą do podobnych rozwiązań.
Różne tempo dla różnych rodzin wirusów
Następnie zespół oszacował tempo ewolucji polimerazy, skupiając się na zmianach, które zmieniają aminokwasy, a więc bardziej prawdopodobnie wpływają na funkcję. Ogólnie polimerazy GII zmieniały się około cztery razy szybciej niż GI, choć obie były wolniejsze niż zewnętrzne białko kapsydu norowirusa, znane z szybkich zmian umożliwiających unikanie odporności. W obrębie każdej grupy niektóre typy polimerazy ewoluowały nieco szybciej niż inne, ale różnice były umiarkowane. Co ważne, większość pozycji w enzymie znajdowała się pod silną presją „oczyszczającą” — mutacje zakłócające funkcję były eliminowane — podczas gdy tylko niewiele miejsc wykazywało ślady pozytywnej selekcji. Gdy te miejsca podlegające pozytywnej selekcji zmapowano na trójwymiarowe modele enzymu, niemal zawsze znajdowały się one poza najsilniej zachowanymi ogniskami, choć kilka leżało wystarczająco blisko, by potencjalnie dopracować sposób wiązania RNA lub ruchy enzymu podczas kopiowania.
Co to oznacza dla przyszłych ognisk i terapii
Razem te ustalenia przedstawiają polimerazę norowirusa jako zaskakująco stabilne jądro otoczone bardziej elastycznymi regionami, które pozwalają na stopniową adaptację. Polimerazy GII, zwłaszcza te związane z historycznie pandemicznymi szczepami, ewoluują nieco szybciej, co może pomóc tym wirusom nadążać za zmieniającymi się gospodarzami i konkurencyjnymi wariantami. Mimo to głęboka konserwacja kluczowych funkcji przez stulecia sugeruje, że enzym ten jest obiecującym, stałym celem dla leków przeciwwirusowych: zakłóć podstawową maszynerię kopiowania, a wirus ma niewiele możliwości ucieczki bez samookaleczenia się. Dla osób niezajmujących się specjalistycznie tematem najważniejszy wniosek jest taki, że choć zewnętrzne powierzchnie norowirusa będą się dalej zmieniać, powodując nowe ogniska, wewnętrzny silnik napędzający te zmiany jest mocno ograniczony i naukowo możliwy do zbadania — co daje stabilny cel dla przyszłych terapii.
Cytowanie: Flint, A., Jawad, M. & Nasheri, N. Molecular evolution and diversity of the norovirus RNA-dependent RNA polymerase. Sci Rep 16, 9042 (2026). https://doi.org/10.1038/s41598-026-40248-5
Słowa kluczowe: norowirus, ewolucja wirusów, polimeraza RNA, cele przeciwwirusowe, epidemiologia molekularna