Clear Sky Science · pl
Caveolina‑1 moduluje aktywność transkrypcyjną Notch podczas dojrzewania wielorzęskowych komórek oddechowych in vitro
Dlaczego te maleńkie rzęski w drogach oddechowych mają znaczenie
Każdy oddech wciąga pył, drobnoustroje i zanieczyszczenia do dróg oddechowych. Cienka warstwa komórek działa jak samoczyszczący taśmociąg, wykorzystując rytmicznie poruszające się struktury włosopodobne, by wypychać śluz i zatrzymane cząstki na zewnątrz płuc. W tym badaniu przyglądamy się, jak ten mechanizm jest zbudowany i utrzymywany, koncentrując się na mało znanym białku błonowym — caveolinie‑1 — oraz jego współpracy z głównym przełącznikiem przeznaczenia komórkowego wewnątrz komórki. Zrozumienie tej współpracy może w przyszłości pomóc naukowcom zaprojektować lepsze terapie dla przewlekłych chorób płuc, w których wyściółka dróg oddechowych jest uszkodzona lub zaburzona.
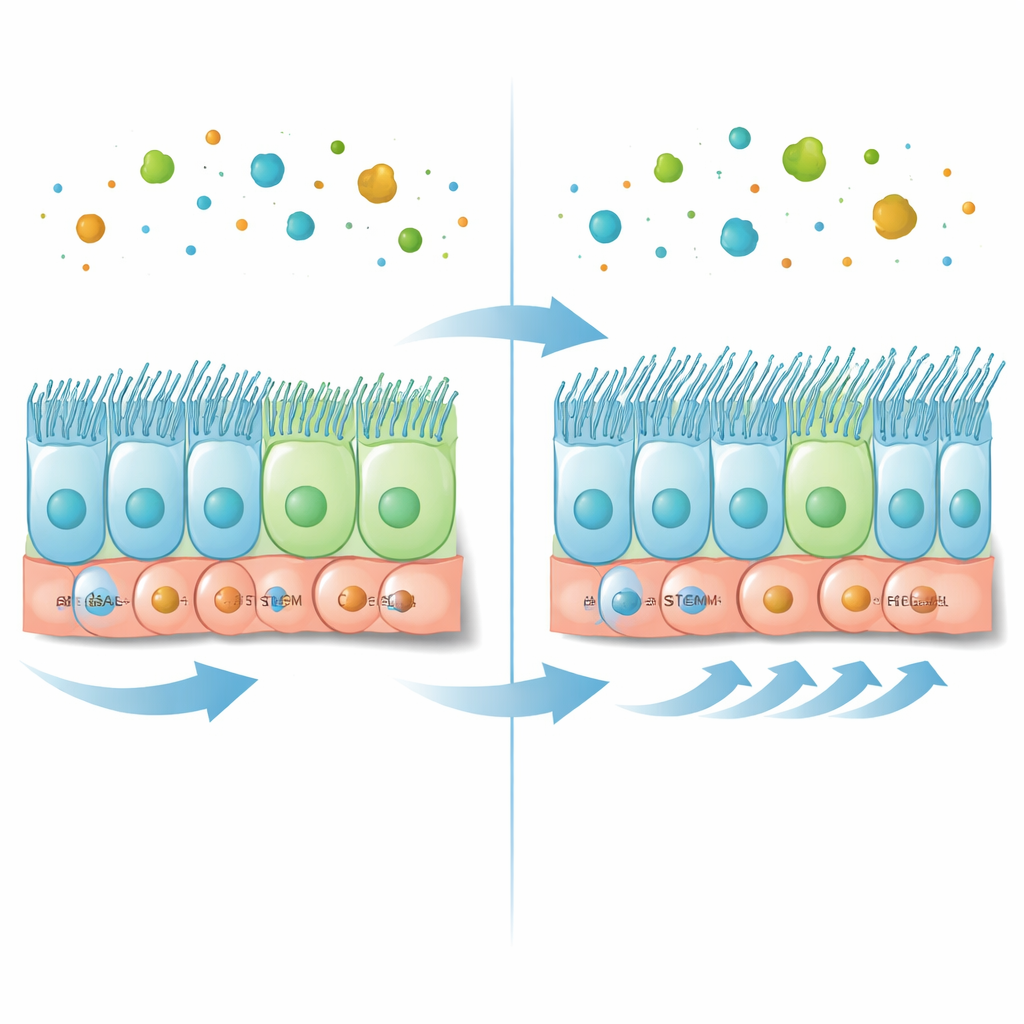
Klocki budulcowe maszyny czyszczącej drogi oddechowe
Wewnętrzna powierzchnia większych dróg oddechowych zbudowana jest z pojedynczej warstwy różnych typów komórek. U podstawy znajdują się komórki macierzyste — komórki podstawne — rezerwowy zasób, który może zarówno odnawiać się, jak i różnicować w wyspecjalizowane komórki. Niektóre ich potomne stają się komórkami wydzielniczymi produkującymi śluz, inne przekształcają się w komórki wielorzęse, pokryte licznymi poruszającymi się rzęskami, które przesuwają śluz w kierunku ust. Odpowiedni stosunek tych komórek jest niezbędny dla drożnych dróg oddechowych i prawidłowego oddychania. W wcześniejszych badaniach zauważono, że białko nazwane caveoliną‑1 jest wzbogacone w komórkach podstawnych i w komórkach wielorzęsych, ale jego dokładna rola w tej delikatnej równowadze nie była jasna.
Śledzenie ukrytego organizatora w wyściółce dróg oddechowych
W tym badaniu naukowcy przeanalizowali tkankę dróg oddechowych myszy oraz hodowle nabłonka oddechowego w laboratorium, aby namierzyć, gdzie pojawia się caveolina‑1 podczas dojrzewania nabłonka. Korzystając z mikroskopii wysokiej rozdzielczości i analiz ekspresji genów, odkryli, że caveolina‑1 występuje najobficiej w komórkach podstawnych oraz w niektórych komórkach pośrednich, które są na krawędzi przekształcenia się albo w producentów śluzu, albo w komórki wielorzęse. W miarę jak tkanka dojrzewa w hodowli, poziomy caveoliny‑1 ogólnie spadają, równocześnie z wzrostem markerów komórek wielorzęsych. Ten wzorzec sugerował, że caveolina‑1 może działać jako hamulec lub regulator dokładności podczas przejścia od komórek macierzystych do w pełni rzęskowanych komórek.
Co się dzieje, gdy hamulec zostaje zdjęty
Aby sprawdzić ten pomysł, zespół zmniejszył lub usunął caveolinę‑1 w komórkach macierzystych i obserwował, jak tworzy się wyściółka dróg oddechowych in vitro. Podstawowa organizacja i funkcja bariery nabłonkowej pozostały nienaruszone, a komórki macierzyste nadal dzieliły się normalnie. Jednak tkanki pozbawione caveoliny‑1 konsekwentnie wytwarzały więcej komórek wielorzęsych, które dojrzewały szybciej. Profilowanie ekspresji genów we wczesnym procesie różnicowania wykazało silną, wczesną aktywację programów związanych z rzęskami w sytuacji braku caveoliny‑1. Późniejsze obrazy mikroskopowe pokazały, że rzęski były dłuższe i poruszały się z większą częstotliwością, co wskazuje, że nie tylko liczba, lecz także wydajność komórek wielorzęsych była zwiększona.
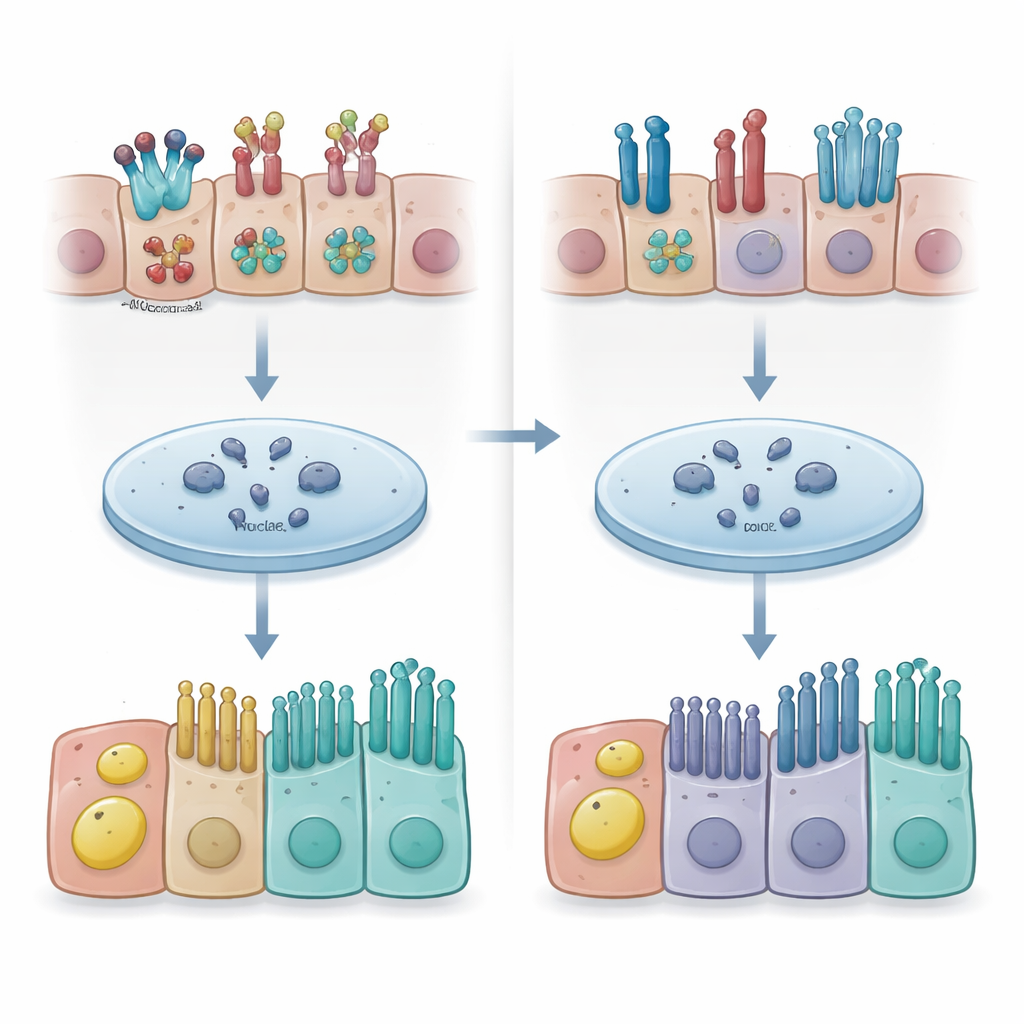
Rozmowa między błoną a komórkowym przełącznikiem decyzji
Naukowcy następnie zastanawiali się, jak caveolina‑1 może wpływać na tak szerokie zmiany losu komórki. Zwrócili się ku sygnalizacji Notch, szlakowi pełniącemu rolę komórkowej centrali: gdy jest aktywny, kieruje komórki podstawne ku losowi wydzielniczemu; gdy jest stłumiony, sprzyja powstawaniu komórek wielorzęsych. Receptory Notch osadzone są w błonie komórkowej i po aktywacji uwalniają fragment wewnątrzkomórkowy, który przemieszcza się do jądra, by regulować aktywność genów. Zespół wykazał, że w komórkach pozbawionych caveoliny‑1 wczesny sygnał Notch był osłabiony, mimo iż geny receptorów i ligandów były normalnie eksprymowane. Badania wiązania z chromatyną pokazały, że aktywny fragment Notch wiązał się z o wiele mniejszą liczbą miejsc na DNA po deplecji caveoliny‑1. Dalsze analizy biochemiczne sugerowały, że caveolina‑1 pomaga organizować przetwarzanie receptorów Notch1 i Notch2 oraz to, jak skutecznie ich aktywne fragmenty docierają do genomu i wchodzą z nim w interakcję.
Dlaczego to ma znaczenie dla zdrowia i chorób płuc
Wspólnie te odkrycia wskazują na caveolinę‑1 jako kluczowego koordynatora decyzji losu komórek macierzystych dróg oddechowych. Zamiast bezpośrednio zmieniać tempo podziałów komórek macierzystych, caveolina‑1 stroi siłę sygnalizacji Notch na początku różnicowania, co z kolei określa, ile komórek stanie się wielorzęsych i jak szybko ich rzęski dojrzeją. Gdy caveolina‑1 jest nieobecna lub zredukowana, wpływ Notch słabnie, przesuwając równowagę w stronę większej liczby i bardziej aktywnych komórek wielorzęsych. W praktycznym ujęciu praca ta ujawnia molekularną dźwignię, którą kiedyś można będzie wykorzystać, by przywrócić zdrową wyściółkę dróg oddechowych w chorobach takich jak astma, przewlekła obturacyjna choroba płuc czy mukowiscydoza, gdzie mechanizmy oczyszczające płuca są często zaburzone.
Cytowanie: Olivera-Gómez, M., Cumplido-Laso, G., Benitez, D.A. et al. Caveolin-1 modulates Notch transcriptional activity during in vitro respiratory multiciliated cell maturation. Sci Rep 16, 9165 (2026). https://doi.org/10.1038/s41598-026-40201-6
Słowa kluczowe: nabłonek dróg oddechowych, komórki wielorzęse, caveolina‑1, szlak Notch, regeneracja płuc