Clear Sky Science · pl
Multimodalna charakterystyka inicjacji i wzrostu skrzepliny wywołanej przepływem w pozaustrojowej oksygenacji membranowej
Dlaczego skrzepy krwi w urządzeniach wspomagania życia mają znaczenie
Pozaustrojowa oksygenacja membranowa, w skrócie ECMO, to rodzaj obejścia sercowo‑oddechowego, które może utrzymać przy życiu pacjentów w stanie krytycznym, dopóki ich narządy się nie zregenerują. Jednak przepuszczanie krwi przez pompy i plastikowe rurki naraża ją na ostre siły mechaniczne, do których nasze ciało nie jest przystosowane. Te siły mogą wywołać niebezpieczne skrzepy wewnątrz obwodu, co z kolei zwiększa ryzyko udaru, uszkodzenia narządów lub awarii urządzenia. Celem tego badania było ustalenie, w jaki sposób przepływ krwi przez pompę ECMO wpływa na powstawanie i rozwój tych skrzepów, z długoterminowym celem zwiększenia bezpieczeństwa i skuteczności ECMO.
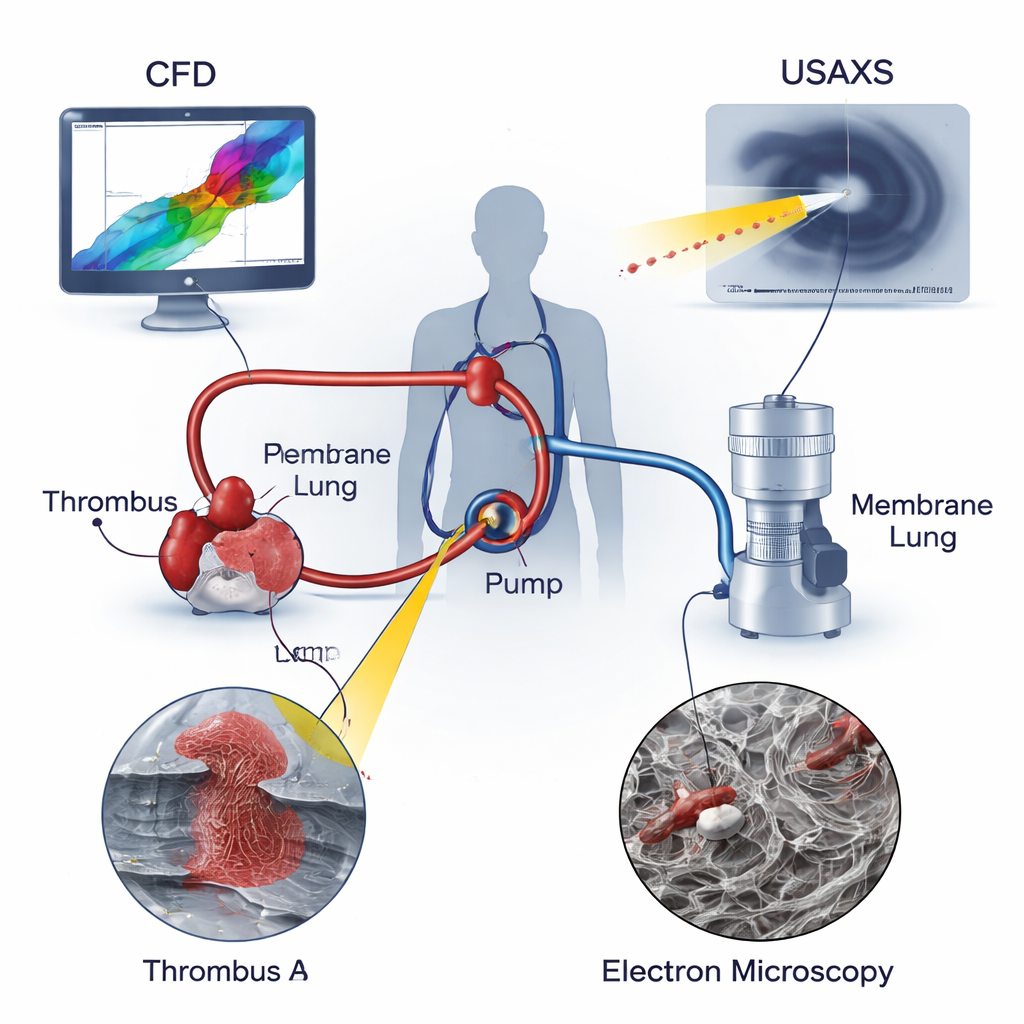
Jak ECMO podtrzymuje pacjentów przy życiu
W ECMO krew pobierana jest z dużej żyły lub tętnicy, przepychana przez pompę odśrodkową przez „płuco membranowe”, które dodaje tlen i usuwa dwutlenek węgla, a następnie zwracana do pacjenta. W odróżnieniu od płynnego przepływu w naturalnych naczyniach, w obwodzie ECMO występują ekstremalne warunki: bardzo szybkie strumienie, gwałtowne zmiany kierunku i niemal stagnujące kieszenie, w których krew zalega. Takie środowiska są znane z tego, że uszkadzają komórki krwi i pobudzają krzepnięcie. Klasyczne medyczne modele koncentrują się na wolnym lub zablokowanym przepływie w naczyniach krwionośnych, ale nie uwzględniają w pełni intensywnego ścinania i rozciągania, jakiego krew doświadcza wewnątrz wirującej pompy. Autorzy twierdzą, że aby naprawdę zrozumieć ryzyko powstawania skrzepów w ECMO, trzeba badać zarówno siły mechaniczne w urządzeniu, jak i mikroskopową strukturę powstających skrzepów.
Oglądanie skrzepów z trzech perspektyw
Naukowcy połączyli trzy potężne narzędzia, aby przeanalizować dwa rzeczywiste skrzepy pobrane z obwodów ECMO stosowanych u dzieci: jeden skrzep przy wlocie pompy (Skrzep A) i drugi w rurze tuż za pompą (Skrzep B). Obliczeniowa mechanika płynów (CFD) symulowała ruch krwi przez pompę, ujawniając obszary recyrkulacji i wirowania oraz wskazując miejsca, gdzie naprężenia ścinające i siły rozciągające osiągały maksimum. Ultra‑małokątowe rozpraszanie promieniowania rentgenowskiego (USAXS) zaglądało głęboko w każdy skrzep, mierząc, jak ciasno upakowany i jak kierunkowo ułożony jest szkielet z fibryny — białkowej sieci utrzymującej skrzepy — w całej próbce. Skaningowa mikroskopia elektronowa (SEM) dała silnie powiększone obrazy powierzchni skrzepu, ukazując kształty krwinek czerwonych, białych, płytek krwi oraz otaczających włókien fibrynowych. Nakładając te trzy obrazy, zespół mógł powiązać lokalne warunki przepływu z wewnętrzną architekturą każdego skrzepu.
Strefa recyrkulacji tworzy twardy, uporządkowany skrzep
CFD wykazało, że obszar przy wlocie pompy, gdzie utworzył się Skrzep A, zawierał strefę recyrkulacji: krew była popychana wstecz i ku górze wzdłuż obudowy, zanim dołączała z powrotem do głównego strumienia. Ten region pozwalał składnikom krwi zalegać, jednocześnie doświadczając ostrych różnic prędkości na granicy między recyrkulującym a napływającym przepływem. W Skrzepie A USAXS wskazało wysoką zawartość fibryny — co najmniej 70 procent — oraz silne ogólne uporządkowanie włókien w preferowanym kierunku, sugerując gęsty, sztywny szkielet. Obrazy SEM potwierdziły gęsto utkany układ fibryny, przeplatany nietypowo ukształtowanymi krwinkami czerwonymi i fragmentami płytek. Autorzy proponują, że połączenie długiego czasu zalegania i silnego lokalnego ścinania sprzyjało powstaniu zwartego, wysoko zorganizowanego skrzepu zdolnego wytrzymać mechaniczne obciążenia pompy.
Wirowy wypływ formuje luźniejszy, skręcony skrzep
W przeciwieństwie do tego Skrzep B, pobrany z rurki za pompą, rósł w obszarze zdominowanym przez wirowy wypływ. CFD ujawniło wirujące, spiralne struktury przepływu wychodzące z wylotu pompy, a dane USAXS wykazały sieć fibryny wciąż dominującą, lecz mniej gęstą i mniej silnie uporządkowaną globalnie. Główny kierunek orientacji fibryny przesuwał się stopniowo przez skrzep, zmieniając kąt nachylenia i odzwierciedlając skręcony wzór przepływu. Obrazy SEM pokazały nici fibrynowe o zróżnicowanej grubości oraz liczne uwięzione krwinki czerwone i białe, w tym dowody uszkodzeń komórek i stanu zapalnego. Co ważne, symulacje zidentyfikowały też niewielkie, lecz istotne części objętości pompy, gdzie siły rozciągające były wystarczająco duże, by rozwinąć czynnik von Willebranda — kluczowe białko krwi, które staje się „lepkie” pod wpływem stresu i może szybko rekrutować płytki. Strefy te koncentrowały się w pobliżu łopatek wirnika i wylotu, co czyni je prawdopodobnymi miejscami początkowej aktywacji prowadzącej do powstania Skrzepu B.
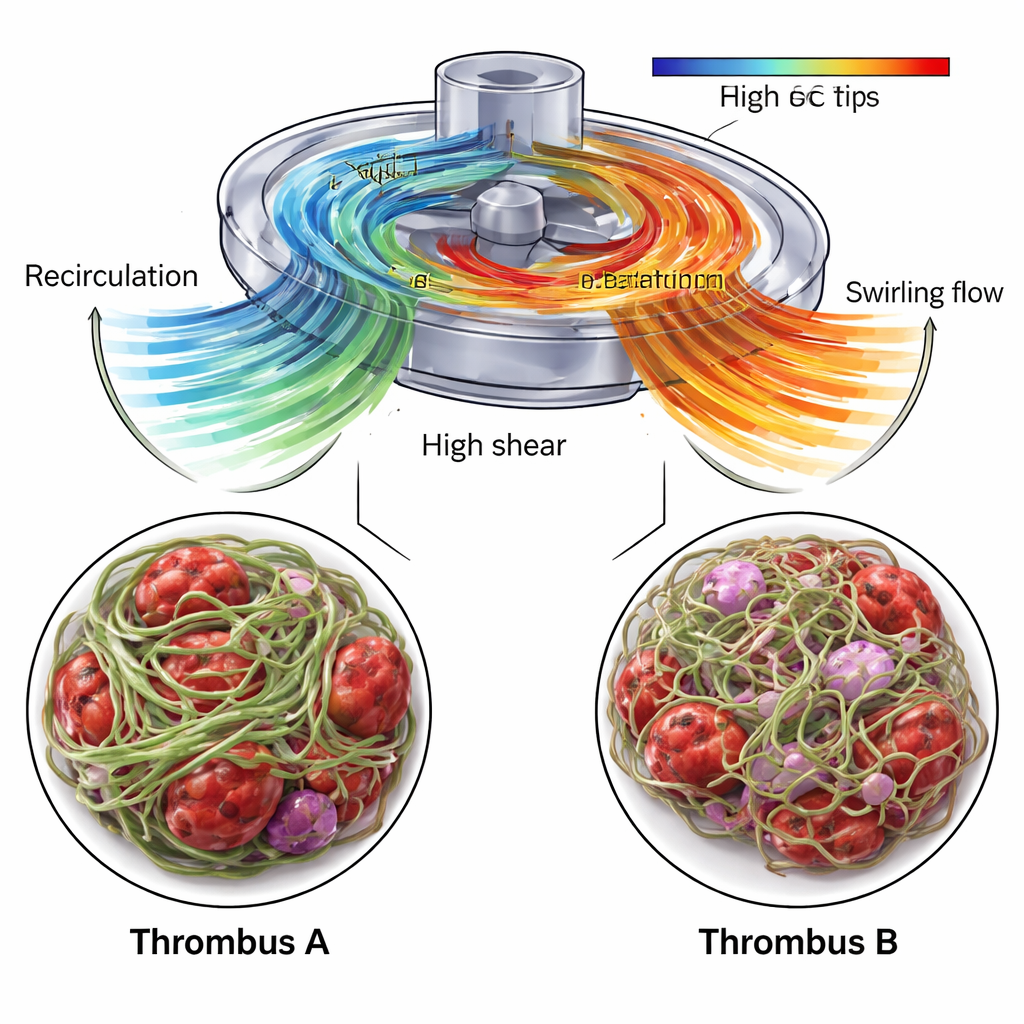
W stronę bezpieczniejszych maszyn wspomagających życie
Łącząc szczegółowe symulacje przepływu krwi z pomiarami rentgenowskimi i mikroskopem elektronowym rzeczywistych skrzepów z ECMO, praca ta pokazuje, że wewnętrzne „ustrukturyzowanie” i gęstość skrzepu odzwierciedlają mechaniczne środowisko, w którym powstał. Recyrkulujący przepływ przy wlocie pompy wiązał się z gęstym, silnie uporządkowanym szkieletem z fibryny, natomiast wirowy wypływ korelował z bardziej skręconą, otwartą siecią, która nadal uwięziła wiele komórek krwi i układu odpornościowego. Te spostrzeżenia wskazują konkretne regiony w pompach i rurach ECMO, gdzie zmiany konstrukcyjne lub celowane modyfikacje antykoagulacji mogłyby najskuteczniej zmniejszyć ryzyko skrzepów. W dłuższej perspektywie takie wieloskalowe mapowanie — od geometrii pompy i wzorców przepływu po ułożenie białek — może naprowadzić na bezpieczniejsze projekty urządzeń i pomóc klinicystom lepiej wyważyć ryzyko krwawienia i zakrzepicy podczas ratującej życie terapii ECMO.
Cytowanie: Nilsson, F., Sochor, B., Henriksson, S. et al. Multimodal characterization of flow-induced thrombus initiation and growth in extracorporeal membrane oxygenation. Sci Rep 16, 7166 (2026). https://doi.org/10.1038/s41598-026-40177-3
Słowa kluczowe: ECMO, krzepnięcie krwi, naprężenie ścinające, odśrodkowa pompa krwi, struktura fibryny