Clear Sky Science · pl
Integracja transkryptomiczna wspomagana uczeniem maszynowym identyfikuje GFM1 jako kandydacki biomarker związany z laktylacją w rozwarstwieniu aorty
Dlaczego to ukryte zagrożenie w aorcie ma znaczenie
Rozwarstwienie aorty to stan nagły, w którym pęknięcie w najważniejszej tętnicy organizmu może w ciągu kilku godzin doprowadzić do zagrażającego życiu krwotoku wewnętrznego. Lekarze często ratują pacjentów pilną operacją, ale wciąż brakuje wiarygodnych badań krwi, które wczesne ostrzegałyby przed ryzykiem, oraz leków hamujących samą chorobę. W tej pracy badano, czy subtelne zmiany w tym, jak komórki ściany naczynia gospodarują energią i sygnałami chemicznymi, mogą ujawnić nowe wczesne wskaźniki — skupiono się na mało znanym genie GFM1, który może łączyć metabolizm komórkowy z osłabieniem ściany aorty.
Zrozumieć mechanizm niebezpiecznego pęknięcia
W rozwarstwieniu aorty krew wciska się w ścianę naczynia, rozdzielając jej warstwy. Dlaczego u niektórych osób dochodzi do takiego uszkodzenia aorty, nie jest jeszcze w pełni jasne. Autorzy przeanalizowali wzory aktywności genów w próbkach od osób z rozwarstwieniem oraz od osób z prawidłową aortą. Szczególną uwagę zwrócono na geny związane z „laktylacją” — niedawno odkrytym mechanizmem, w którym laktat (znany z narastania w mięśniach podczas intensywnego wysiłku) modyfikuje białka i regulację genów. Ponieważ laktylacja powiązana jest z zapaleniem i przebudową tkanki, zespół podejrzewał, że geny związane z metabolizmem laktatu mogą odgrywać rolę w uszkodzeniu ściany aorty.
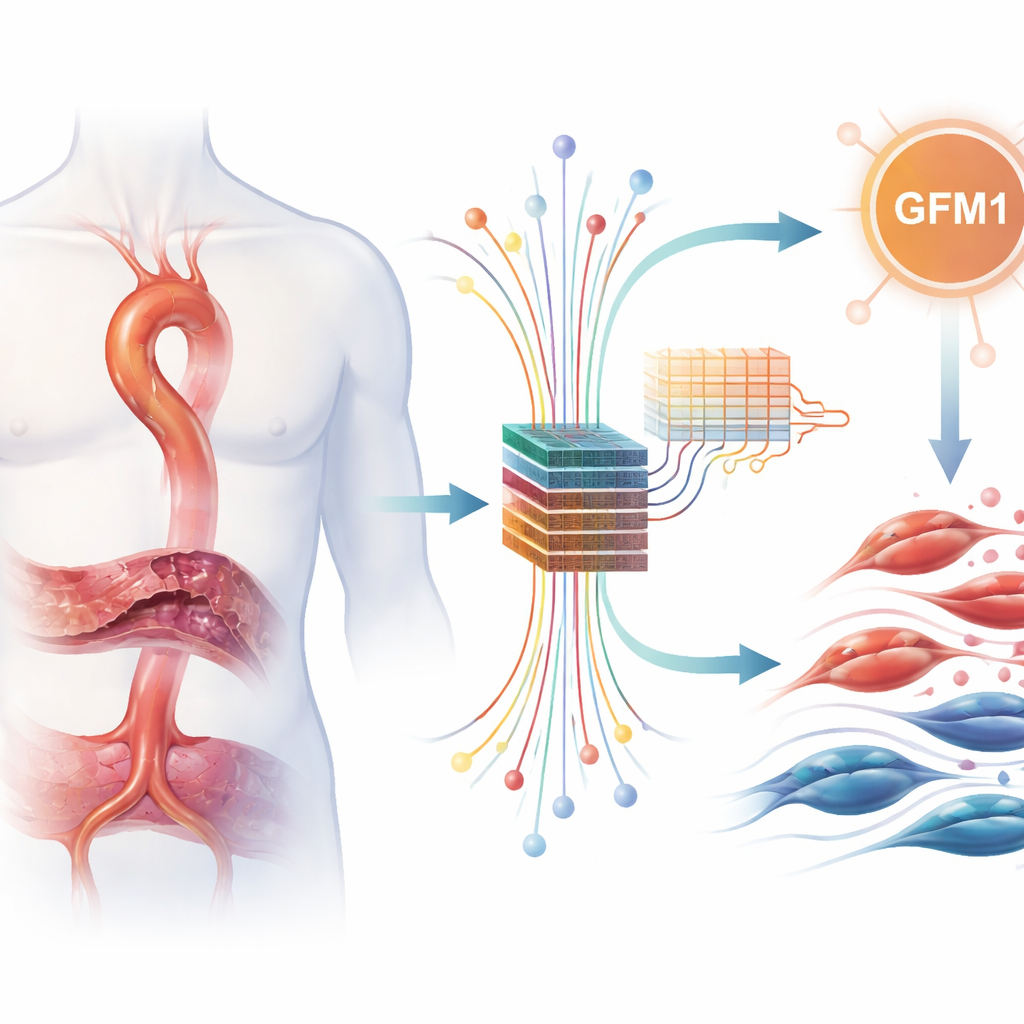
Eksploracja dużych zbiorów danych za pomocą inteligentnych algorytmów
Aby przetestować hipotezę, badacze połączyli kilka publicznie dostępnych zestawów danych dotyczących genów w tkance aorty. Dokładnie skorygowali techniczne różnice między badaniami, a następnie wyszukali geny, których aktywność konsekwentnie różniła się między próbkami chorymi a zdrowymi. Spośród tysięcy genów wybrano 217 z wyraźnymi zmianami, z których wiele wskazywało na reakcje immunologiczne i przebudowę rusztowania tkankowego wspierającego aortę. Następnie skupiono się na starannie dobranej liście genów związanych z metabolizmem laktatu i laktylacją i zidentyfikowano 11, które były zarówno zmienione w rozwarstwieniu aorty, jak i należały do tych programów związanych z laktatem.
Poddanie kluczowego podejrzanego głosowaniu maszyn
Lista 11 interesujących genów była wciąż zbyt obszerna do dogłębnych badań laboratoryjnych, więc zespół użył metod uczenia maszynowego jako obiektywnego „systemu głosowania”. Dane dla tych genów wprowadzono do trzech modeli — LASSO, Random Forest i XGBoost — powszechnie stosowanych do wyodrębniania wzorców najlepiej odróżniających pacjentów od kontroli. Każda metoda wyróżniła swoje faworyty, ale tylko jeden gen, GFM1, był silnie i konsekwentnie wybierany przez wszystkie trzy. Takie potrójne sprawdzenie sprawiło, że GFM1 wyróżnił się jako szczególnie solidny kandydat, choć modele te służyły do rankingu, a nie do budowy gotowego testu diagnostycznego.
Zbliżenie na mięśniowe komórki tętnic
GFM1 uczestniczy w kontroli, jak mitochondria — fabryki energetyczne komórek — syntetyzują własne białka. Ponieważ równowaga energetyczna jest kluczowa dla zachowania komórek ściany tętnicy, autorzy przyjrzeli się GFM1 dokładniej. Potwierdzili, że poziomy GFM1 były wyższe w tkankach pacjentów z rozwarstwieniem aorty niż w aortach bez zmian chorobowych. Następnie przeszli do kontroli in vitro, używając mysich mięśniowych komórek gładkich naczyń — komórek podobnych do mięśni, które nadają aorcie wytrzymałość. Po stymulacji tych komórek angiotensyną II, hormonem powiązanym z nadciśnieniem i stresem naczyniowym, komórki wykazywały zwiększoną proliferację i migrację, naśladując szkodliwe zmiany obserwowane w chorych naczyniach. Gdy naukowcy obniżyli poziom GFM1 za pomocą małego interferującego RNA, wzrost i migracja indukowane angiotensyną zostały wyraźnie zmniejszone, co sugeruje, że GFM1 sprzyja tym ryzykownym zachowaniom.
Co to oznacza, a czego jeszcze nie udowodniono
W sumie wyniki wskazują, że GFM1 może działać jako pomost między zmienionym metabolizmem komórkowym a agresywnym zachowaniem komórek ściany aorty w rozwarstwieniu. Mówiąc prościej: wyższa aktywność GFM1 koreluje z bardziej niestabilną, podatną na uszkodzenia aortą, a jej obniżenie w hodowlach komórkowych zmniejsza skłonność do nadmiernego wzrostu i migracji. Autorzy jednak podkreślają, że praca ta ma charakter wczesny i generuje hipotezy. Nie zmierzono bezpośrednio laktylacji w tkankach ani nie udowodniono, że sam GFM1 jest chemicznie modyfikowany w ten sposób, a zdolność predykcyjna modeli nie została sprawdzona w niezależnych grupach pacjentów. Przyszłe badania będą musiały potwierdzić te wyniki w większych kohortach i dokładnie zbadać, jak GFM1 i powiązane zmiany metaboliczne osłabiają ścianę aorty. Jeśli te wysiłki się powiodą, GFM1 lub związane z nim szlaki mogą ostatecznie stać się celami nowych testów krwi lub terapii zapobiegających temu często śmiertelnemu pęknięciu, zanim ono nastąpi.
Cytowanie: Chen, J., Jiang, N., Guo, Z. et al. Machine-learning–guided transcriptomic integration identifies GFM1 as a lactylation-related candidate biomarker in aortic dissection. Sci Rep 16, 9033 (2026). https://doi.org/10.1038/s41598-026-40139-9
Słowa kluczowe: rozwarstwienie aorty, mięśniowe komórki gładkie naczyń, metabolizm laktatu, funkcja mitochondriów, odkrywanie biomarkerów