Clear Sky Science · pl
Ciprofol łagodzi uszkodzenie niedokrwienno‑niedotlenieniowe mózgu u szczurów, hamując ferroptozę przez zwiększenie aktywności AMPK
Dlaczego ochrona mózgu po udarze ma znaczenie
Gdy osoba doświadcza udaru niedokrwiennego, lekarze śpieszą się, by udrożnić zablokowany naczynie i przywrócić przepływ krwi do mózgu. Paradoksalnie ten ratujący życie krok może sam w sobie spowodować dodatkowe uszkodzenie, zjawisko zwane urazem reperfuzyjnym. Mózg, nagle zalany tlenem i składnikami odżywczymi po okresie niedoboru, uruchamia burzę reakcji chemicznych, które mogą zabić wrażliwe komórki nerwowe. W tym badaniu sprawdzono, czy ciprofol — nowy lek znieczulający stosowany już do sedacji — może także działać ochronnie na mózg w tym krytycznym oknie, łagodząc niektóre z najbardziej szkodliwych procesów wywoływanych po przywróceniu krążenia.
Od zablokowanego przepływu krwi do uszkodzenia mózgu
Aby odtworzyć to, co dzieje się podczas ludzkiego udaru, badacze tymczasowo zablokowali główną tętnicę mózgową u szczurów, a następnie przywrócili przepływ krwi, tworząc tzw. uszkodzenie niedokrwienno‑niedotlenieniowe mózgu. Część zwierząt przeszła sam zabieg, inne otrzymały ciprofol krótko po wznowieniu przepływu. Zespół ocenił sprawność ruchową i reakcje na dotyk oraz przebadał mózgi pod kątem obszarów martwicy i uszkodzeń strukturalnych w komórkach nerwowych. Szczury leczone ciprofolem miały mniejsze obszary uszkodzeń mózgu, komórki nerwowe o zdrowszym wyglądzie oraz lepsze wyniki testów ruchowych i czuciowych niż zwierzęta nieleczone, co sugeruje, że lek złagodził najcięższe konsekwencje urazu.
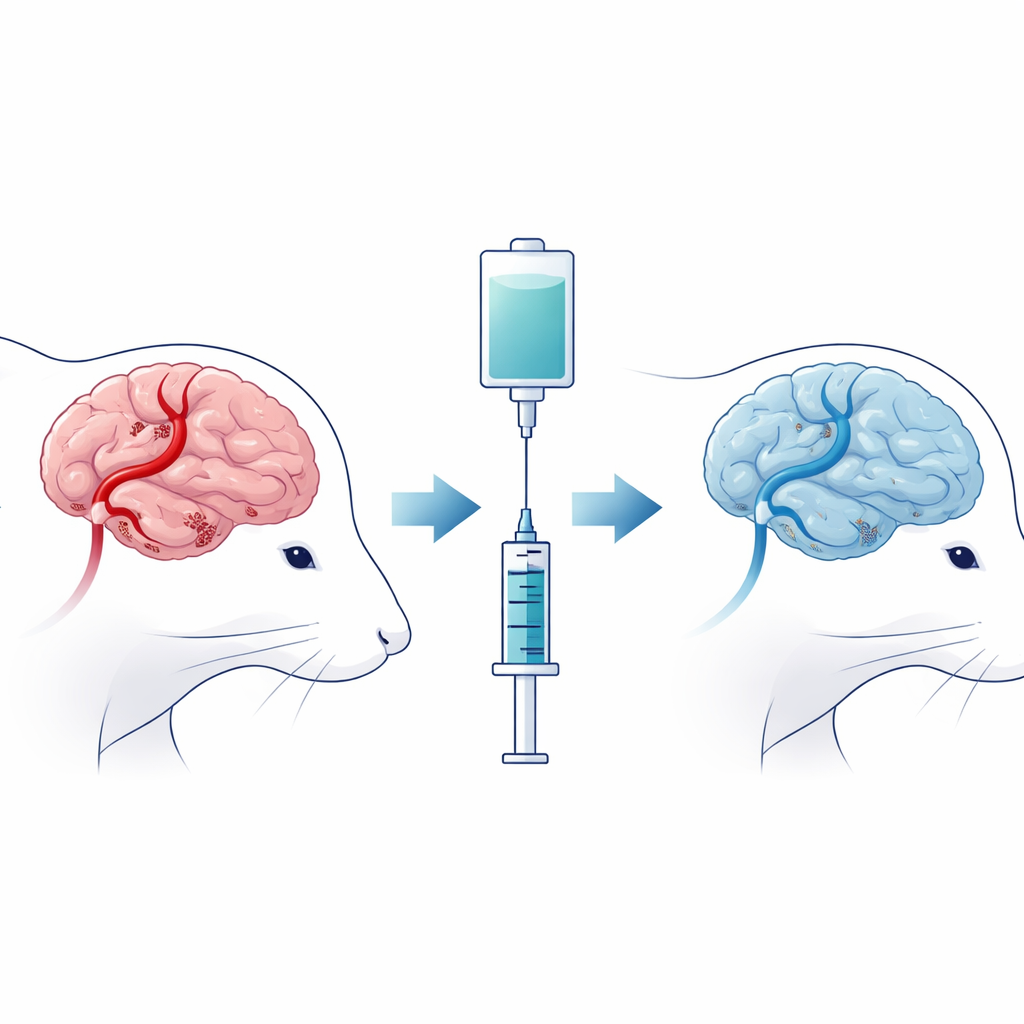
Ukryta forma śmierci komórek napędzana żelazem
Ponad widocznymi zmianami tkankowymi autorzy skupili się na niedawno rozpoznanym typie śmierci komórkowej zwanym ferroptozą, napędzanym przez żelazo i wymykające się spod kontroli reakcje chemiczne atakujące lipidowe składniki błon komórkowych. U nieleczonych szczurów w tkance mózgowej z obszaru zagrożonego wokół rdzenia uszkodzenia stwierdzono więcej żelaza, wyższe poziomy produktu rozpadu lipidów oraz mitochondria komórek nerwowych, które pod mikroskopem elektronowym wyglądały na spuchnięte i strukturalnie uszkodzone. Testy molekularne wykazały, że ochronne białka zwykle detoksyfikujące szkodliwe produkty rozpadu lipidów były zmniejszone, podczas gdy białka sprzyjające temu destrukcyjnemu procesowi były zwiększone. Ciprofol w dużym stopniu odwrócił te zmiany: spadły poziomy żelaza i uszkodzeń lipidów, równowaga kluczowych białek przesunęła się w kierunku ochrony, a mitochondria zachowały bardziej prawidłowe kształty i strukturę wewnętrzną.
Czujnik energii komórkowej jako przełącznik kontrolny
Następnie badanie zajęło się mechanizmem, dzięki któremu ciprofol wywołuje te efekty ochronne. Uwagę zwrócono na AMPK — białko działające jak czujnik energii komórkowej i responder na stres. W uszkodzonych mózgach nieleczonych szczurów aktywność AMPK była obniżona. Ciprofol zwiększył formę aktywowaną AMPK, równolegle ze spadkiem uszkodzeń związanych z ferroptozą. Aby sprawdzić, czy ten czujnik energii rzeczywiście stoi u źródła łańcucha ochronnych zdarzeń, badacze użyli innego leku, Związku C (Compound C), blokującego AMPK. Gdy zwierzęta otrzymały zarówno ciprofol, jak i ten blokujący AMPK związek, korzyści płynące z ciprofolu częściowo zniknęły: markery związane z ferroptozą zaczęły wracać do szkodliwych poziomów, kumulacja żelaza powróciła, a sygnał aktywności AMPK spadł nawet niżej niż u nieleczonych zwierząt po udarze. Ten wzorzec wspiera tezę, że aktywacja AMPK jest kluczowym krokiem w mechanizmie ochronnym ciprofolu.
Tłumienie zapalnej burzy mózgu
Uszkodzenie związane z udarem to nie tylko śmierć komórek neuronów; znaczącą rolę odgrywa też odpowiedź immunologiczna mózgu. Zespół zmierzył kilka zapalnych mediatorów, które zwykle gwałtownie rosną po niedokrwieniu‑reperfusji. U zwierząt nieleczonych sygnały te były silnie podwyższone, odzwierciedlając intensywną reakcję zapalną. Ciprofol zmniejszył wszystkie trzy główne mierzone markery zapalenia, sugerując, że nie tylko hamuje uszkodzenia błon powodowane przez żelazo, lecz także łagodzi następującą po tym burzę zapalną. Gdy AMPK został zablokowany Związkiem C, te kojące efekty na stan zapalny osłabły, ponownie łącząc korzyści ciprofolu z tą centralną ścieżką czujnika energii.
Co to może oznaczać dla przyszłej opieki
Razem wyniki wskazują na ciprofol jako coś więcej niż tylko środek sedujący: w tym modelu u szczurów wydaje się ograniczać uszkodzenia mózgu związane z udarem przez aktywację AMPK, co z kolei hamuje żelazozależną śmierć komórek i tłumi stan zapalny. Ponieważ ciprofol jest już stosowany w klinikach do znieczulenia i sedacji zabiegowej, jego dodatkowy potencjał jako środka neuroprotekcyjnego jest szczególnie intrygujący. Mimo to praca ma istotne ograniczenia, w tym poleganie na jednym modelu zwierzęcym oraz możliwość, że lek blokujący AMPK ma własne działania niepożądane. Potrzebne będą dalsze badania, w tym na innych gatunkach i ostatecznie u pacjentów, aby potwierdzić, czy ciprofol może bezpiecznie pomagać chronić mózg podczas i po leczeniu udaru.
Cytowanie: Zeng, H., Yu, X., Zheng, Z. et al. Ciprofol attenuates cerebral Ischemia‒reperfusion injury in rats by inhibiting ferroptosis through upregulating AMPK. Sci Rep 16, 9282 (2026). https://doi.org/10.1038/s41598-026-40104-6
Słowa kluczowe: udary niedokrwienne, uszkodzenie reperfuzyjne, ciprofol, ferroptoza, neuroprotekcja