Clear Sky Science · pl
Mechanizm przeciwnowotworowy oklacynibupu w chłoniaku psów
Dlaczego to ma znaczenie dla psów i ich rodzin
Chłoniak jest jednym z najczęstszych nowotworów u psów domowych. Choć chemioterapia pomaga wielu pacjentom, nie zawsze jest skuteczna i może powodować znaczne skutki uboczne. Oklacitinib, doustny lek powszechnie przepisywany psom z świądem związanym z alergicznym zapaleniem skóry, niedawno wykazał zaskakujące korzyści u niektórych psów z chłoniakiem skóry. Badanie stawia proste, lecz istotne pytanie: w jaki dokładnie sposób ten lek przeciwalergiczny może działać przeciwko komórkom nowotworowym i czy można przewidzieć, które psy mają największe szanse na korzyść?
Od leku na alergię do środka przeciwnowotworowego
Oklacitinib został opracowany, aby uspokajać nadmierne sygnały immunologiczne napędzające atopowe zapalenie skóry. Działa poprzez blokowanie rodziny molekularnych przełączników zwanych JAK, zwłaszcza JAK1, które przekazują sygnały od cząsteczek zapalnych na powierzchni komórki do jądra. Weterynarze zaczęli zauważać, że u niektórych psów z pewną postacią chłoniaka skórnego następuje poprawa po podaniu oklacitinibu, lecz przyczyny były niejasne, a odpowiedzi niekonsekwentne. Naukowcy postanowili zbadać to w kontrolowany sposób, używając hodowanych w laboratorium komórek chłoniaka pochodzących od psów oraz próbek od rzeczywistych pacjentów, aby sprawdzić, kiedy i jak oklacitinib rzeczywiście może zabijać komórki nowotworowe, a nie tylko łagodzić objawy skórne. 
Badanie komórek chłoniaka w laboratorium
Zespół przebadał jedną linię komórkową skórnego (powierzchniowego) chłoniaka psów oraz osiem dodatkowych linii chłoniaków wysokiego stopnia, reprezentujących zarówno nowotwory z komórek T, jak i B. Po ekspozycji tych komórek na oklacitinib w stężeniach podobnych do osiąganych u leczonych psów, około połowa linii komórkowych wykazała wyraźne spowolnienie wzrostu, a kilka przeszło w śmierć komórkową. Komórki wrażliwe kumulowały się w fazie spoczynkowej cyklu komórkowego i wykazywały cechy zaprogramowanej śmierci komórki, w tym aktywację białka egzekutora zwanego kaspazą-3. Natomiast inne linie chłoniaka prawie w ogóle nie reagowały w tym samym zakresie stężeń, co podkreśla, że chłoniak u psów nie jest jednorodną chorobą, lecz zbiorem biologicznie odmiennych nowotworów.
Skupienie się na wrażliwej ścieżce sygnalizacyjnej
Aby ustalić, co odróżniało guzy wrażliwe od opornych, naukowcy skoncentrowali się na szlaku sygnalizacyjnym JAK/STAT, powszechnej ścieżce przeżycia w wielu nowotworach krwi. Stwierdzili, że tylko linie komórkowe chłoniaka reagujące na oklacitinib wykazywały silną podstawową aktywację dwóch kluczowych graczy: JAK1 i STAT5. Gdy te wrażliwe komórki poddano działaniu oklacitinibu, aktywność STAT5 spadła gwałtownie, podczas gdy całkowite poziomy białek pozostawały takie same. Drugi lek hamujący JAK1 stosowany w medycynie ludzkiej, filgotinib, wywołał podobny wzorzec hamowania wzrostu i wyłączenia STAT5. Dogłębne profilowanie aktywności genów ujawniło, że oklacitinib osłabiał zestawy genów związanych z sygnalizacją JAK/STAT oraz zmniejszał ekspresję c-Myc — głównego promotora wzrostu często przejmowanego przez nowotwory — co pomaga wyjaśnić obserwowany zatrzymanie cyklu komórkowego i śmierć komórek. 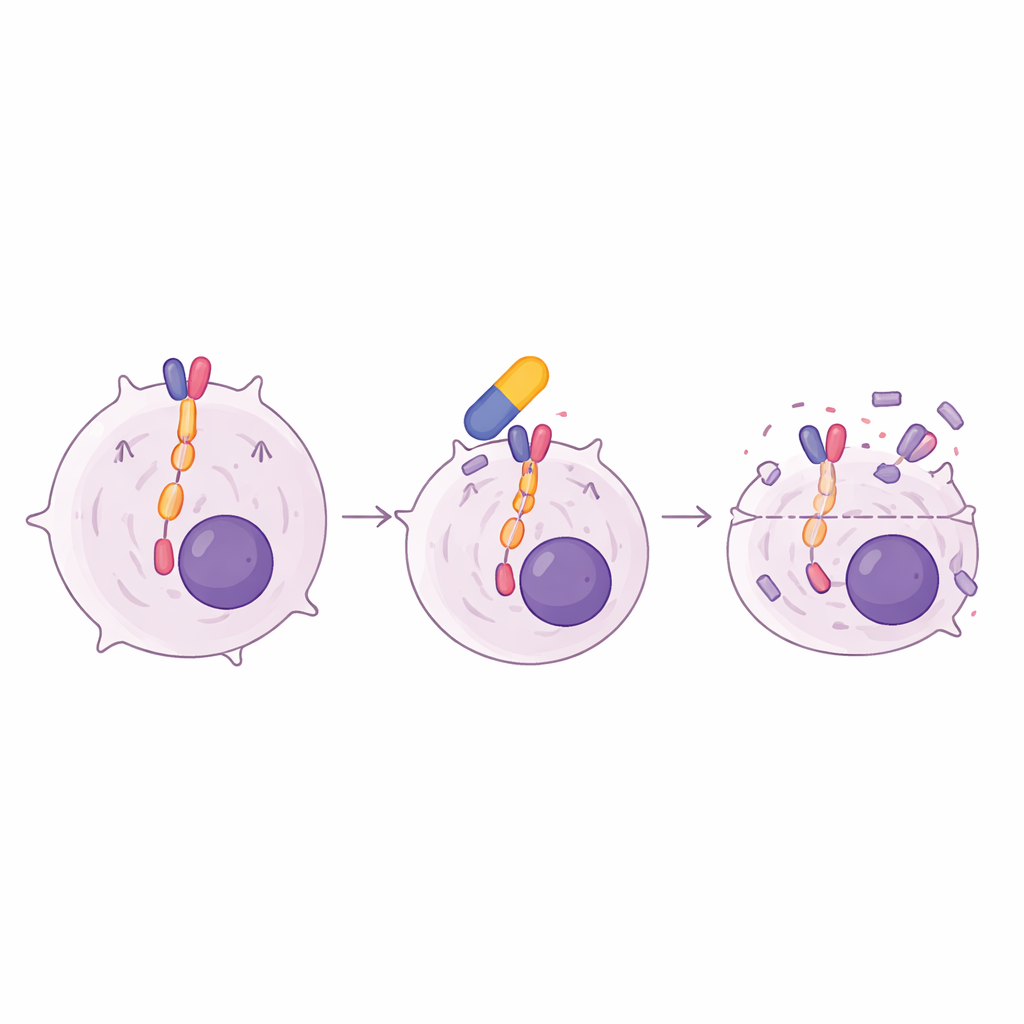
Powiązanie ustaleń z laboratorium z rzeczywistymi pacjentami
Następnie badacze sięgnęli po próbki biopsji od psów z chłoniakiem skórnym leczonych oklacitinibem w klinikach. Stosując metody barwienia uwidaczniające aktywowane białka, stwierdzili, że psy, których guzy wykazywały aktywowane JAK1 i STAT5, częściej osiągały częściowe lub całkowite odpowiedzi na lek. Niektórzy pacjenci-nieresponderzy wciąż mieli te sygnały włączone, co sugeruje, że dodatkowe drogi ucieczki mogą podtrzymywać niektóre guzy, jednak ogólny wzorzec wskazywał na silne powiązanie. Co ważne, wiele próbek chłoniaka z węzłów chłonnych i jelit od innych psów także wykazywało ten sam wzorzec aktywacji JAK1/STAT5, co otwiera możliwość, że korzyści oklacitinibu mogą wykraczać poza chłoniaka skóry i obejmować szerszy zestaw agresywnych chłoniaków psów.
Co to może znaczyć dla przyszłego leczenia
Podsumowując, praca pokazuje, że oklacitinib może bezpośrednio hamować, a czasem zabijać niektóre komórki chłoniaka psów przez wyłączenie kluczowej ścieżki przeżyciowej skoncentrowanej na JAK1 i STAT5 oraz obniżenie aktywności genów promujących wzrost, takich jak c-Myc. Prawidłowe limfocyty zdrowych psów były znacznie mniej dotknięte przy dawkach istotnych klinicznie, choć wysokie stężenia spowalniały ekspansję aktywowanych komórek immunologicznych, co podkreśla konieczność wyważenia efektów przeciwnowotworowych z ryzykiem supresji układu odpornościowego. Badanie sugeruje, że testowanie guzów pod kątem aktywowanego JAK1 i STAT5 mogłoby pomóc weterynarzom zidentyfikować psy, które najprawdopodobniej skorzystają na oklacitinibie i podobnych lekach. Mimo że potrzebne są dalsze badania kliniczne, ten szeroko dostępny lek przeciwalergiczny może stać się częścią celowanego zestawu terapii dla chłoniaka psów, kierowanego prostymi markerami molekularnymi.
Cytowanie: Harada, M., Inanaga, S., Sakurai, M. et al. The antitumor mechanism of oclacitinib in canine lymphoma. Sci Rep 16, 8427 (2026). https://doi.org/10.1038/s41598-026-40066-9
Słowa kluczowe: chłoniak psów, oklacitinib, szlak JAK1 STAT5, celowana terapia przeciwnowotworowa, onkologia weterynaryjna