Clear Sky Science · pl
MyoFuse to w pełni oparty na sztucznej inteligencji workflow do zautomatyzowanej ilościowej oceny fuzji komórek mięśni szkieletowych in vitro
Dlaczego liczenie komórek mięśniowych ma znaczenie
Kiedy ćwiczymy, regenerujemy się po urazie lub rozwijają się choroby takie jak cukrzyca, nasze mięśnie szkieletowe nieustannie się przebudowują. W laboratorium naukowcy naśladują ten proces, hodując komórki mięśniowe na szalce i obserwując, jak pojedyncze komórki zlewają się w długie, wielojądrowe włókna. Prosty wskaźnik zwany indeksem fuzji informuje ich, jak dobrze przebiega to zlewanie. Dziś jednak tę wartość zazwyczaj uzyskuje się ręcznie, licząc tysiące drobnych jąder komórkowych na ekranie — jest to praca powolna, podatna na niespójności i błędy. W tym badaniu przedstawiono MyoFuse, w pełni oparty na SI workflow, który automatyzuje to zadanie liczenia, mając na celu przyspieszenie badań nad mięśniem, zwiększenie ich niezawodności i zmniejszenie uprzedzeń.
Problem z widzeniem tego, co naprawdę jest
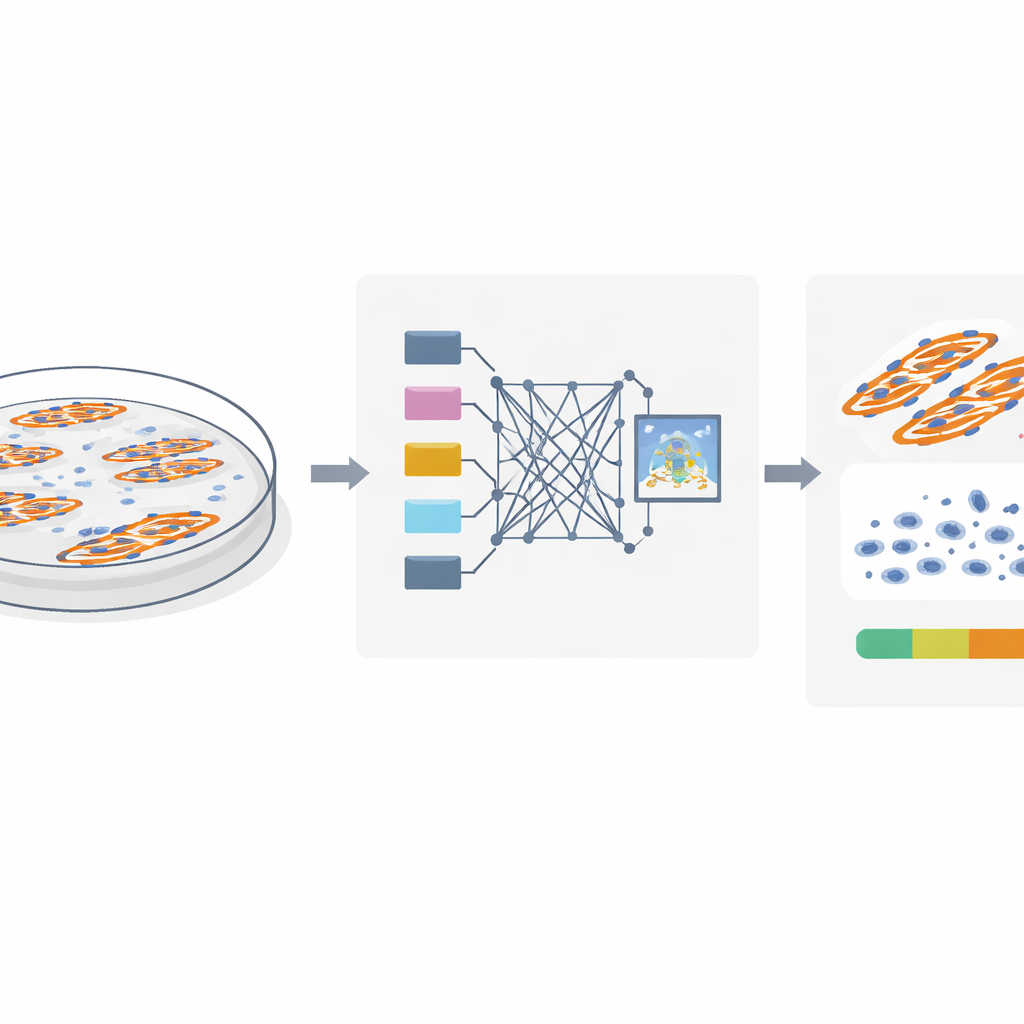
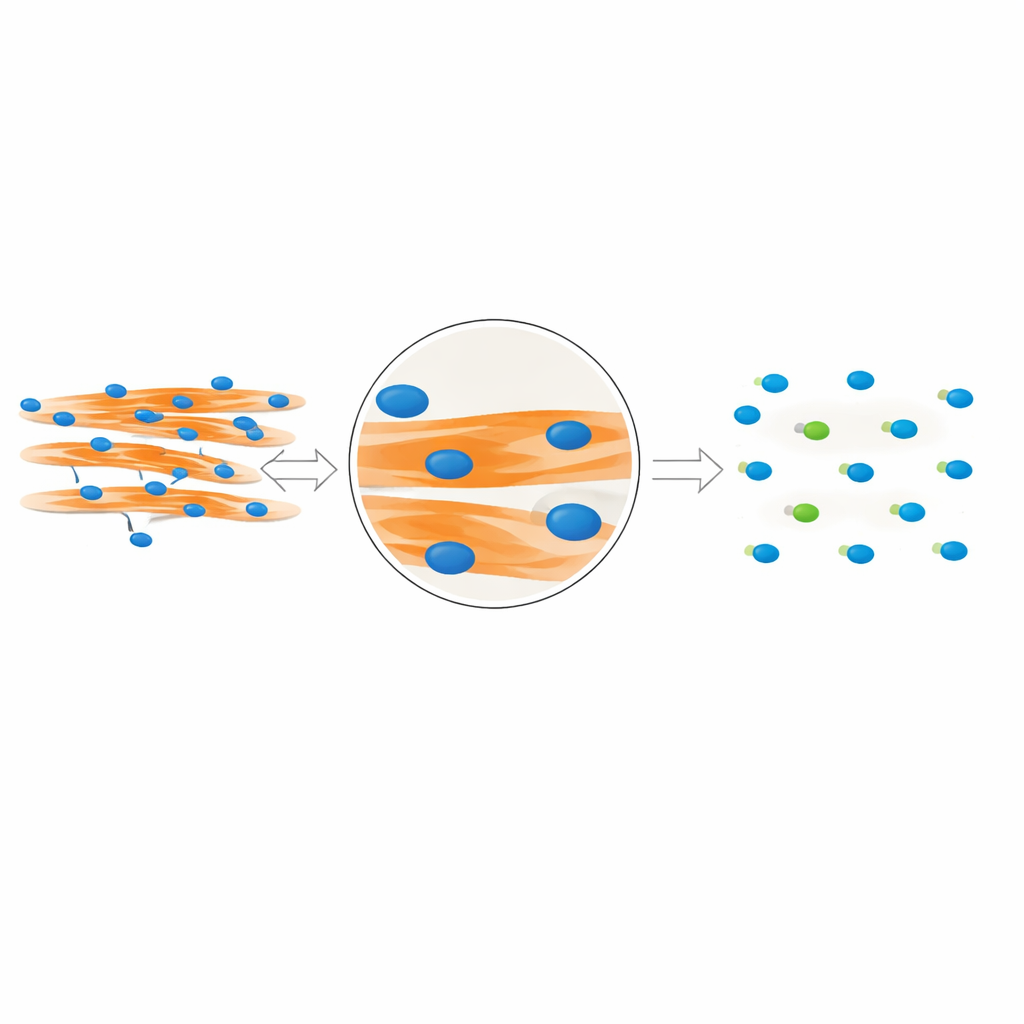
Aby badać fuzję komórek mięśniowych, badacze barwią jądra komórkowe i włókna mięśniowe barwnikami fluorescencyjnymi i wykonują zdjęcia mikroskopowe. Kluczowe pytanie brzmi, które jądra znajdują się naprawdę wewnątrz zrośniętych włókien, a które należą do niezrośniętych komórek leżących w pobliżu. Tradycyjne metody zakładają, że jeśli jądro nakłada się na włókno mięśniowe na płaskim, dwuwymiarowym obrazie, to musi ono znajdować się wewnątrz tego włókna. Jednak komórki rosną w trzech wymiarach: jądro może łatwo leżeć nad lub pod włóknem i nadal wyglądać, jakby się nakładało na obrazie. Autorzy wykorzystują szczegółowe obrazowanie konfokalne zarówno w komórkach mysich, jak i ludzkich, aby pokazać, że ten trik z nakładaniem może wprowadzać w błąd, powodując błędne zaliczanie wielu pobliskich jąder jako części zrośniętych włókien i tym samym zawyżając indeks fuzji.
Inteligentniejszy sposób odczytu obrazów fluorescencyjnych
Zespół zauważył, że prawdziwe jądra „wewnątrz włókna” zostawiają charakterystyczny wizualny ślad. Ponieważ te jądra fizycznie zajmują przestrzeń wewnątrz włókna, tworzą małe ciemne przerwy w sygnale fluorescencyjnym oznaczającym białko mięśniowe MyHC. W przeciwieństwie do tego, jądra leżące nad lub pod włóknem nie zakłócają tego sygnału. W oparciu o tę obserwację autorzy zaprojektowali MyoFuse, dwustopniowy workflow oparty na SI. Najpierw wyspecjalizowany model segmentacji (dostosowany z narzędzia open‑source Cellpose) precyzyjnie obrysowuje pojedyncze jądra, nawet gdy są ściśle zgrupowane w skupiska. Następnie lekka sieć neuronowa klasyfikuje lokalny sygnał MyHC wokół każdego jądra i decyduje, czy jądro leży wewnątrz włókna, czy na zewnątrz, opierając decyzję wyłącznie na tym lokalnym wzorze, a nie na prostym nakładaniu.
Jak dobrze SI zgadza się z ekspertami
Badacze rygorystycznie przetestowali MyoFuse na obrazach mysich komórek C2C12 oraz pierwotnych ludzkich komórek mięśniowych z różnych mięśni. Dla obu gatunków liczba jąder wyliczona przez SI oraz obliczony indeks fuzji zgadzały się bardzo dobrze ze starannymi ręcznymi adnotacjami ekspertów, z niemal doskonałą korelacją. Na poziomie pojedynczych jąder klasyfikator poprawnie rozróżniał jądra wewnątrz i na zewnątrz włókien w ponad 90% przypadków we wszystkich zestawach danych, osiągając metryki porównywalne z ludzką dyskryminacją. Co ważne, MyoFuse dobrze sprawdził się także na oddzielnym zestawie ludzkich komórek, które nigdy nie były używane do treningu, co sugeruje, że podejście może uogólniać się na nowe próbki, a nie jedynie zapamiętywać obrazy treningowe.
Ujawnianie ukrytych uprzedzeń w powszechnych metodach
Ponad dokładnością, MyoFuse ujawnił systemowe problemy w szeroko używanych metodach opartych na maskach, które polegają na prostym nakładaniu sygnałów jądrowych i włóknistych. Gdy autorzy porównali indeksy fuzji z MyoFuse z wynikami udoskonalonej metody masek zastosowanej do tych samych obrazów, metoda maskowa konsekwentnie przeszacowywała fuzję, szczególnie w obszarach, gdzie włókna mięśniowe zajmowały większą część szalki. Dostosowanie progów wykrywania zmieniało liczby, ale nie usuwało tego podstawowego uprzedzenia; pozorne poprawy często wynikały z błędów nawzajem się znoszących, a nie z lepszego odzwierciedlenia biologii. Zespół pokazał też, że estymaty fuzji mogą znacznie różnić się w różnych regionach jednej studzienki, co podkreśla, że analizowanie tylko kilku ręcznie wybranych pól może dać zniekształcony obraz rzeczywistego stopnia zlewania komórek.
Co to oznacza dla przyszłych badań nad mięśniami
MyoFuse oferuje biologom mięśni narzędzie do pomiaru fuzji komórek, które jest zarówno szybsze, jak i wierniejsze temu, co faktycznie dzieje się na szalce. Poprzez połączenie zautomatyzowanej mikroskopii z SI, która potrafi segmentować i klasyfikować setki tysięcy jąder w ciągu kilku minut, workflow zmniejsza nakład pracy ludzkiej, minimalizuje subiektywne decyzje o tym, gdzie patrzeć i jak progować obrazy, oraz unika liczenia pobliskich komórek jako zrośniętych mięśni. Autorzy przyznają, że ekstremalne warunki obrazowania lub bardzo odmienne protokoły barwienia mogą wymagać retreningu, ale metoda jest udostępniona otwarcie i zaprojektowana tak, by dało się ją dostosować. Dla laboratoriów badających rozwój mięśni, starzenie, regenerację czy choroby metaboliczne, MyoFuse obiecuje bardziej odporne pomiary fuzji — a wraz z nimi bardziej wiarygodne wnioski o tym, jak mięśnie rosną i się zmieniają.
Cytowanie: Lair, B., Cazorla, C., Lobeto, A. et al. MyoFuse is a fully AI-based workflow for automated quantification of skeletal muscle cell fusion in vitro. Sci Rep 16, 9387 (2026). https://doi.org/10.1038/s41598-026-40047-y
Słowa kluczowe: mięsień szkieletowy, fuzja komórek, sztuczna inteligencja, analiza obrazów, miogeneza