Clear Sky Science · pl
Dynamiczne zmiany aktynowe zależne od kaldesmonu‑1 są niezbędne do osteogenicznej różnicowania miąższu komórek śródzastawkowych aorty
Dlaczego usztywnienie zastawki serca ma znaczenie
W miarę starzenia się u jednej z głównych bram serca — zastawki aortalnej — tkanka może stopniowo stawać się sztywna i twarda jak skała. Ten stan, nazywany stenozą aortalną, zmusza serce do cięższej pracy i może prowadzić do niewydolności serca. Obecnie jedynymi pewnymi metodami leczenia są zabiegi chirurgiczne lub przezcewnikowe wymiany zastawki. Badanie streszczone tutaj stawia podstawowe, lecz kluczowe pytanie: co sprawia, że miękka, elastyczna tkanka zastawki stopniowo przekształca się w materiał przypominający kość? Odkrycie istotnego molekularnego gracza w tym procesie wskazuje drogę do przyszłych leków, które mogłyby spowolnić lub nawet zapobiec zwapnieniu zastawki, zamiast jedynie wymieniać zniszczoną zastawkę.
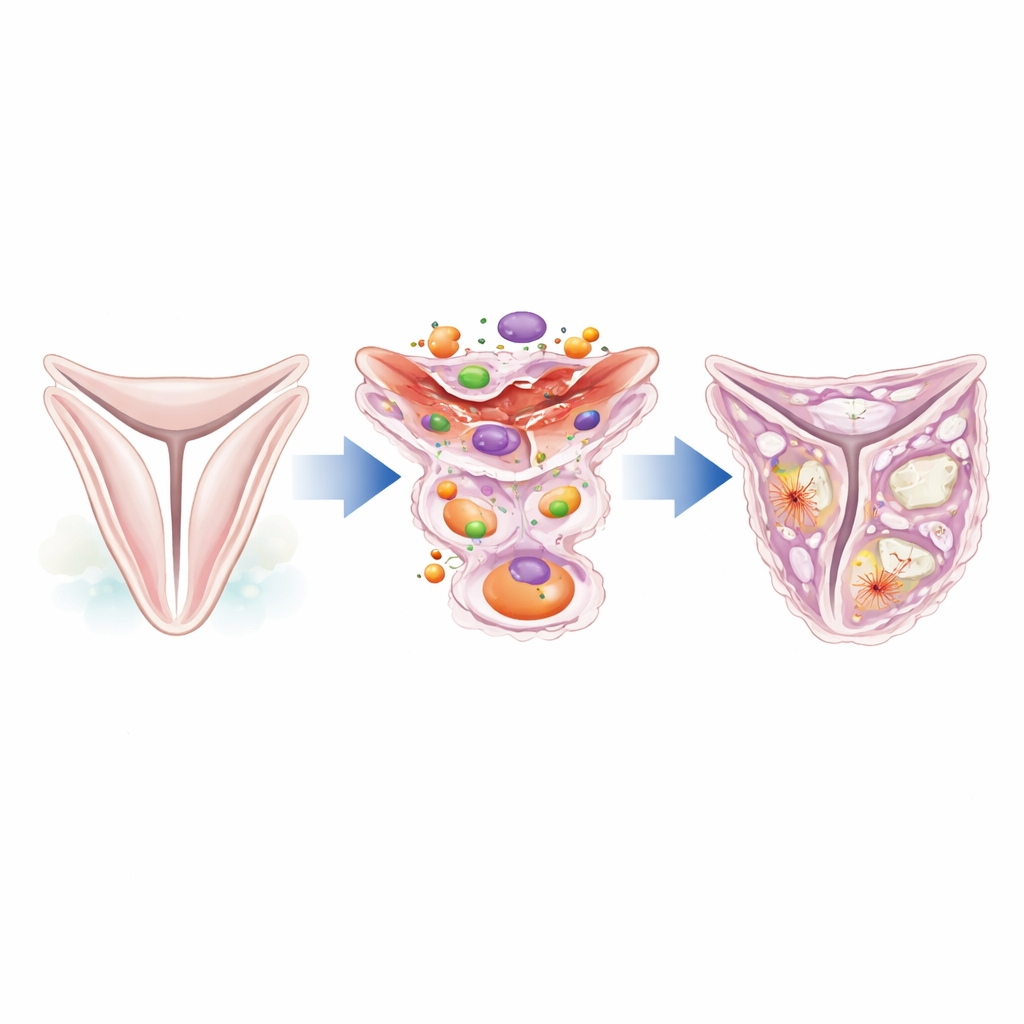
Bliższe spojrzenie na ukrytych pracowników zastawki
Płatki zastawki aortalnej wspierane są przez cienką warstwę wyspecjalizowanych komórek podporowych, nazywanych komórkami śródzastawkowymi. W zdrowej zastawce te komórki pozostają w stanie spoczynku i pomagają utrzymywać strukturę tkanki. Pod wpływem stresu lub urazu mogą jednak zmienić tożsamość i zacząć zachowywać się jak komórki tworzące blizny lub nawet jak komórki tworzące kość. Autorzy skupili się na białku zwanym kaldesmon‑1, które pomaga kontrolować wewnętrzne rusztowanie komórek zbudowane z filamentów aktynowych. Analizując istniejące dane z pojedynczych komórek (single‑cell RNA sequencing) pochodzące z ludzkich zastawek, stwierdzili, że poziom kaldesmonu‑1 jest znacznie podwyższony w zastawkach pacjentów ze stenozą aortalną w porównaniu z zastawkami prawidłowymi, szczególnie wśród komórek śródzastawkowych zlokalizowanych w pogrubionych, włóknistych obszarach.
Z elastycznej tkanki w kierunku włóknistych i kostnych ognisk
Badania mikroskopowe ludzkich próbek zastawki wykazały, że białko kaldesmon‑1 jest obficie obecne w chorych płatkach i koreluje z markerami aktywowanych, kurczliwych komórek oraz komórek podobnych do fibroblastów produkujących kolagen. Komórki bogate w kaldesmon‑1 skupiają się wokół obszarów włóknienia i wczesnego zwapnienia, co sugeruje, że uczestniczą w budowie dodatkowej macierzy, która pogrubia zastawkę. Dalsza analiza wykazała, że te komórki ekspresjonują geny typowe dla typów komórek przypominających mięśnie gładkie i skłonnych do osteogenezy, i są głównymi producentami białek strukturalnych, takich jak kolagen typu I. Innymi słowy: gdziekolwiek zastawka się usztywnia i bliznuje, obecne są komórki śródzastawkowe pozytywne względem kaldesmonu‑1.
Jak białko kształtujące wpływa na kierunek ku kości
Aby zrozumieć związek przyczynowo‑skutkowy, zespół wyizolował ludzkie komórki śródzastawkowe i zastosował małe interferujące RNA, by obniżyć poziom kaldesmonu‑1. Bez tego białka komórki traciły wydłużony, wrzecionowaty kształt i stawały się bardziej zaokrąglone. Ich wewnętrzne filamenty aktynowe przerzedzały się, a zdolność do dzielenia się i poruszania w sposób zorganizowany malała. Po wystawieniu tych komórek na osteogeniczne, czyli stymulujące powstawanie tkanki kostnej, warunki hodowlane, komórki normalne chętnie tworzyły złogi wapnia, natomiast komórki pozbawione kaldesmonu‑1 wykazywały znacznie mniejsze odkładanie minerałów. Dużej skali sekwencjonowanie RNA potwierdziło, że wiele genów zaangażowanych w tworzenie kości i przebudowę tkanki, w tym dobrze znane promotory osteogenezy jak RUNX2 i fosfataza alkaliczna, było silnie aktywowanych przez warunki osteogeniczne, lecz nie ulegało zwiększeniu po obniżeniu poziomu kaldesmonu‑1.
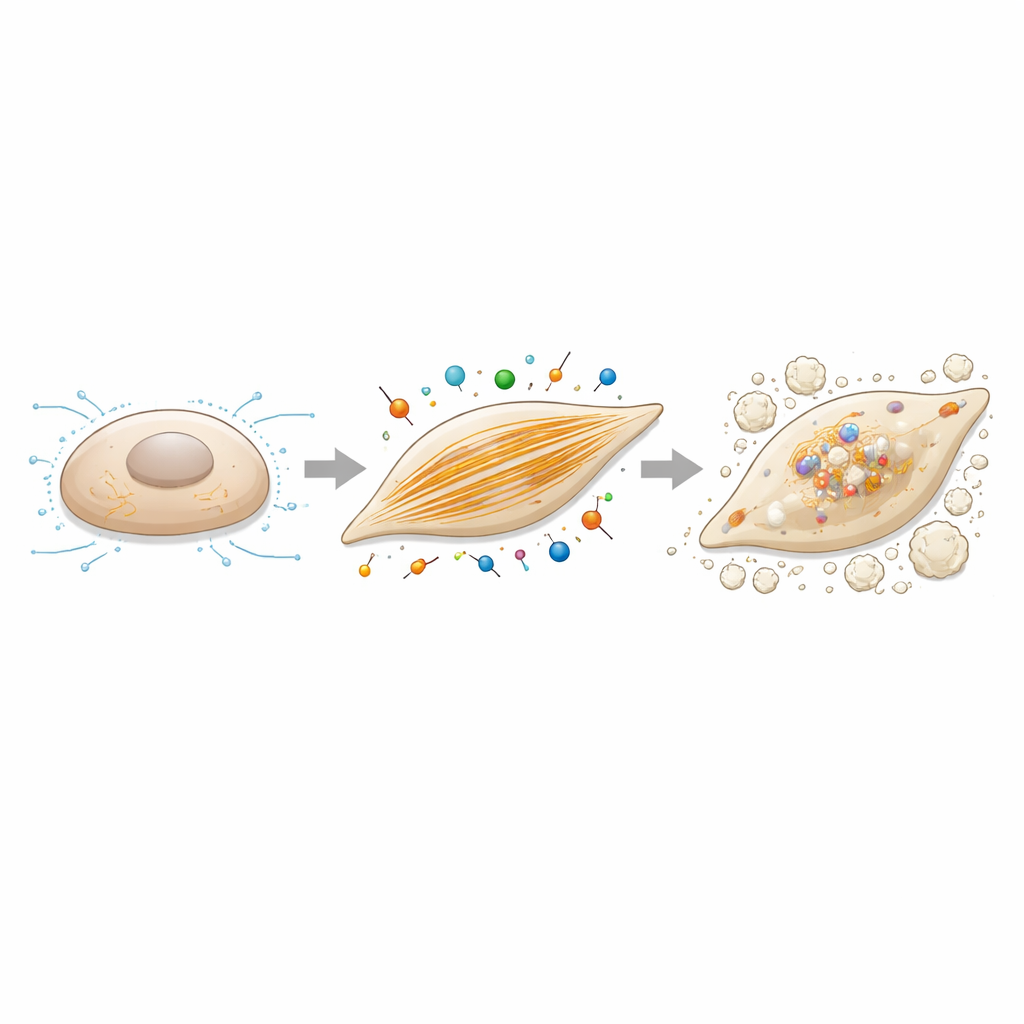
Filamenty aktynowe jako dźwignia kontroli zwapnienia
Ponieważ kaldesmon‑1 reguluje aktynę, autorzy zapytali następnie, czy zmiana montażu aktynowych filamentów sama w sobie zmieni skłonność komórek do zwapnienia. Leczyli komórki śródzastawkowe cytochalazyną B, związkiem umiarkowanie zaburzającym wzrost filamentów aktynowych, stosując jednocześnie te same warunki promujące powstawanie kości. W dawkach, które nie uszkadzały istotnie przeżywalności komórek, to leczenie wyraźnie zmniejszyło odkładanie wapnia i obniżyło ekspresję genów związanych z kostnieniem, w tym kaldesmonu‑1 i RUNX2. W połączeniu z eksperymentami wyciszania genów, wyniki te tworzą spójny obraz: rozbudowane sieci filamentów aktynowych i siły kurczliwe, które one wspierają, nie są biernymi obserwatorami — aktywnie napędzają przełączanie komórek z roli cichych komórek podporowych w komórki tworzące tkankę kostną w zastawce.
Co to oznacza dla przyszłych terapii
Dla osoby niebędącej specjalistą główny wniosek jest taki, że usztywnienie zastawki aortalnej to proces aktywny i regulowany, a nie jedynie „zużycie”. To badanie identyfikuje kaldesmon‑1 jako centralnego koordynatora łączącego wewnętrzny szkielet komórkowy z programem genetycznym produkcji tkanki przypominającej kość. Poprzez wspieranie przyjęcia przez komórki śródzastawkowe tożsamości kurczliwej, włóknistej, a ostatecznie osteogenicznej, kaldesmon‑1 przyczynia się bezpośrednio do gromadzenia twardych złogów, które zwężają zastawkę. Chociaż każda terapia ukierunkowana na to białko lub dynamikę aktyny będzie wymagać ostrożnych badań, aby uniknąć niepożądanych efektów w innych tkankach, szlaki zależne od kaldesmonu‑1 wyróżniają się jako obiecujące kandydaty do leków mających spowolnić lub zatrzymać zwapnianie zastawki zanim konieczna będzie operacja.
Cytowanie: Komoda, M., Sakaue, T., Nakao, Y. et al. Caldesmon-1–mediated actin dynamics is essential for osteogenic differentiation of aortic valve interstitial cells. Sci Rep 16, 9385 (2026). https://doi.org/10.1038/s41598-026-39938-x
Słowa kluczowe: zwapnienie zastawki aortalnej, kaldesmon‑1, komórki śródzastawkowe, cytoszkielet aktynowy, osteogeniczne różnicowanie