Clear Sky Science · pl
Inteligentne ramy opieki zdrowotnej do diagnozowania raka wątrobowokomórkowego oparte na agregowanych uczniach z danych biomedycznych wykorzystujących wyjaśnialną sztuczną inteligencję
Dlaczego inteligentniejsze badania w kierunku raka wątroby są ważne
Rak wątroby, zwłaszcza powszechny jego typ — rak wątrobowokomórkowy, często rozwija się cicho, aż staje się trudny do leczenia. Lekarze już gromadzą bogaty zestaw rutynowych wyników badań pacjentów, ale przekształcenie tych wszystkich liczb w wczesne ostrzeżenie jest trudne. Badanie to analizuje, jak zaawansowane programy komputerowe mogą przesiać codzienne dane medyczne, by wskazać pacjentów o wysokim ryzyku, jednocześnie wyjaśniając swoje rozumowanie w sposób, któremu lekarze mogą zaufać.
Przekształcanie rutynowych badań w wczesne ostrzeżenia
Naukowcy koncentrują się na pacjentach z przewlekłymi problemami wątroby, którzy są obarczeni większym ryzykiem rozwoju poważnego raka wątroby. Zamiast polegać na drogich skanach czy skomplikowanych badaniach genetycznych, wykorzystują standardowe pomiary kliniczne — takie jak biochemia krwi, enzymy wątrobowe i podstawowe informacje o stanie zdrowia. Pomiary te są najpierw starannie przeskalowane tak, aby wszystkie cechy mieściły się w tym samym zakresie liczbowym. Ten prosty, ale istotny krok oczyszczania pomaga modelom komputerowym rzetelniej uczyć się wzorców i zapobiega, by pojedyncza niezwykle duża wartość zdominowała prognozy.
Wiele cyfrowych „drugich opinii” działających razem
Zamiast polegać na jednym algorytmie, zespół tworzy ensemble, czyli zespół trzech różnych modeli uczenia głębokiego. Jeden model kompresuje dane, aby odkryć najbardziej informatywne kombinacje cech. Drugi model został zaprojektowany do rozpoznawania wzorców rozwijających się jak sekwencje, wychwytując, jak kilka pomiarów razem może sugerować ryzyko. Trzeci model łączy kilka prostych warstw, aby uchwycić skomplikowane, nieliniowe zależności ukryte w danych. Każdy model wydaje własny osąd, czy pacjent należy do grupy wysokiego czy niskiego ryzyka, a wyższej rangi łącznik waży i scala te opinie w jedną ostateczną decyzję.
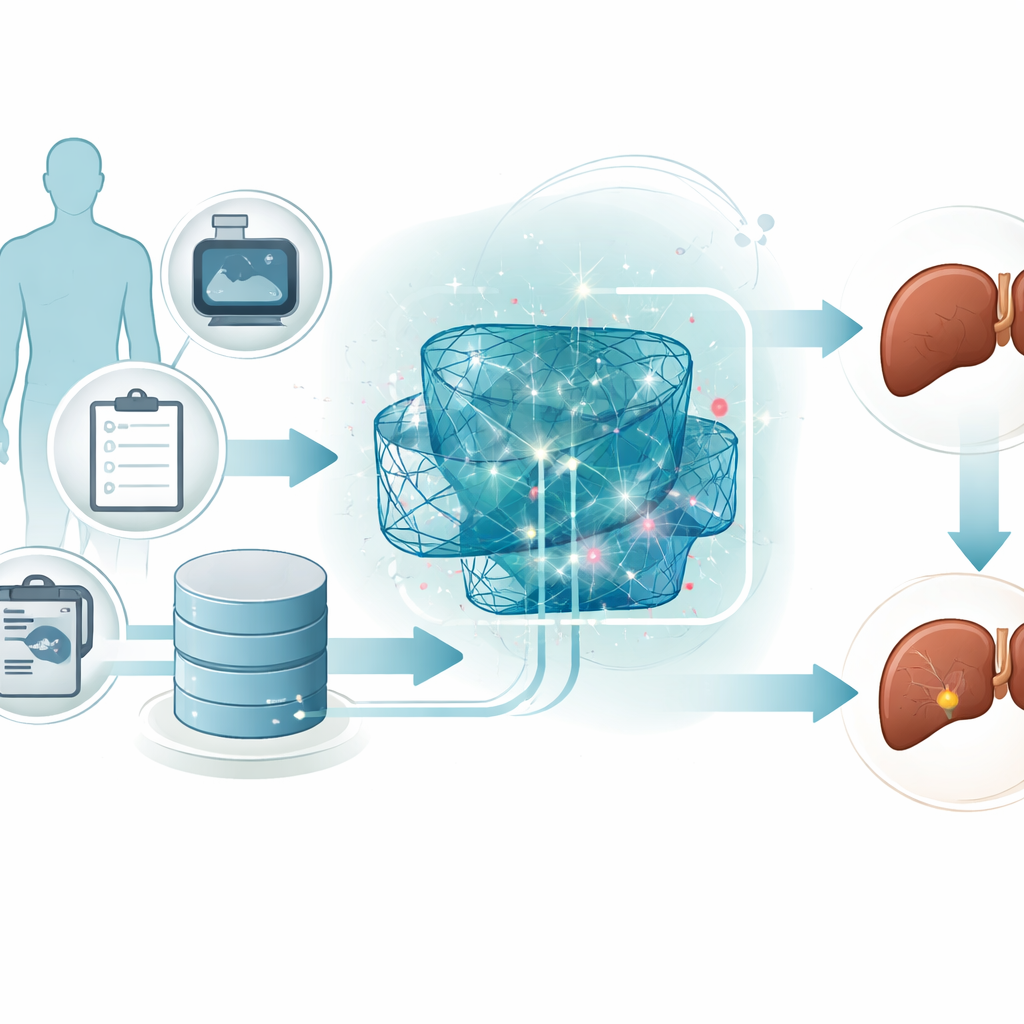
Otwieranie czarnej skrzynki dla lekarzy
Mimo swojej mocy systemy uczenia głębokiego często są krytykowane za działanie jak tajemnicze „czarne skrzynki”. Aby temu zaradzić, autorzy dodają warstwę wyjaśnialnej sztucznej inteligencji opartą na metodzie znanej jako SHAP. Technika ta szacuje, jak bardzo każda cecha wejściowa przesuwa indywidualną prognozę w kierunku bezpieczniejszego lub bardziej ryzykownego wyniku. Na przykład pewne poziomy enzymów wątrobowych, markery funkcji wątroby i oznaki rozsiewu poza wątrobę okazują się szczególnie wpływowe. Lekarze mogą zobaczyć nie tylko to, że system oznaczył pacjenta jako wysokiego ryzyka, ale też które konkretne pomiary wpłynęły na tę decyzję i w jakim kierunku, tworząc bardziej przejrzyste partnerstwo między klinicystą a maszyną.
Jak dobrze działa to podejście?
Zespół testuje swoje ramy na publicznym zestawie danych obejmującym 165 pacjentów obserwowanych przez co najmniej rok, z etykietami przeżył/nie przeżył. Pomimo skromnej wielkości zbioru danych, model złożony uczy się rozdzielać pacjentów wysokiego i niskiego ryzyka z uderzającą dokładnością: w końcowych etapach treningu poprawnie klasyfikuje około 98 na 100 przypadków. W porównaniu z szeregiem istniejących metod — w tym klasycznymi modelami statystycznymi i kilkoma nowoczesnymi sieciami neuronowymi — podejście to nie tylko dorównuje lub przewyższa ich dokładność, precyzję i równowagę między przegapieniami a fałszywymi alarmami, ale robi to także przy stosunkowo niskim czasie obliczeniowym. Badanie ablacjne, w którym trzy komponenty testuje się osobno, pokazuje, że każdy wnosi wartość, jednak ich kombinacja wypada najlepiej.
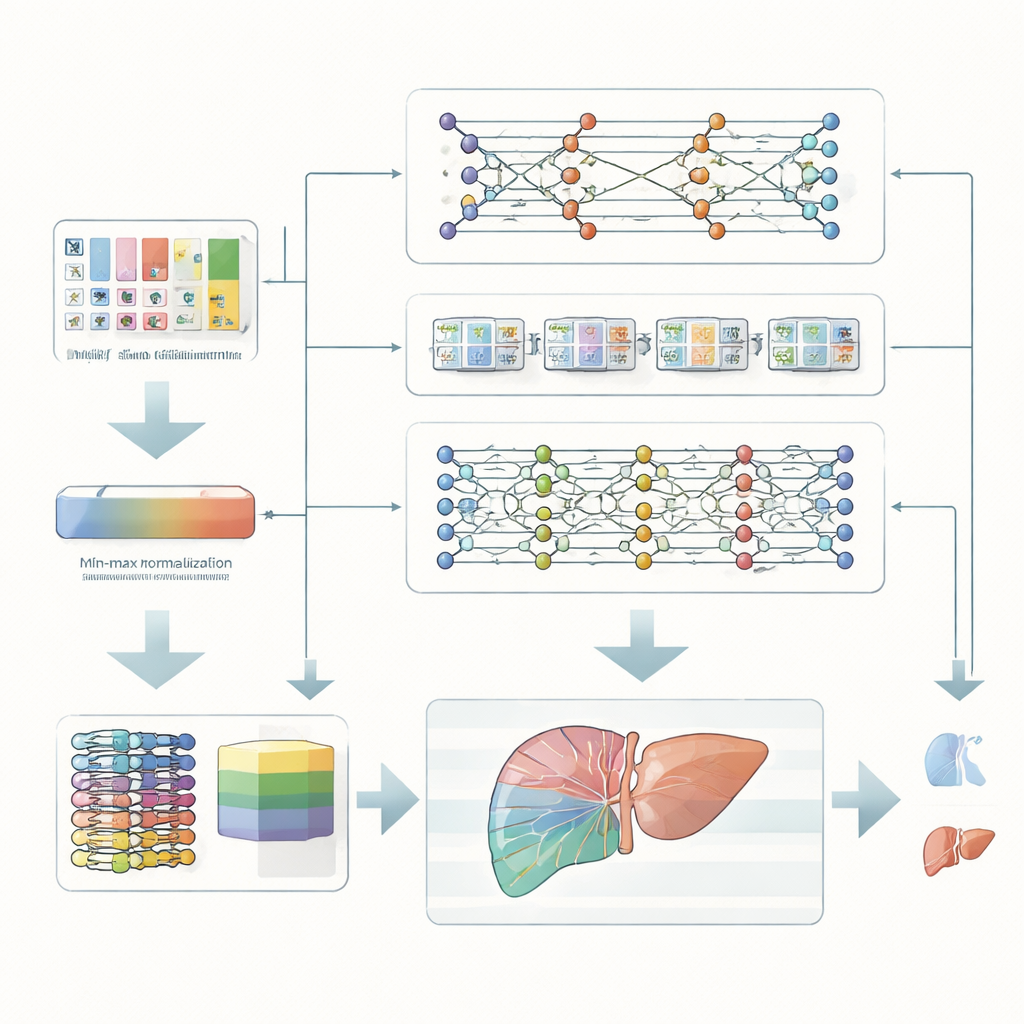
Co to może znaczyć dla opieki nad pacjentem
Dla codziennej praktyki medycznej praca ta wskazuje na narzędzia decyzyjne, które są jednocześnie celne i zrozumiałe. System zbudowany w oparciu o te zasady mógłby pomóc oznaczać pacjentów wątrobowych, którzy cicho wchodzą w strefę zagrożenia na długo przed pojawieniem się objawów, wykorzystując dane już zbierane w wielu przychodniach. Jednocześnie jego wyjaśnienia — podkreślające, które wyniki badań i objawy kliniczne są najważniejsze dla konkretnej osoby — mogłyby wspierać lekarzy w dopracowywaniu planów leczenia i omawianiu ryzyka z pacjentami. Choć badanie nadal opiera się na stosunkowo niewielkim, jednorodnym zbiorze danych i pomija dane obrazowe oraz genetyczne, stanowi mapę drogową dla inteligentniejszych, bardziej przejrzystych modeli ryzyka nowotworowego, które przy większych i bardziej zróżnicowanych danych mogłyby pewnego dnia stać się rutynowymi sprzymierzeńcami w walce z rakiem wątroby.
Cytowanie: Alqaralleh, B.A.Y., Alksasbeh, M.Z., Kulakli, A. et al. An intelligent healthcare framework for hepatocellular carcinoma diagnosis based on aggregated learners from biomedical data utilising explainable artificial intelligence. Sci Rep 16, 9357 (2026). https://doi.org/10.1038/s41598-026-39871-z
Słowa kluczowe: rak wątroby, medyczna AI, wczesna diagnoza, wyjaśnialna AI, wsparcie decyzji klinicznych