Clear Sky Science · pl
Identyfikacja wieloomowych kluczowych celów dla osteogenicznej różnicowania ludzkich mezenchymalnych komórek zrębu szpiku kostnego pod wpływem stresu oksydacyjnego
Dlaczego zestresowane kości mają znaczenie
Wraz z wiekiem lub w przebiegu chorób przewlekłych, takich jak cukrzyca i osteoporoza, kości tracą zdolność do naprawy. Głównym winowajcą jest „stres oksydacyjny” – narastanie reaktywnych cząsteczek uszkadzających komórki. W badaniu postawiono praktyczne pytanie o istotnych implikacjach dla złamań i implantów kostnych: co dokładnie dzieje się wewnątrz ludzkich komórek macierzystych ze szpiku kostnego, gdy są narażone na stres oksydacyjny, i czy można znaleźć molekularny przełącznik, który pomoże im nadal tworzyć nową kość?
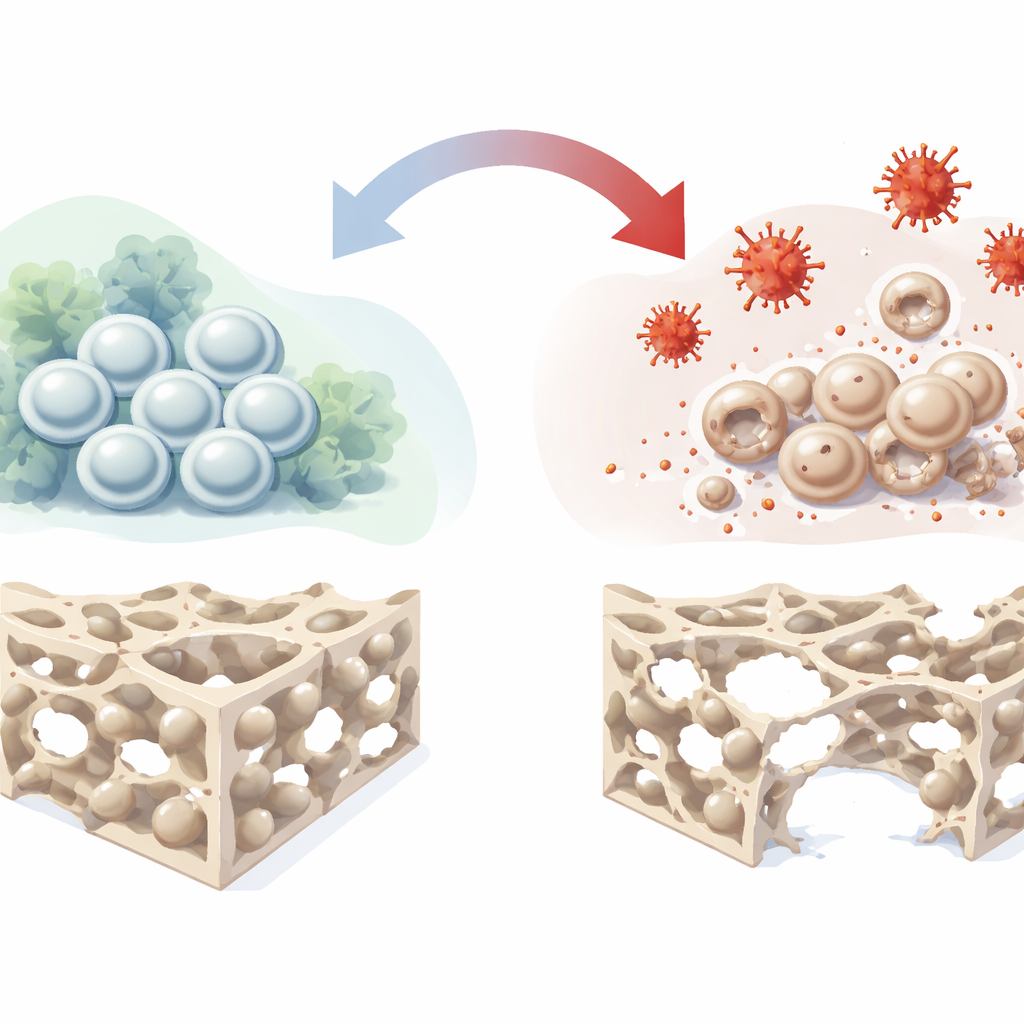
Komórki macierzyste, które budują kość
Głęboko wewnątrz naszych kości znajdują się mezenchymalne komórki zrębu szpiku kostnego — wszechstronna populacja, która potrafi odnawiać się i dojrzewać w komórki tworzące kość, chondrocyty oraz adipocyty. Ponieważ naturalnie uczestniczą w naprawie uszkodzonych tkanek, są jednym z głównych kandydatów do terapii następnej generacji naprawiających ubytki kostne i osteonekrózę. W rzeczywistych warunkach klinicznych te komórki często znajdują się w nieprzyjaznym środowisku o słabym ukrwieniu, niskim stężeniu tlenu, zapaleniu i stresie oksydacyjnym. W takich warunkach ich zdolność do przekształcania się w komórki kostne słabnie, co ogranicza powodzenie terapii opartych na komórkach macierzystych. Autorzy postanowili odtworzyć to nieprzyjazne środowisko w laboratorium i szczegółowo prześledzić, jak zaburza ono powstawanie kości.
Odtwarzanie surowego środowiska w laboratorium
Naukowcy użyli nadtlenku wodoru, powszechnego źródła reaktywnych form tlenu, aby wywołać stres oksydacyjny w hodowlach ludzkich komórek macierzystych ze szpiku kostnego. Starannie dawkowali substancję, aby znaleźć punkt, w którym komórki były zestresowane, ale nie zabite. Przy stężeniach do 400 mikromolarnych komórki zachowywały swój normalny wrzecionowaty kształt i pozostawały żywe, chociaż ich wewnętrzna chemia wyraźnie się zmieniła: wzrosły poziomy reaktywnych form tlenu, zaczęła się zmieniać funkcja mitochondriów, a równowaga między białkami związanymi z przeżyciem i śmiercią przesunęła się w kierunku adaptacji do stresu. Przy wyższych dawkach komórki traciły kształt i masowo umierały. Przy użyciu tolerowanego stężenia 400 mikromolarnych zespół następnie indukował różnicowanie kostne i obserwował zachodzące zmiany.
Jak stres blokuje tworzenie kości
Pod wpływem stresu oksydacyjnego zdolność komórek macierzystych do przekształcenia się w osteoblasty pogorszyła się w kilku uzupełniających się testach. Wczesna aktywność osteogeniczna, śledzona za pomocą enzymu fosfatazy alkalicznej, spadła wraz ze wzrostem stresu. Później, gdy komórki powinny były odkładać minerały, w naczyniach hodowlanych pojawiło się mniej i słabszych guzków wapniowych. Kluczowe geny i białka związane z kością, takie jak RUNX2 i osteopontyna, również zostały przyciszone. Aby zajrzeć „pod maskę”, naukowcy połączyli dwie potężne metody omiczne: sekwencjonowanie RNA, by określić, które geny były bardziej lub mniej aktywne, oraz szeroko zakrojoną analizę białek, by zobaczyć, które białka zmieniły obfitość. Razem te zbiory danych ujawniły setki przesunięć w kontroli cyklu komórkowego, zachowaniu chromosomów, metabolizmie i organizacji rusztowania otaczającego komórki, kreśląc obraz komórek macierzystych, których wewnętrzny rytm i wsparcie strukturalne zostały zaburzone przez stres oksydacyjny.
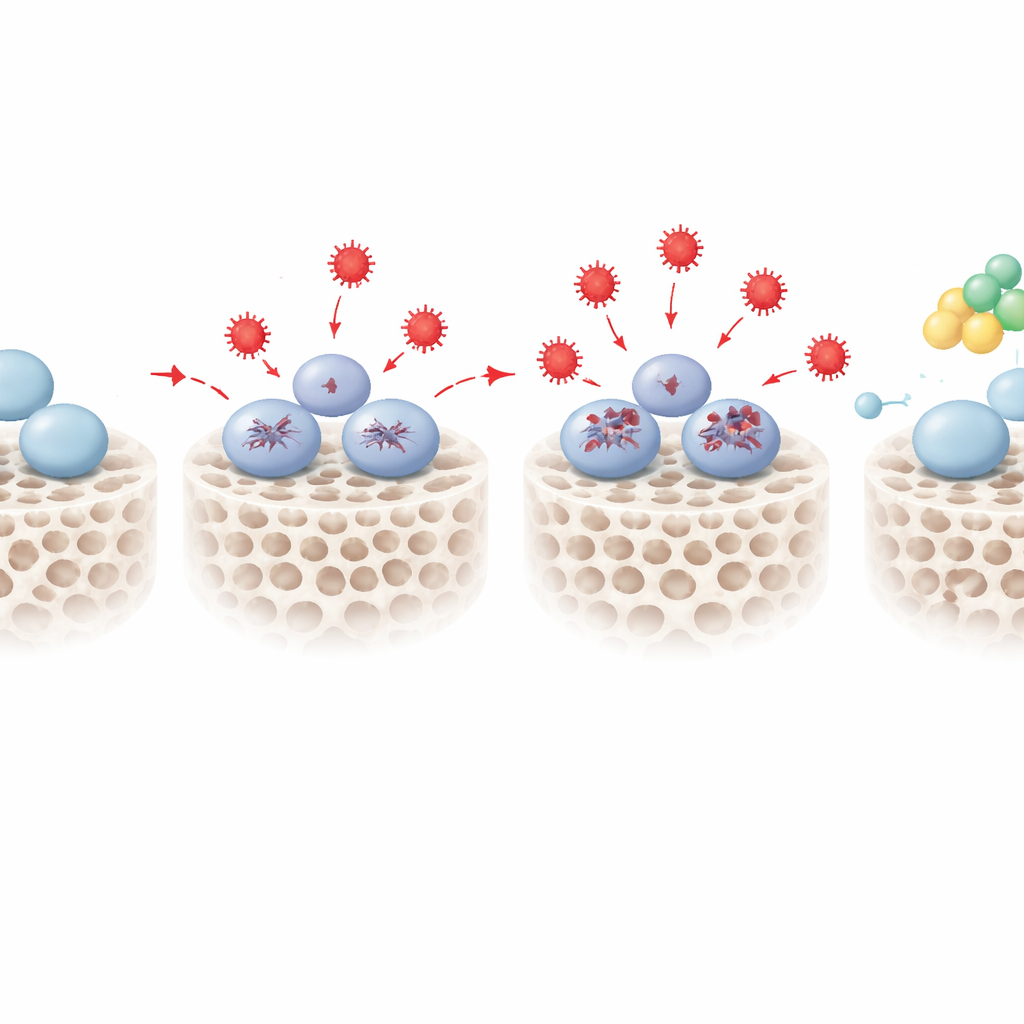
Odnalezienie ochronnego przełącznika o nazwie PENK
Poprzez nałożenie map RNA i białek zespół zawęził listę do 18 cząsteczek, które konsekwentnie zmieniały się w zestresowanych komórkach i były powiązane zarówno z odpowiedziami na stres, jak i z tworzeniem kości. Jeden z nich wyróżniał się: proenkefalina, czyli PENK, znana głównie jako prekursor naturalnych peptydów opioidowych. Pod wpływem stresu oksydacyjnego poziomy PENK rosły w sposób zależny od dawki. Gdy naukowcy sztucznie obniżyli ekspresję PENK przy użyciu narzędzi genetycznych, zestresowane komórki macierzyste jeszcze gorzej radziły sobie z tworzeniem kości, wykazując słabszą wczesną aktywność enzymatyczną i mniejsze odkładanie minerałów. Gdy zwiększyli poziom PENK, zaobserwowano efekt odwrotny: nawet w tych samych warunkach oksydacyjnych komórki odzyskiwały znaczną część zdolności do budowy zmineralizowanej macierzy kostnej. Dalsze analizy szlaków sygnałowych sugerowały, że PENK może działać poprzez modulację pewnych tras metabolicznych, w tym metabolizmu sfingolipidów, które łączą równowagę redoks z decyzjami o utrzymaniu potencjału komórki macierzystej lub przejściu na los kostny.
Co to oznacza dla przyszłej naprawy kości
Badanie pokazuje, że sam stres oksydacyjny wystarcza, by sparaliżować zdolność do tworzenia kości ludzkich komórek macierzystych ze szpiku kostnego, oraz identyfikuje PENK jako wbudowany czynnik ochronny, który pomaga im przeciwdziałać temu uszkodzeniu. Dla osób niebędących specjalistami przesłanie jest jasne: powodzenie terapii opartych na komórkach macierzystych będzie zależeć nie tylko od samych komórek, ale też od zestresowanego środowiska, w którym są umieszczane, oraz od molekularnych przełączników pomagających im sobie radzić. Wskazując PENK jako obiecujący cel, praca ta ukierunkowuje przyszłe badania nad lekami lub podejściami genowymi, które mogłyby wzmocnić naprawę kości u pacjentów, których tkanki są zanurzone w stresie oksydacyjnym — od osób starszych po chorych z przewlekłymi schorzeniami metabolicznymi lub zapalnymi.
Cytowanie: Dong, W., Zheng, Y., Zhou, Y. et al. Multi-omics identification of key targets for the osteogenic differentiation of human bone marrow mesenchymal stromal cells under oxidative stress. Sci Rep 16, 8215 (2026). https://doi.org/10.1038/s41598-026-39818-4
Słowa kluczowe: regeneracja kości, stres oksydacyjny, komórki macierzyste mezenchymalne, różnicowanie osteogeniczne, PENK