Clear Sky Science · pl
Wpływ utleniania RNA G-kwadrupaksów na ich dynamikę konformacyjną i interakcję z TDP-43 powiązanym z ALS
Dlaczego to ma znaczenie dla zdrowia nerwów
Stwardnienie zanikowe boczne (ALS) to choroba śmiertelna, w której komórki nerwowe kontrolujące ruch stopniowo obumierają, a przyczyny tej selektywnej szkody pozostają w dużej mierze niejasne. W tym badaniu postawiono proste, lecz istotne pytanie: czy wraz z wiekiem i narastającymi „rdzewiejącymi” uszkodzeniami chemicznymi w komórkach, zużycie to w RNA — funkcjonalnej kopii naszych genów — zaburza istotne sygnały, które utrzymują neurony ruchowe przy życiu? Skupiając się na specjalnym złożonym kształcie RNA i kluczowym białku związanym z ALS, TDP-43, praca ujawnia, jak drobne chemiczne blizny mogą przyczynić się do zapoczątkowania choroby. 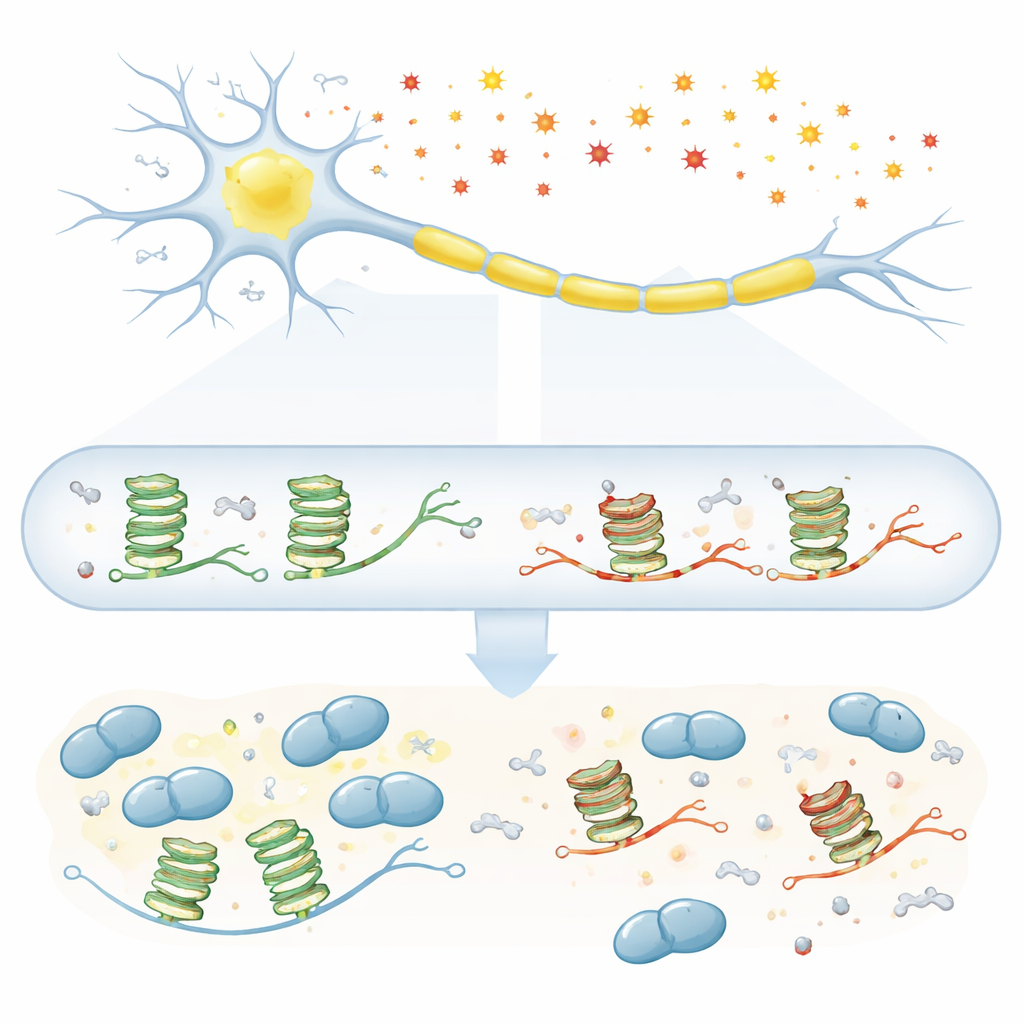
Delikatny supł RNA w centrum neuronów ruchowych
Neurony ruchowe polegają na dalekosiężnym transporcie komunikatów RNA wzdłuż aksonów, aby białka mogły być produkowane na miejscu, w pobliżu połączeń z mięśniami. Wiele z tych komunikatów zawiera specjalny strukturalny „supł” zwany G-kwadrupaksem, zbudowany z odcinków zawierających zasadę guaninę. Białka takie jak TDP-43 rozpoznają ten supł i przyczepiają RNA do granul transportowych poruszających się wzdłuż aksonu. Problem w tym, że guanina jest też najłatwiej ulegającą utlenieniu zasadą, gdy komórki są pod wpływem reaktywnych form tlenu, które kumulują się z wiekiem. Wcześniejsze wskazówki sugerowały, że G-kwadrupaksy i TDP-43 odgrywają centralną rolę w ALS, lecz nie było jasne, w jaki sposób utlenianie tych supłów RNA mogłoby zakłócać ich współpracę.
Obserwowanie, jak stres oksydacyjny deformuje kształty RNA
Naukowcy najpierw naświetlili ludzkie komórki neuroblastoma nadtlenkiem wodoru, powszechnym czynnikiem oksydacyjnym, a następnie zbadali stan struktur G-kwadrupaksów. Sygnały z sondy czułej na G-kwadrupaksy spadły wraz ze wzrostem stresu oksydacyjnego, co wskazywało, że te zwarte supły RNA tracą swój normalny kształt. Aby ustalić szczegóły chemiczne, zespół zsyntetyzował następnie RNA tworzące G-kwadrupaksy i celowo wprowadził różne ilości 8-oksoguaniny — dobrze znanej utlenionej formy guaniny występującej w starzejących się neuronach i tkankach ALS. Z wykorzystaniem szeregu narzędzi biofizycznych wykazali, że nawet umiarkowane poziomy tej modyfikacji poluzowują regularne układy stakowania G-kwadrupaksu, choć dokładny efekt zależy od otaczającego sekwencją RNA. 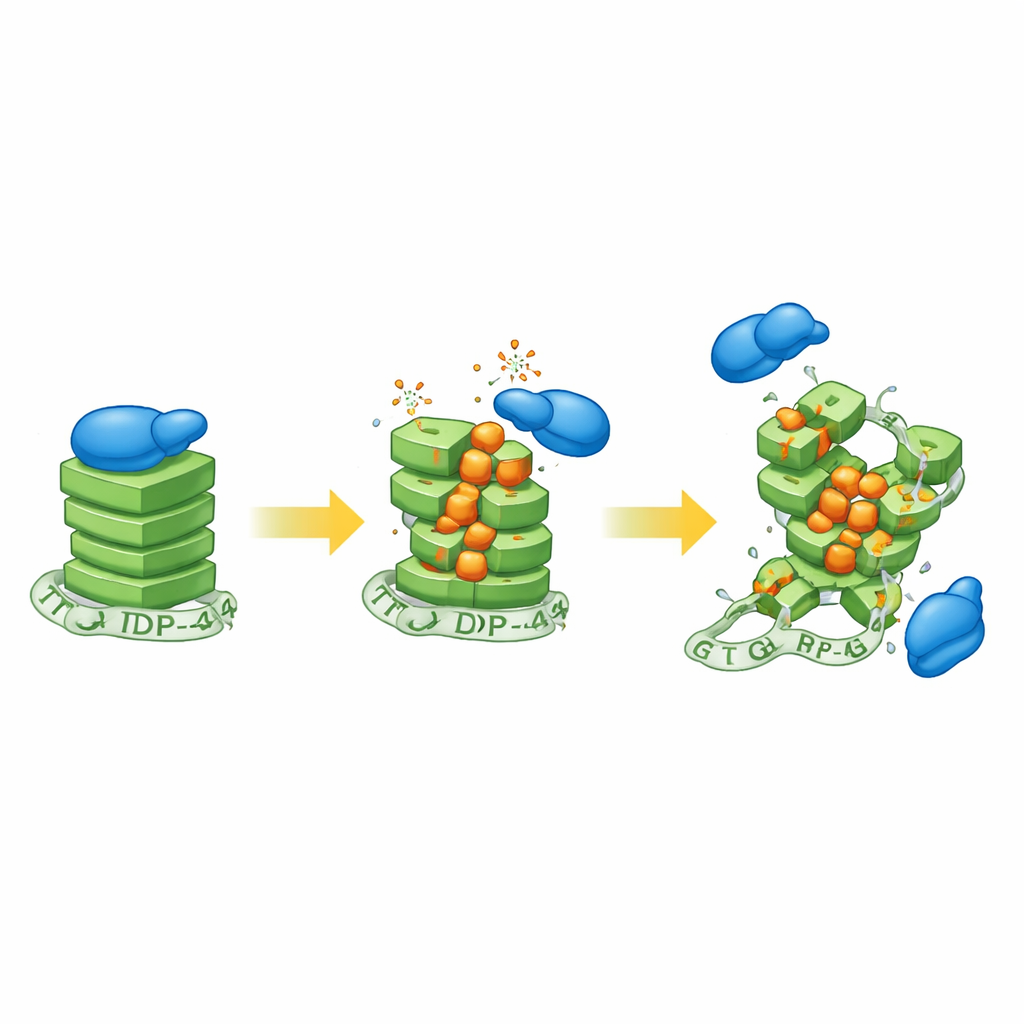
Nowe usterki: niedopasowane zasady i błędne parowania nici
Bardziej szczegółowa analiza ujawniła dwa odrębne typy problemów strukturalnych. W jednym G-kwadrupaksie pochodzącym z komunikatu PSD-95 utlenione guaniny miały skłonność do nieprawidłowego łączenia się z pobliskimi adeninami, tworząc „niedopasowania”, które subtelnie deformowały fałd. Te niedopasowania pojawiały się najłatwiej przy pośrednich poziomach utlenienia, gdy RNA wciąż mogło przejściowo składać się w G-kwadrupaks, co doprowadzało do zetknięcia niewłaściwych partnerów. W innym G-kwadrupaksie pochodzącym z komunikatu CaMKIIα silne utlenienie destabilizowało zwykły wewnątrzcząsteczkowy supł tak mocno, że pozostałe nieuszkodzone guaniny szukały partnerów na innych nićiach RNA, sprzyjając tworzeniu nietypowych międzycząsteczkowych G-kwadrupaksów. Takie źle połączone struktury mogły zaplątać różne RNA ze sobą i zakłócać normalny ruch RNA wewnątrz neuronów.
Kiedy uszkodzone RNA traci swego partnera białkowego
Badanie następnie zbadało, jak te zdeformowane supły wchodzą w interakcję z TDP-43. Przy użyciu żelowych testów wiązania wykazano, że TDP-43 zdecydowanie preferuje nienaruszone, równoległe G-kwadrupaksy i coraz słabiej wiąże się w miarę wprowadzania kolejnych utlenionych zasad. Struktura CaMKIIα, już bardzo ciasna, okazała się szczególnie wrażliwa: nawet niskie utlenienie niemal całkowicie znosiło wiązanie z TDP-43. Drugie białko, FUS — również powiązane z ALS — wykazało podobną, lecz nieco mniej dotkliwą utratę powinowactwa, co sugeruje, że utlenianie ogólnie osłabia chwyt białek wiążących G-kwadrupaksy. Co ciekawe, gdy TDP-43 mieszano z łagodnie utlenionym RNA, dane wskazywały, że białko angażowało niestabilną formę przejściową G-kwadrupaksu, a nie w pełni złożony supł, sugerując dynamiczną walkę między stabilizacją a rozpadem.
Dodatkowa wrażliwość w mutacjach TDP-43 związanych z ALS
Praca dodatkowo przebadała dziesięć wariantów TDP-43 znalezionych u pacjentów z ALS, z których większość niesie zmiany w elastycznym, bogatym w glicynę ogonie, który dopracowuje rozpoznawanie RNA. Wszystkie te mutacje już wiązały normalne G-kwadrupaksy słabiej niż białko typu dzikiego. Gdy wprowadzono utlenione G-kwadrupaksowe RNA jako konkurentów, mutanty były jeszcze mniej zdolne niż białko normalne do rozpoznawania i wiązania uszkodzonych struktur. Niektóre warianty zlokalizowane w szczególnie podatnych na nieuporządkowanie regionach były najbardziej dotknięte. Sugeruje to podwójny cios u starzejących się osób noszących takie mutacje: TDP-43 jest nie tylko z natury mniej skuteczne, ale utlenianie RNA związane z wiekiem dodatkowo osłabia jego zdolność do opiekowania się kluczowymi komunikatami wzdłuż aksonów neuronów ruchowych.
Co to oznacza dla zrozumienia ALS
Mówiąc krótko, badanie pokazuje, że napędzane wiekiem uszkodzenia chemiczne przekształcają delikatne supły RNA, które kierują transportem komunikatów w neuronach ruchowych, i że zniekształcone supły przestają dobrze współpracować z TDP-43 i pokrewnymi białkami. Skutkiem jest większe prawdopodobieństwo źle skierowanych lub zablokowanych ładunków RNA, dokładnie w długich, wrażliwych aksonach, które utrzymują kontrolę nad mięśniami. U osób dziedziczących mutacje TDP-43, osłabienie interakcji RNA–białko wywołane utlenianiem może przybliżać już zestresowane neurony do awarii. Poprzez naświetlenie tego subtelnego, lecz silnego łańcucha zdarzeń — od stresu oksydacyjnego po zmienioną architekturę RNA i zaburzony transport — praca wskazuje utlenianie RNA G-kwadrupaksów jako obiecujące molekularne ogniwo łączące starzenie z ALS oraz potencjalny cel przyszłych terapii ochronnych.
Cytowanie: Ishiguro, A. Impact of G-quadruplex RNA oxidation on its conformational dynamics and interaction with ALS-associated TDP-43. Sci Rep 16, 8802 (2026). https://doi.org/10.1038/s41598-026-39767-y
Słowa kluczowe: stwardnienie zanikowe boczne, utlenianie RNA, G-kwadrupaks, TDP-43, degeneracja neuronu ruchowego