Clear Sky Science · pl
Identyfikacja markerów związanych z uszkodzeniem bariery krew–mózg w przebiegu zawału mózgu przy użyciu analizy transkryptomicznej
Dlaczego ma to znaczenie dla udaru i zdrowia mózgu
Gdy u kogoś dochodzi do udaru spowodowanego zatorem naczynia mózgowego, lekarze widzą uszkodzenia na obrazach, ale wciąż mają trudności z przewidzeniem, kto rozwinie większe obrzęki, krwawienie lub trwałą niepełnosprawność. Duża część tego uszkodzenia zachodzi w ochronnym strażniku mózgu — barierze krew–mózg, która normalnie zapobiega przedostawaniu się szkodliwych substancji z krwi do delikatnej tkanki nerwowej. W badaniu postawiono proste, lecz ważne pytanie: czy istnieją molekularne sygnały, które ujawniają, kiedy ta bariera ulega naruszeniu, i czy sygnały te mogłyby w przyszłości poprawić diagnostykę i leczenie pacjentów po udarze?
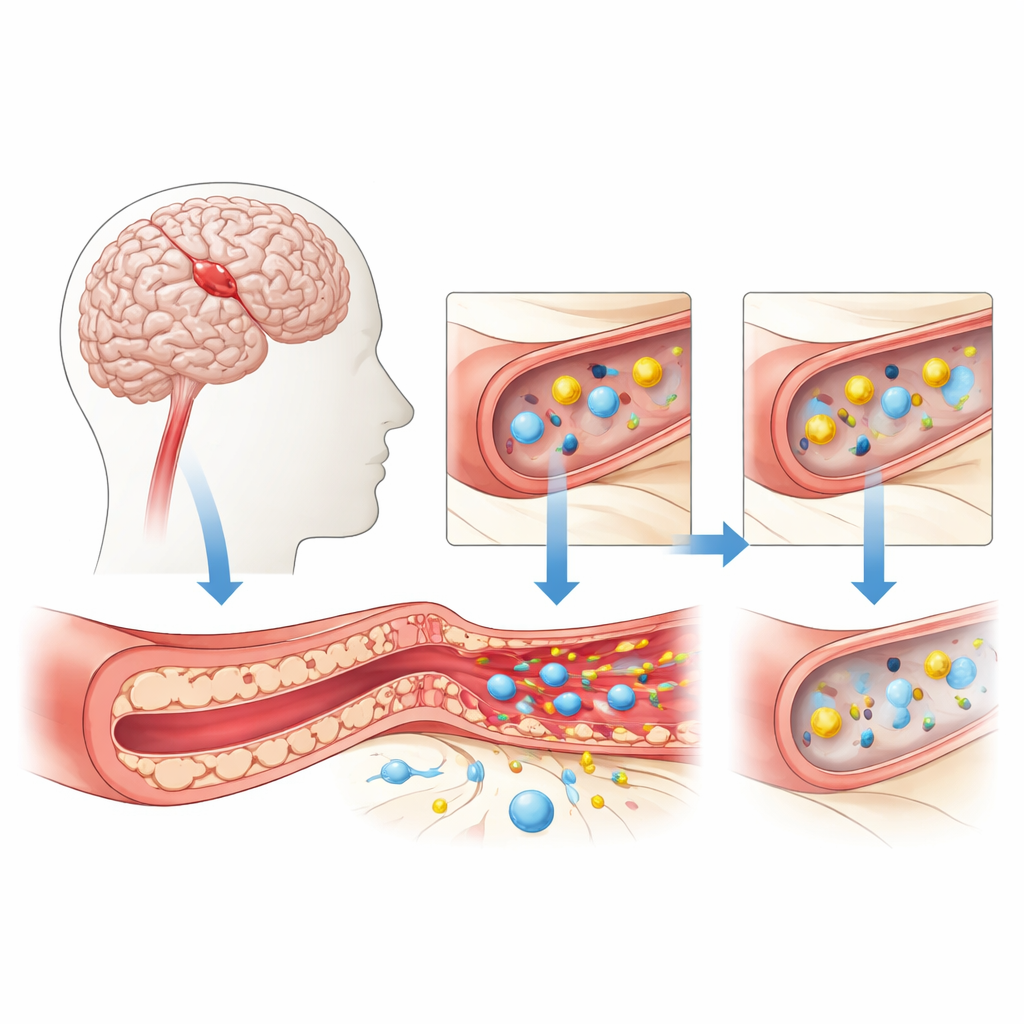
Ochronna brama mózgu pod obciążeniem
Bariera krew–mózg powstaje z ciasno do siebie przylegających komórek wyściełających drobne naczynia krwionośne mózgu. Komórki te precyzyjnie regulują, co może przejść z krwi do mózgu — wpuszczają niezbędne składniki, takie jak tlen i glukoza, a blokują toksyny i komórki układu odpornościowego, które mogłyby wyrządzić szkody. Podczas zawału mózgu, czyli udaru niedokrwiennego, przepływ krwi nagle spada. Bez wystarczającej ilości tlenu i cukru komórki wyściełające naczynia ulegają stresowi i zaczynają tracić szczelność. Pomiędzy nimi pojawiają się szczeliny, płyn przesiąka do otaczającej tkanki, a miejsce ogarniają mediatory zapalenia — wszystko to może nasilić obrzęk i uszkodzenie mózgu.
Odtworzenie uszkodzeń udarowych w laboratorium
Aby zbadać, co dzieje się w tych komórkach bariery, badacze użyli dobrze opisanej ludzkiej linii komórkowej imitującej wyściółkę naczyń mózgowych. Poddali te komórki warunkom o niskiej zawartości tlenu i braku glukozy — tzw. deprywacji tlenu i glukozy — aby naśladować stan udaru, a następnie przywrócili normalne warunki, by odwzorować leczenie i regenerację. Mierzyli przeżywalność komórek, uwalnianie enzymu wskazującego na uszkodzenie komórek oraz wydzielanie cząsteczek zapalnych. Jak można było się spodziewać, stresujące warunki pogorszyły kondycję komórek, zwiększyły sygnały zapalne takie jak IL-1β, IL-6 i TNF-α oraz zwiększyły wypływ markera uszkodzenia LDH. Po przywróceniu tlenu i składników odżywczych wiele z tych szkodliwych zmian osłabło, a komórki odzyskały częściowo zdolność do tworzenia struktur przypominających naczynia w teście wzrostu.
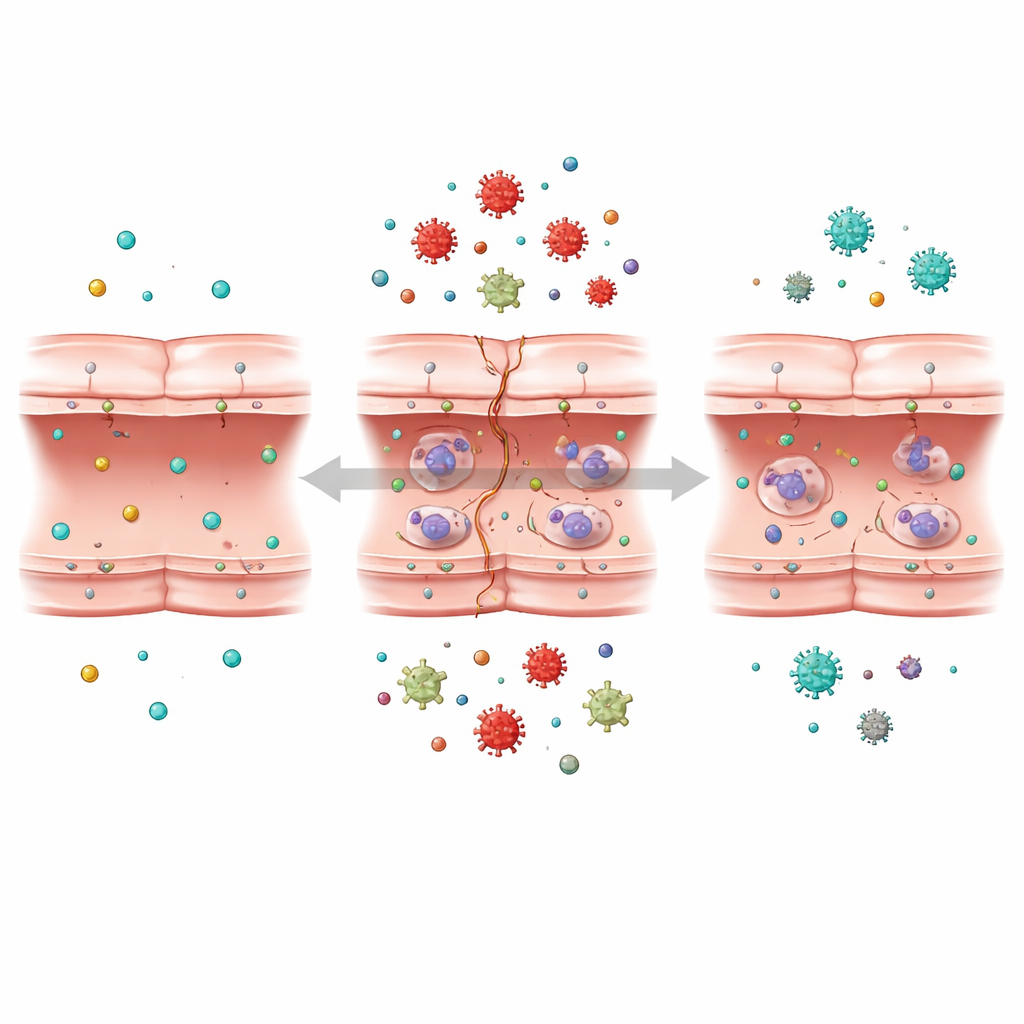
Nasłuchiwanie molekularnej rozmowy komórki
Zespół sięgnął następnie po potężną technikę zwaną transkryptomiką, która odczytuje poziomy aktywności tysięcy genów jednocześnie. Porównując komórki normalne, poddane deprywacji tlenu i glukozy oraz te dopuścnione do regeneracji, zidentyfikowali ponad tysiąc genów, których aktywność zmieniała się w odpowiedzi na stres przypominający udar. Przy użyciu zaawansowanych narzędzi analitycznych i uczenia maszynowego pogrupowali geny o podobnym zachowaniu i wyszukali te najsilniej powiązane z uszkodzeniem bariery. Wykazali, że wiele z najbardziej dotkniętych genów było związanych z trzema kluczowymi strukturami wewnątrzkomórkowymi: rybosomem, który syntetyzuje białka; siateczką śródplazmatyczną, która pomaga w fałdowaniu i obróbce białek; oraz mitochondriami, małymi elektrowniami dostarczającymi energię.
Rybosomy jako wyraźne sygnały
Z tej rozbudowanej puli genów badacze użyli algorytmu random forest — rodzaju uczenia maszynowego opartego na drzewach decyzyjnych — aby zawęzić listę do krótkiego zestawu szczególnie informacyjnych genów. Następnie zmapowali interakcje między odpowiadającymi im białkami. Analiza wyróżniła sześć genów kluczowych, z których większość wiązała się z rybosomem, fabryką białek komórki. W warunkach przypominających udar te geny związane z rybosomem były silniej aktywowane, a ich aktywność wracała w kierunku normy po przywróceniu tlenu i glukozy. Schemat ten sugeruje, że zmiany w maszynerii produkcji białek komórki mogą stanowić czuły, wczesny sygnał uszkodzenia i regeneracji bariery krew–mózg.
Co to może oznaczać dla przyszłej opieki
Dla czytelnika niezwiązanego z medycyną kluczowa informacja jest taka, że badanie wskazuje na nową klasę molekularnych „kontrolnych lampek ostrzegawczych”, które zapalają się, gdy bariera ochronna mózgu zostaje uszkodzona podczas udaru. Zamiast skupiać się wyłącznie na dobrze znanych winowajcach, takich jak enzymy degradujące ścianę naczynia, praca pokazuje, że wewnętrzne fabryki białek komórki intensywnie reagują na uraz i uspokajają się po poprawie warunków. Jeśli dalsze badania potwierdzą, że te markery związane z rybosomami można wykryć w próbkach pacjentów, na przykład we krwi, lekarze mogliby kiedyś używać ich do oceny stopnia uszkodzenia bariery, do wyznaczania optymalnego czasu terapii przeciwzapalnych i przeciwobrzękowych oraz do testowania nowych leków mających na celu ochronę tego kluczowego strażnika zdrowia mózgu.
Cytowanie: Liu, X., He, Y., Zhang, N. et al. Identification of blood-brain barrier injury-related biomarkers in cerebral infarction using transcriptomic analysis. Sci Rep 16, 8119 (2026). https://doi.org/10.1038/s41598-026-39763-2
Słowa kluczowe: udar niedokrwienny, bariera krew–mózg, markery, geny rybosomalne, komórki śródbłonka