Clear Sky Science · pl
Kolonizacja nowotworów przez bakterie napędza aktywację odporności i skuteczność blokady punktów kontrolnych
Dlaczego mali lokatorzy w guzach mają znaczenie
Leczenie nowotworów zostało zrewolucjonizowane przez immunoterapie, które uwalniają komórki odpornościowe organizmu przeciwko guzom. Mimo to wielu pacjentów odnosi niewielkie korzyści, a przewidzenie, kto zareaguje, pozostaje trudne. Badanie to analizuje nieoczekiwanego gracza, który może przechylić szalę: bakterie żyjące bezpośrednio w guzach. Na modelach mysich autorzy pokazują, że ci mikroskopijni lokatorzy mogą zmieniać zachowanie układu odpornościowego w obrębie guza i wokół niego, a w efekcie wpływać na to, czy powszechnie stosowana immunoterapia zwana przeciw–PD-1 zadziała skutecznie, czy zawiedzie.
Ukryte bakterie wewnątrz guzów
Przez lata największą uwagę poświęcano bilionom mikroorganizmów w jelitach i ich wpływowi na ogólną odporność. W ostatnim czasie naukowcy odkryli, że wiele ludzkich guzów również skrywa niewielkie, lecz aktywne społeczności bakteryjne. Zespół stojący za tym badaniem postawił dwa podstawowe pytania: czy powszechnie używane mysie modele nowotworowe także zawierają bakterie i, jeśli tak, czy te bakterie rzeczywiście wpływają na wzrost guza i odpowiedź na leczenie? Porównali dwa modele: MCA-205, rodzaj mięsaka, oraz MOC1, model raka głowy i szyi. Za pomocą testów opartych na DNA, sekwencjonowania i metod hodowlanych wykazali, że guzy MCA-205 konsekwentnie zawierały żywe bakterie, podczas gdy guzy MOC1 ich nie miały, nawet gdy znajdowały się w bakteryjnie bogatej jamie ustnej. W MCA-205 poziomy bakterii miały tendencję do wzrostu wraz z powiększaniem się guzów, co sugeruje, że rosnący guz zapewniał korzystne siedlisko dla mikroorganizmów.
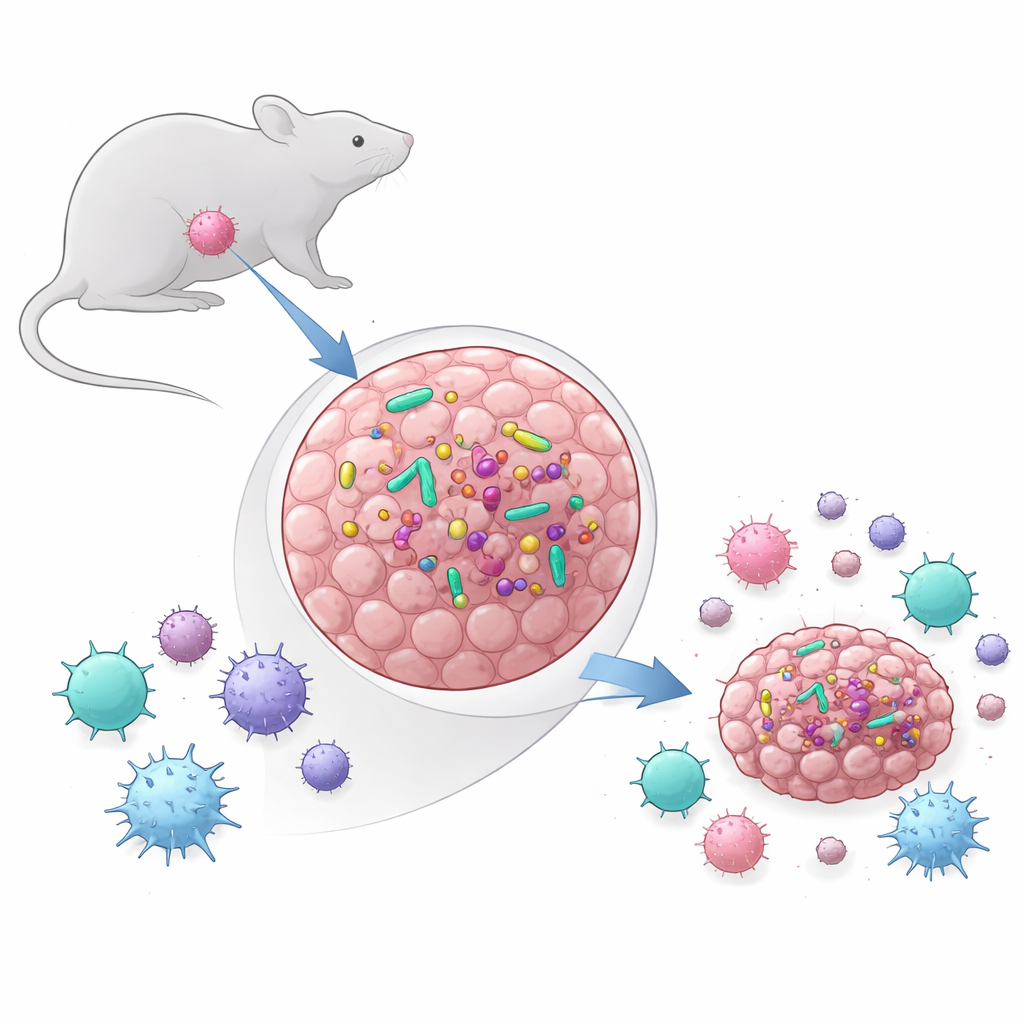
Śledzenie, skąd pochodzą drobnoustroje
Odkrycie bakterii wewnątrz guzów rodziło kolejne pytanie: czy te najeźdźcy pochodzą ze skóry, jamy ustnej czy jelit? Porównując DNA bakteryjne z guzów z próbkami kału, wymazami skóry i jamy ustnej, badacze ustalili, że społeczność wewnątrztumorowa była prostsza i mniej zróżnicowana niż bogate ekosystemy jelit i ust. Większość rodzajów bakterii w guzach pokrywała się z tymi obserwowanymi w przewodzie pokarmowym, a stosunkowo niewiele odpowiadało bakteriom skóry. Sugeruje to, że bakterie mogą przeciekać z jelit lub jamy ustnej do krwiobiegu, a następnie kolonizować guz, w którym tylko niektóre gatunki potrafią przetrwać. Skład grup bakteryjnych odzwierciedlał te opisywane w kilku nowotworach ludzkich, co wzmacnia tezę, że mysie guzy mogą modelować rzeczywiste interakcje między guzami a mikrobiomem.
Jak bakterie w guzie kształtują skuteczność immunoterapii
Głównym odkryciem badania jest to, że bakterie zasiedlające guzy mogą przesądzać o sukcesie terapii przeciw–PD-1, inhibitora punktu kontrolnego mającego na celu przywrócenie aktywności wyczerpanych limfocytów T cytotoksycznych. Gdy zespół zastosował antybiotyki przenikające do guza i usuwające lokalne bakterie przy jednoczesnym względnym oszczędzeniu kolonizacji jelit, guzy MCA-205 stały się znacznie mniej wrażliwe na przeciw–PD-1. Odpowiedzi spadły jeszcze bardziej, gdy mikrobiota jelit została szeroko zakłócona. Natomiast w guzach MOC1, które od początku nie wykazywały wykrywalnych bakterii, antybiotyki nie miały większego wpływu ani na ładunek bakteryjny, ani na wynik leczenia. W MCA-205 guzy, które zmniejszały się w odpowiedzi na przeciw–PD-1, zwykle zawierały więcej bakterii niż te oporne na terapię, co łączy wysokie wewnątrztumorowe obciążenie bakteriami z lepszą kontrolą wzrostu.
Wnętrze frontu walki immunologicznej
Aby zrozumieć, jak bakterie przechylają równowagę immunologiczną, badacze przeanalizowali komórki odpornościowe wewnątrz i wokół guzów. Gdy bakterie wewnątrztumorowe usunięto za pomocą antybiotyków penetrujących guz, do guza napływało mniej cytotoksycznych limfocytów CD8, a stosunek tych komórek do limfocytów T regulatorowych przesunął się na stronę supresji. Komórki dendrytyczne, zwiadowcy pobierający materiał guza i aktywujący limfocyty T, również występowały w mniejszej liczbie i wykazywały niższe oznaki aktywacji przy braku bakterii. Co ciekawe, samo dodanie szczepu niepatogennego Escherichia coli do guza lub wyłączenie głównej ścieżki wykrywania drobnoustrojów (MyD88) w kluczowych komórkach odpornościowych nie poprawiło terapii. Sugeruje to, że nie wystarczy dowolna obecność bakterii ani proste sygnały alarmowe; prawdopodobnie wymagane są specyficzne społeczności i bardziej zniuansowana komunikacja z układem odpornościowym.
Co to oznacza dla przyszłej opieki onkologicznej
Dla osoby niebędącej specjalistą wniosek jest taki, że bakterie żyjące w guzach nie są jedynie biernymi obserwatorami. W przynajmniej niektórych nowotworach pomagają one przyciągnąć odpowiednie komórki odpornościowe do guza i wspierać działanie leków przeciw–PD-1. Inne guzy mogą pozostać niemal wolne od bakterii i reagować zupełnie inaczej. Projektując i testując nowe terapie na myszach, wiedza o tym, czy dany model guza nosi bakterie — i jakie to rodzaje — może być niezbędna do prawidłowej interpretacji wyników i wyboru strategii, które przełożą się na pacjentów. W dłuższej perspektywie precyzyjne strojeniе drobnych społeczności wewnątrz guzów mogłoby dołączyć do leków i komórek odpornościowych jako nowe narzędzie poprawy immunoterapii nowotworów.
Cytowanie: Rolig, A.S., Ziglari, T., McGee, G.H. et al. Bacterial colonization of tumors drives immune activation and checkpoint blockade efficacy. Sci Rep 16, 8464 (2026). https://doi.org/10.1038/s41598-026-39758-z
Słowa kluczowe: mikrobiota wewnątrztumorowa, immunoterapia nowotworów, przeciw-PD-1, mikrośrodowisko guza, bakterie i nowotwory